| 废旧镍氢电池浸出液除杂工艺研究 |
b. 江西理工大学, 机电工程学院, 江西 赣州 341000
b. Faculty of Mechanical and Electronic Engineering; Jiangxi University of Science and Technology, Ganzhou 341000, China
在文献[1-2]中曾对废旧镍氢电池正负极材料的浸出工艺条件和稀土回收做了报道, 经过浸出和稀土回收两段流程之后, 镍氢电池浸出母液中所含绝大部分为镍钴的硫酸化合物, 但同时还含有其他易溶于硫酸介质的其他杂质(Zn, Mn, Fe, Ca), 这些金属若不除去, 对镍、钴的后续分离, 镍、钴产品的质量都会造成影响, 另外还可以通过综合回收这些金属, 提高经济效益.
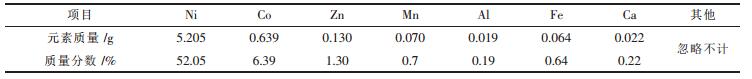
分别称取正负极废料各5g, 在适合工艺条件下通过硫酸浸出后[1-2], 送赣州有色冶金研究所进行检测后, 各元素的含量如表 1所示.
| 表 1 各金属元素的质量含量 |
 |
| 点击放大 |
1 黄钠铁矾法除铁
湿法冶金过程中, 除铁[3-4]的方法有:氢氧化铁法、亚硫酸盐法、磷酸盐法、赤铁矿法、针铁矿法和黄钾(钠)铁矾法等.其中, 黄钾(钠)铁矾法[5]应用较为广泛, 该法的优点是在常压下进行反应, 对设备无特殊要求, 且铁矾渣易于过滤和洗涤[6], 针对此原料拟采用该方法.
镍氢电池正负极废料经硫酸浸出后, 形成的多为二价的铁离子硫酸盐, 但形成铁矾时需要三价的铁离子[7], 所以在沉淀前首先要对Fe2+进行氧化使之变成Fe3+, 在原理上讲, 电位高于铁从三价变成二价的物质都可作为铁离子的氧化剂, 但从产品纯度考虑, 钠离子一般在后续工序中不容易沉淀且容易分离, 故选用NaC1O3做氧化剂, 发生的化学反应式为:
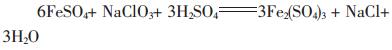
|
生成黄钠铁矾的反应十分复杂, 主要反应[8]为:
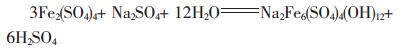
|
从以上反应式可看出, 反应过程中产生了酸, 而黄钠铁矾的生成需要在一定的pH值下进行, 所以必须用碱中和反应过程中产生的酸, 故加入Na2CO3做调节剂[9].
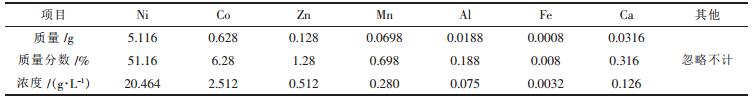
将200 mL的正负极浸出混合液搅拌后, 控制以下条件:用Na2CO3调pH值到1.3~1.6, 加热温度为92℃, 加入理论用量的2.5~3倍NaC1O3使Fe2+氧化成Fe3+, 用铁氰化钾检查二价铁的含量, 当Fe2+的含量 < 0.1mg/L时, 再缓慢加入8%的Na2CO3中和至pH值到1.7~1.9, 反应2h后, 过滤洗涤, 对除铁后的过滤液用ICP检查分析换算后, 结果如表 2所示.
| 表 2 黄钠铁矾法除铁后各金属含量 |
 |
| 点击放大 |
比较表 1和表 2结果可以看出, 用黄钠铁矾法对该浸出液的除铁效果比较理想, 体系中铁几乎全部除净.从镍钴的共沉淀率来看, 只有不到2%的金属随之流失, 也能达到较为理想的效果.实验的过程中, 金属Ca的含量有所上升, 这是因为使用的超纯水过滤洗涤时中不小心混进了少量含钙的普通水, 以后实验可通过实验操作避免.
2 P204萃取深度净化除其他杂质实验在进行除铁工艺后, 根据表 2知, 混合液中还含有少量的Zn, Mn, Ca等杂质, 这些杂质可以用普通的化学法分类将它们除去, 如加NaF除Ca[10], 过硫酸铵法除锰[11]等, 但针对本原料, 若想一次性将这些杂质深度除去, 那么溶剂萃取法是最有效的办法, 而在众多萃取剂中, P204(二-(2-乙基己基)磷酸)已被证明是最经济实用有效的萃取剂.
2.1 实验方案在进行P204萃取除杂实验之前, 必须找到适宜的实验条件, 选定温度时, 结合刘晓剑等[12]人的实验, 证明了用P204萃取剂萃取锰钙等金属时, 温度影响很小, 为节约成本, 本实验在室温下进行; 对其他因素, 通过计算选定萃取剂浓度, 再对pH值、相比和皂化率等几个主要因素进行逐一单因素实验以确定实验条件.
2.2 实验试剂与仪器试剂:回收稀土和除铁后的正负极混合浸出液, P204, 市售煤油, 氢氧化钠溶液.
仪器:分液漏斗、量筒、玻璃棒、烧杯、ⅡXSP型ICP分析检测仪、pH值检测笔.
3 结果与讨论(1) 萃取剂浓度选择.当料液中金属离子浓度一定且其他条件保持不变时, 萃取因数E随萃取剂浓度增加而提高[13-14].但萃取剂的浓度不是越高越好, 浓度太高会使黏度增加, 使分相困难, 从而造成金属的损失或者除杂不净, 特别是对多级萃取, 萃取剂的浓度可适当降低.在大概选择萃取剂浓度之前, 先进行萃取容量实验计算:
对杂质Zn2+: 2Na(R2PO4)+Zn2+ → Zn(R2PO4)2+ 2Na+
一般市场上所售的P204萃取剂的分子量为322.4, 当P204皂化率为100%时, 则1g P204能萃取Zn2+= 65/(2×344.4)= 0.094 g, 则用1L10%含量P204, 比重= 0.97, 纯度93%, 皂化率为70%, 相比O/A=1:1时, 其萃取容量为:
0.1×0.094×0.97×0.93×0.7×1000 = 5.93 g/L
可以看出, 萃取Zn的最大饱和容量为5.93 g/L, 一般萃取时取80%左右最大容量进行操作[13], 而实验原料试剂中所有杂质金属总量都不会超过2g/L的浓度, 所以选择体积比为10%的P204-煤油溶液萃取剂浓度作为实验萃取剂浓度.
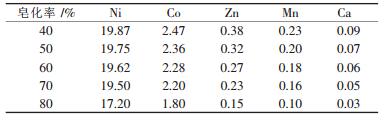
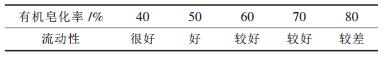
(2) 皂化率的选择.固定下列条件:有机相组成为10% P204+煤油, 水相pH值3.5~4, 相比A/O=1:1, 加入不同的NaOH数量, 在6组不同的皂化率下分别进行1级萃取实验, 当3min后, 通过ICP测定萃余液的成分和体系的特性分别如表 3和表 4所示.由表 3知, 进行1级萃取实验时, 随着皂化率的增大, 各金属的萃取量都在增大, 但当皂化率在80%时, 由于流动性变差, 两相分离较为困难, 造成金属的损失.故从体系的流动性和萃取效果来看, 选择70%的皂化率较为适宜.
| 表 3 不同皂化率下萃余液中各金属的浓度/(g·L-1) |
 |
| 点击放大 |
| 表 4 不同皂化率下体系的流动性 |
 |
| 点击放大 |
(3) 相比、pH值和萃取时间等条件选择.固定其他条件, 被考察因素条件取不同水平(考察相比影响时, 指定有机相组成:10% P204+煤油, pH值3.5~4, 皂化率70%, 萃取时间3min; 考察时间影响时, 将萃取时间换成相比(A/O)为2:1, 其他条件同上; 同理固定条件考察pH影响), 所得结果如表 5、表 6、表 7所示.
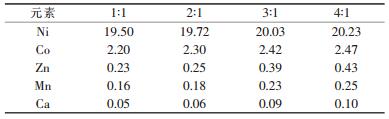
| 表 5 不同相比(A/O)时萃余液中各金属的浓度/(g·L-1) |
 |
| 点击放大 |
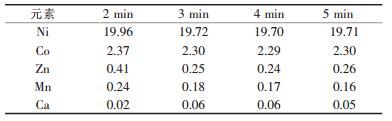
| 表 6 不同时间下萃余液中各金属的浓度/(g·L-1) |
 |
| 点击放大 |
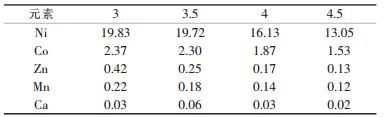
| 表 7 不同pH值时萃余液中各金属的浓度/(g·L-1) |
 |
| 点击放大 |
由表 5知, 相比(A/O)为1:1和2:1时, 镍钴和其他杂质金属的萃取相差不大, 而当相比增大到3:1以上时, 杂质金属萃取率明显下降.这是因为, 从P204萃取剂的最大萃取容量上看, 相比为2:1时仍然在其萃取容量范围之内, 而高于3:1时就会超出萃取容量, 从而达不到萃取分离杂质的效果.由表 6知, 萃取时间在3min时较为适宜, 3min之前萃取未进行完全, 3min之后再等待时间没有必要性.由表 7知, pH值是反应过程中最重要的一个影响因素, 其直接影响除杂效果和镍钴的损失, 从表 7中数据得出3.5的pH值被认为是较为理想的条件.
4 结论针对Ni-MH电池正负极废料浸出液成分特点, 除杂实验可得出如下结论:
(1) 利用黄钠铁矾法除铁完全可行, 除去率近99%, 同时镍钴的损失不到2%, 其实验条件为:溶解后pH值为1.3~1.6, 氧化前pH值为1.7~1.9, 除铁终点pH值为2~2.5, 反应温度92℃, 反应时间2 h.
(2) 通过单因素1级萃取实验, 找到了用P204萃取剂深度除杂的适宜条件, 分别为:有机相组成为10%P204+煤油, 皂化率为70%, 相比(A/O)为2:1, pH值为3.5, 萃取时间3min.
| [1] |
夏李斌, 罗俊, 田磊. 废旧镍氢电池正极浸出试验研究[J].
江西有色金属, 2009, 8(3): 16–18.
|
| [2] |
廖春发, 胡礼刚, 夏李斌. 废旧镍氢电池负极浸出液中稀土的回收[J].
湿法冶金, 2010(4): 7–9.
|
| [3] |
杨建华. 赤铁矿法处理锌浸出渣[J].
重有色冶炼, 2006(3): 36–36.
|
| [4] |
中南矿冶学院.
针铁矿法除铁技术资料[M]. 长沙: 中南矿冶学院出版社, 1977.
|
| [5] |
宋焕笔, 胡业藏. 用黄钾铁矾法从某铀矿浓酸浸出液中除铁的研究[J].
铀矿冶金, 2007, 16(1): 13–13.
|
| [6] |
Huggare L. The Application of Cobalt[J].
World Mining, 1994, 27(2): 36–42. |
| [7] |
王德全, 宋庆双, 彭瑞东. 用硫酸亚铁浸出同时沉淀铁矾法处理低品位锰矿[J].
东北大学学报:自然科学版, 1998(2): 45–47.
|
| [8] |
林娟. 钴溶液除铁的工艺改进[J].
山西冶金, 2004(4): 58–58.
|
| [9] |
张守卫, 谢曙斌, 徐爱东. 镍的资源、生产及消费状况[J].
世界有色金属, 2003(11): 23–25.
|
| [10] |
林才顺. 氟化钠去除钙镁工艺的影响因素分析与控制[J].
湖南冶金, 2003, 31(4): 36–38.
|
| [11] |
夏煜, 黄美松, 杨小中, 等. 用废Ni-MH电池正极材料制备电子级硫酸镍的研究[J].
矿冶工程, 2005, 25(4): 46–49.
|
| [12] |
刘晓剑. 镍钴二次资源回收过程溶液深度净化及材料制备研究[D]. 长沙: 中南大学, 2007.
http://cdmd.cnki.com.cn/Article/CDMD-10533-2007172736.htm |
| [13] |
杨佼庸, 刘大星.
萃取[M]. 北京: 冶金工业出版社: 1988.
|
| [14] |
李培植, 钟盛文. 不同锂配比Li [Ni1/3Co1/3Mn1/3]O2正极材料的合成与性能研究[J].
江西理工大学学报, 2008, 29(1): 76–78.
|
 2011, Vol. 2
2011, Vol. 2
