| 铜电解中添加剂的检测 |
铜的电解精炼,是对火法精炼所产粗铜阳极的进一步提纯,其最终目标是获得表面光滑、结晶致密、化学成分合格的阴极铜产品。铜电解生产中,在不增加生产设备的条件下,提高电流密度是增加产量、提高生产效率的最直接最有效的方法。然而,高电流密度下进行铜电解生产,对添加剂的准确控制有更高的要求,其加入量稍有不当就可能引起阴极表面粗糙、生长结瘤,甚至导致阴阳极间短路,使电流效率降低,电耗增加。因此,添加剂的准确控制,是获得优质阴极铜的重要保证。但目前,国内外铜电解生产企业主要还是通过人工观察阴极沉积物表面结晶情况,凭经验判断添加剂的加入量是否适当或需要调节。这不仅是滞后操作,而且调节的量常常偏离最佳值,尤其是当电解液成分波动、电流密度改变、电解液温度不稳以及添加剂质量有变化时,添加剂的控制靠人工调节更难把握。
图 1是铜电极的阴极极化曲线[1],当电流密度控制塔费尔区域(AB直线段)内,可获得致密的阴极铜;当电流密度超过塔费尔区域时,电解过程进入混合控制区,这将导致浓度梯度的存在,所得阴极铜表面晶粒会变粗,而且易长瘤和长刺。图 1中B点相应的电流密度为100 A/m2,而铜电解精炼通常所采用的电流密度为220~300 A/m2。可见,铜电极反应在实际生产条件下的电流密度是处在混合控制区,因此不易得到致密阴极沉积物。为了得到致密的电解铜,需要设法扩大塔费尔范围,增加电化学极化主要手段就是控制阴极交换电流或极化值。目前增加电化学极化最有效的方法是在电解液中添加有机表面活性物质。
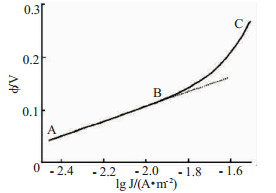 |
| 图 1 阴极过电位与电流密度的关系 |
铜电解精炼中,常用添加剂有明胶、硫脲以及盐酸,国外多数铜电解生产企业还添加阿维同、木质素磺酸钠等,国内只有少数企业使用。它们的加入量一般为每吨电铜几十克。在电解液中加入适量的添加剂,可以通过其在电极表面的吸附来改变电极反应的相关动力参数,从而改变阴极极化电位,达到细化结晶的效果。对于同一个电解系统而言,铜离子和硫酸浓度是相对较稳定的,添加剂必然成为影响阴极铜质量的主要因素。
2 明胶的测定明胶是由简单的天然蛋白质组成的长链氧基酸化合物的混合物,分子量为1.75~45万内变化。它是以胶的水溶液形式加入铜电解液中的。胶在酸性电解液中与铜离子形成络合物,Cu2+成为载胶体,受静电吸引而趋向阴极,以胶膜的形态吸附在阴极表面[2]。络合离子延缓了阴极放电,使阴极电化学极化增大,从而减小了阴极沉积物的晶粒尺寸并使沉积物的密度和硬度增大,抑制了阴极表面突出部分的电活性,使阴极表面平整光滑。随着明胶浓度的增加,阴极过电位迅速增大;明胶浓度超过30 mg/L后,电化学极化值就不再增加反而减小[3],而且胶粒分散度降低,可能会发生凝聚现象,降低铜离子在胶粒上的吸附能力,使阴极析出恶化。这说明,明胶的浓度只有在一定的范围内才有效。
2.1 明胶浓度的测定雷克润等[4]采用重铬酸钾氧化法,以浓硫酸做分析介质,饱和食盐水浴加热,用过量重铬酸钾定量氧化电解液中的明胶,再用亚铁盐标准溶液回滴剩余重铬酸钾,测定并计算出电解液中明胶的浓度。铜电解液中除氯离子外,其他组分均不干扰测定;当氯离子小于40 μg时也不干扰明胶的测定。
重铬酸钾氧化法的测定条件为:浓硫酸5~7 mL,沸水浴加热90 min以上或盐水浴加热50~60 min,氯离子小于40 μg时,直接测定明胶。该法简便,适用于一般电解液中明胶的测定,测定范围10~300 mg/L,相对标准偏差3.8 %。
然而,上述测定所需时间较长,而且测定结果是溶液中各种明胶分子的总浓度,并不是真正能起作用的活性胶浓度的真实体现,因此对明胶实时加入量的调整不能起到很好的指导作用。
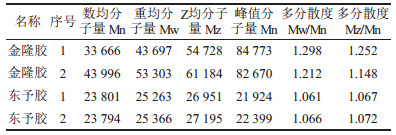
2.2 明胶分子量分布的测定张源等[5]采用凝胶过滤色谱法(GFC),使用紫外检测器(UV)和示差折光检测器(RI),分析了中国和日本的铜电解生产企业所用明胶的平均分子量和分子量分布。首先用RI测定明胶的各种分子浓度后,再经聚乙烯氧化物(PEO)换标得出平均分子量,所得结果见表 1。
| 表 1 中国和日本的铜电解生产企业所用明胶的平均分子量及分子量分布 |
 |
| 点击放大 |
用GFC法分析得到的明胶的分子量及其分布,可以真实体现明胶在铜电解液中的起始有效浓度,从而使铜电解控制水平又深入了一个层次。
3 硫脲的测定硫脲(SCN2H4)也是铜电解精炼中不可缺少的表面活性物质,它与明胶配合使用,主要起细化晶粒的作用。硫脲是一种还原剂,它可与Cu2+反应生成二硫化甲脒(H3N2CS-SCN2H3,简称FDS)和Cu+,Cu+还可与二硫化甲脒形成络合物。硫脲与CuSO4生成CuSO4- H2S-硫脲络合物[6],同时也可与Cu+生成络合物。硫脲及其生成的各种络合物,都能在铜阴极表面产生吸附,所形成的分子薄膜能降低固-液相间的界面张力,抑制阴极上活性区域的发展,从而使阴极表面光滑、结晶致密且有光泽。当硫脲浓度小于10 mg/L时,阴极铜含硫没有明显的变化;而当硫脲浓度高于10 mg/L时,可能造成阴极铜含硫量增加。控制好硫脲的用量,对于优化阴极铜产品品质,提高电流效率,降低生产成本,起到直接的影响作用。硫脲可增加阴极铜的密度。作用机理为:硫脲在酸性硫酸铜溶液中可以分解成SH-、硫脲衍生物、络合阴离子等,SH-、络合阴离子在电场作用下与Cu2+、Cu+、SO42-反应生成微晶沉积于阴极活性区铜结晶棱界面上,使电阻增大,从而引起阴极极化电位增大。同时由于此种微晶中较小原子嵌缀,还改变了铜的晶格结构,增加了阴极铜的密度[7]。
对电解液中硫脲浓度进行及时准确的测定,是铜电解生产企业十分关注的问题。由于铜电解液中Cu2+的大量存在,严重干扰了硫脲的测定,故用通常的方法无法准确测定电解液中的硫脲。早期对铜电解液中的硫脲常用萃取碘光度法、电化学法进行测定。这些分析方法过程复杂、时间较长而且灵敏度较低。
魏艳等[8]通过研究发现,硫脲在“乙二胺-KBrCu2+”(pH=10.2)底液中,示波极谱仪峰电位在-0.37 V(vs.SCE)上有一灵敏的二次导数电流峰,提出了在“乙二胺-KBr-Cu2+”底液中利用示波极谱测定微量硫脲的新方法。该法在溶液pH=11.5,KBr浓度0.16 mol/L,乙二胺浓度1.6 %的条件下,硫脲浓度在22.8~342 μg/L范围内,峰高与硫脲浓度有良好的线性关系,相关系数为0.999 9,检测下限达3.8 μg/L。
硫脲在“乙二胺-KBr-Cu2+”底液中的反应历程可能是:硫脲被溶液中的Cu2+氧化成二硫甲脒(FDS),FDS与过量的Cu2+形成(FDSCu)2+络合物,当有Br-离子存在时改变了其双电层结构,有利于带正电荷的(FDSCu)2+的吸附。在阴极扫描时,络合物中的FDS在电极上还原生成硫脲,从而产生高灵敏的吸附还原波。当KBr量为0.5~2.0 mL,Cu2+离子量为0.22~0.53 g/L,明胶量为0.05 g/L,Cl-离子为20 μg,温度在10~30 ℃之间时,峰值恒定且峰形正常。
考查了多种离子对测定76 μg/L硫脲的影响,其结果为:105倍的Cl-、SO42-、NO3-、NH4+,103倍的Fe3+、Fe2+、As5+、As3+、Sn2+、Ba2+、Ni2+,500倍的Pb2+,250倍的Co2+,200倍的Bi3+、Sb3+等对硫脲的测定均不产生影响。考虑到铜电解液中所含铁、铋、铅、锑均较大,采取先加氨水的办法,将它们以氢氧化物的形式沉淀下来,然后将溶液过滤,再取滤液进行分析检测,便可排除以上离子的干扰。铜电解液中金和硫的含量很少,可忽略不计。运用此法测定铜电解液中硫脲时,干扰因素少,可不经分离Cu2+离子而直接测定电解液中微量的硫脲。邵存权[9]也利用示波极谱法测定铜电解液中微量硫脲,进一步验证了实验方法的可靠性。
美国阿马里洛铜精炼厂发明的“添加剂控制法”[10],实质就是控制铜电解液中硫脲的浓度。他们认为电解槽出口的溶液中硫脲浓度控制在0.1~0.5 mg/L范围内可显著地提高电流效率,使阴阳极短路减少,阴极表面更加光滑,电解铜中所含杂质更低。显然,要控制电解液中硫脲浓度,快速、准确的硫脲分析方法是十分必要。
4 氯离子的测定盐酸是一种比较特殊的添加剂,微量的Cl-能与其他添加剂协同作用,增大阴极极化,从而影响电解铜表面的光亮度。它具有以下作用:Cl-与阳极溶解的Ag+生成AgCl沉淀,减少贵金属损失;Cl-与Cu+形成Cu2C12胶体对漂浮阳极泥具有共沉淀作用,从而减少阴极污染;Cl-还具有去极化作用,对由于铅、铋过高造成的阳极钝化具有活化作用。Cl-在硫酸溶液中本来能起活化作用,但因为CuC12在硫酸溶液中溶解度较小,所以Cl-浓度太高将产生有害的影响。
在含有硫脲或明胶-硫脲的硫酸铜溶液中,存在中等浓度的Cl-将使阴极沉积物的内应力最小,从而改善沉积物的性能。Cl-与硫脲形成[Cu(N2H4CS)]C12胶体沉淀,当硫脲浓度过低时,这种胶体会部分解析补充其不足;当这种胶体浓度过大时,会大量沉淀于槽底或粘附于阴、阳极,造成添加剂的损失,并且能引起槽电压升高。盐酸(Cl-)的加入量,一般视阳极杂质成分Ag、As、Bi及Sb含量而定。
4.1 氯化银比浊分光光度法准确分析铜电解液中的微量Cl-,对于优化阴极铜品质是十分必要的。资料显示,微量Cl-的测定方法主要有三种:①硫氢酸汞间接比色法[11]。②离子选择电极法。③氯化银目视比浊法。金川集团公司检测中心的梁玉霞等经过研究,确定了用乙醇作稳定剂以氢氧化钠沉淀分离主体元素Cu2+、Ni2+的氯化银比浊分光光度法。该法测定铜电解液中Cl-的具体操作为:选择400 g/L的NaOH溶液1 mL,放置15 min,加入1:1的硝酸10 mL,分析纯乙醇10 mL,0.1 mol/L的AgNO3溶液4 mL,放置15 min后,于3 cm比色皿中,以试样空白做参比,于7230型分光光度计在波长420 nm处测定其吸光度。通过共存离子的干扰试验,确定当被测溶液中存在104倍的SO42-、103倍的铜和镍、200倍的铁、25倍的明胶、硫脲、砷、锑、铋及碲时,不影响测定结果。该方法操作简便可靠,有良好的重现性及较高的准确性和精密度,有效地指导了生产实践。
4.2 硫氰化物容量法某铜电解生产企业采用“硝酸银-硫氰酸钾标液”滴定法,以Fe3+作为指示剂,测定铜电解中Cl-的含量。
具体操作为:在100 mL的铜电解液中加入1:1的硝酸5 mL、10 % AgNO3溶液5 mL和蒸馏水100 mL,加热煮沸数分钟后过滤。所得AgCl滤渣放瓷坩埚内600 ℃灰化并放冷。在原坩埚内,加5 mL浓硫酸,在电炉上驱赶Cl-至烟干,冷却后加1:1的硝酸10 mL,移至200 mL烧杯中洗净,并冷至室温。再加100 mL水,加10 %硫酸高铁铵溶液10 mL(作指示剂),用KSCN标液滴定至微红色,15 s内不退色为终点。该方法优点是,可以比较准确的测定铜电解液中的氯离子含量。但是操作比较繁琐和费时,也不可能及时体现铜电解液中Cl-的瞬时变化。
5 阴极过电位的在线监控在不同的电解条件(如温度、电流密度、金属离子浓度、添加剂)下,阴极过电位是电解液性质的实时反映。当电解液温度、硫酸及金属离子浓度等相对稳定时,添加剂是影响阴极过电位最显著的因素。通过对阴极过电位的在线监控[12, 13],在很大程度上可有助于调整和控制添加剂的加入量,使其维持在有利于优质阴极铜沉积的浓度范围。
李仕雄等[1]发明了“金属电积过程中在线监控有机添加剂的方法和装置”。通过对阴极过电位—添加剂浓度(加入量)—阴极铜品质三者间关系的研究得出:当阴极过电位在(51±0.5)mV时,可获得致密光滑的高纯阴极铜;当阴极过电位低于49 mV时,需增加添加剂加入量;当阴极过电位高于53 mV时,需减少添加剂加入量。此外,阴极电流效率随阴极过电位而改变,当阴极过电位为45 mV时,电流效率为97.48 %;当阴极过电位增加至51.25 mV时,电流效率为98.55 %;继续增加阴极过电位,电流效率反而降低。因此,通过监控阴极过电位并自动调节添加剂的加入量及浓度,维持最佳阴极过电位,可稳定产出高纯阴极铜,并维持优越的电流效率和技术经济指标。
铜电解过程中电解液质量工业监控的技术线路为:首先将添加剂溶解于槽中,以一定速度加入铜电解槽的进液系统,在电解液送往电解槽的过程中,通过计量装置抽取少许溶液送往阴极过电位在线检测仪进行在线检测。检测的阴极过电位送往智能仪表,与最佳过电位比较,当测定的阴极过电位低于最佳阴极过电位时,智能仪表自动控制执行器,加大添加剂的流量;当测定的阴极过电位高于最佳阴极过电位时,则自动减少添加剂的流量;当测定的阴极过电位与最佳阴极过电位相等时,则自动维持添加剂的流量不变。由于在线检测仪的溶液来自系列的进液系统,其成分和温度与系列电解槽的电解液相同,所以,在线检测仪检测的阴极过电位代表了系列所有电解槽阴极的电结晶特征。该技术使铜电解有机添加剂的控制由经验操作变为通过阴极过电位控制,将添加剂的控制由电沉积后的滞后调节变为电沉积前的超前控制。采用该专利技术测定铜基底上电解液的阴极过电位,可以快速准确地指示铜电解液的质量,并根据监测的电化学参数决定添加剂的最佳量,从而在线控制铜电解的阴极过程。
在铜电解精炼过程中添加剂对于保证电解铜质量常常起着至关重要的作用。因此,对各种添加剂作用机理的基础理论研究还需要深入;而对添加剂浓度的实时准确测定方法的研究也还需要加强。
| [1] |
李仕雄, 谢大元, 林升叨, 等. 铜电解添加剂的工业监控[J].
中国有色金属学报, 2004, 14(1): 132–136.
|
| [2] |
马朝庆. 铜电解精炼新型添加剂的实验研究[J].
有色矿冶, 2000(4): 32–34.
|
| [3] |
任忠文. 对电解铜箔生产明胶加入方法的讨论[J].
印刷电路信息, 2002(10): 31–32.
|
| [4] |
雷克润, 吴心传, 夏速萍. 铜电解液中明胶的测定[J].
湖南冶金, 1990(5): 36–37.
|
| [5] |
张源, 李国才. 明胶作为铜电解添加剂的研究与实践[J].
稀有金属, 2000, 24(1): 66–69.
|
| [6] |
董云会, 许珂敬, 刘曙光, 等. 硫脲在铜阴极电沉积中的作用[J].
中国有色金属学报, 1999, 9(2): 370–376.
|
| [7] |
陆湖南, 朱忠全. 添加剂对阴极铜质量的影响[J].
有色矿冶, 2005, 21(6): 33–35.
|
| [8] |
魏艳, 杨改霞, 黄宋献. 铜电解液中硫脲的测定[J].
湖南冶金, 1995(6): 51–53.
|
| [9] |
邵存权. 示波极谱法测定铜电解液中微量硫脲[J].
理化检验-化学分册, 1995, 31(3): 151–152.
|
| [10] |
Ramachandran V. The Electrorefiningand WiningofCopper [C]//The Metallurgical SocietyofAIME, TMS116thAnnualMeeting. NewYork:IntersciencePublishers, 1987:24-26.
|
| [11] |
白林山, 仇进. 硫氰酸汞吸光光度法同时测定水中微量氯离子及余氯[J].
理化检验-化学分册, 2001(6): 13–14.
|
| [12] |
Kerby R C, Jankola W A.Proceeding of international symposium on electrometallurgical plont practice [C]//elaesseens P L, Harris G B.Montreal:Pergamon Press, 1990:320-323.
|
| [13] |
Robert C, Kerby. Method and Apparatus for Controlling the Quaility ofElectrolytes:USA, 4324621A[P].1982-07-18.
|
 2008, Vol. 22
2008, Vol. 22
