| 酸性水溶液氯化提金新方法与工艺的研究 |
2. 赣州市环境监测站, 江西 赣州 341000
2. The Enrironmental Minotor Station of Gannan, Ganzhou 341000, Jiangxi, China
20世纪80年代以来, 黄金提取面临两大挑战, 一是可直接氰化的金矿资源日趋减少, 留下和新发现的金矿多为贫杂的难浸金矿石, 应用传统的氰化法已无法有效提金; 二是世界各国对生态平衡和环境提出了更高更严的要求。这两大挑战使人们寻找新的提金方法和工艺, 而酸性水溶液氯化的提出是最有应用前景的方法之一。该工艺具有药剂成本低、浸出速度快、浸出率高、环境污染少等优点, 尤其适合难浸金矿石的处理。
1 方法原理根据氯化理论, 水份对金氯化具有重要作用, 湿氯与干氯完全不同, 可在不加热情况下与金反应[1]。按氯化剂类型, 氯化温度和氯的水分不同, 氯化过程力学和机理是不同的。在氯化冶金中, 按介质种类和作业方式不同, 氯化浸出可分为盐酸浸出、氯盐浸出、氯气浸出和电氯化浸出共4种[2]。金的氯气浸出, 一般是在酸性介质中进行。在酸性条件下, Au与Cl2和Cl-之间的主要反应为:
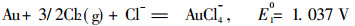
|
(1) |
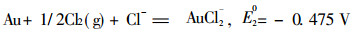
|
(2) |
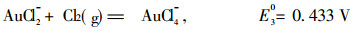
|
(3) |
金溶解进入溶液总浓度[Au]T为:
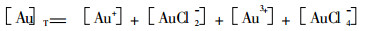
|
在实际提金中, 由于Cl2过量, 又是强氧化剂, 故Au溶解于酸性溶液中的主要形式为AuCl4-, 其离解常数β4= 10-26, 其氧化还原电位Ef为:
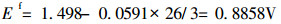
|
即Au由原来标准电位1.498V降为0.8858V, 此时Au易被Cl2所氧化, Cl2标准电位为E0 = 1.3595V。
从热力学分析, 见文献[3], [Au]T与Cl2的压力(PCl2), 溶液电位(Eh)和游离Cl-浓度([Cl-])密切相关, 三者关系式为:
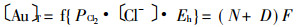
|
(4) |
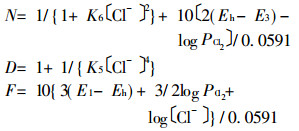
|
式中:
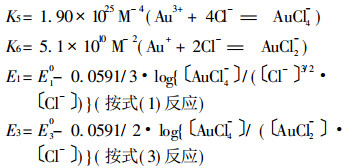
|
从热力学研究和按(4)式计算可表明以下几点。
(1) PCl2改变对金的溶解有显著影响, 即log [Au]T与PCl2呈线性关系, 当溶液中Eh= 1.0V、[Cl-] = 10mol/L且PCl2 = 5.07×104Pa时, 则[Au]T = 0.09mol/L; 若PCl2 = 15.20×10-4Pa时, [Au]T = 0.49 mol/L, [Au]T猛增近5倍。
(2) 游离[Cl-]浓度对[Au]T影响也很大, 随着[Cl-]增加, [Au]T明显增大, 由log[Au]T ~ log[Cl-]关系图可得斜率为0.92, 即当[Cl-]增加一个数量级, 则[Au]T增加9倍。
(3) [Au]T对溶液中Eh变化也非常敏感, 以PCl2 = 10.13×104Pa和[Cl-]= 1mol/L为例, 当Eh= 0.95V时, [Au]T = 8×10-5mol/L; 当Eh= 1.0V时, [Au]T = 2.6×10-2mol/L; 而当Eh = 1.05V时, [Au]T= 9 mol/L。
上述的理论研究和计算结果, 为酸性水溶液氯化提金工艺条件的选择提供了必要的理论依据。
2 实验部分 2.1 矿样性质在试验中, 选取江西兴国留龙金矿作试样, 该金矿含金、砷、铅等多硫化物石英脉型金矿, 属难浸矿石, 金呈不均匀嵌布, 部分金银被黄铁矿、毒砂所包裹, 含砷高, 氧化程度也高。取原矿500kg经粉碎至0.083~0.074mm, 试样号SG-100, 多元素分析结果见表 1。
| 表 1 兴国留龙金矿多元素分析结果 % |
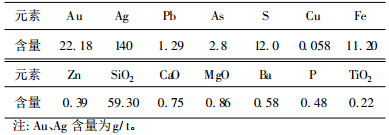 |
| 点击放大 |
2.2 浸出操作 2.2.1 条件试验
取金试样100g于500ml玻璃反应器中, 反应器附加电动搅拌器和密封装置, 利用新鲜液氯钢瓶控制流量, 通Cl2搅拌氯化。试验固定条件为:常温25℃, 搅拌速度180r/min, NaCl浓度为5%。改变下列条件:①HCl(mol/L) : 2.0、1.0、0.5。②固液比为1:2、1:3、1:4。③氯化时间(h) : 6、10、14。以三因素三水平L9(33)安排正交试验, 试样指标选择金浸出率(%), 经试验优选获取最适宜试验条件: HCl浓度0.5 mol/L, 固液比为1:3, 浸出时间为10h。
2.2.2 最适宜条件下酸性水溶液氯化浸出取SG-100金试样100g, 在最适宜浸出条件下(HCl 0.5mol/L, 固液比1:3, 浸出时间10h, NaCl用量5%)重复酸性水溶液氯化浸出, 浸出结果测定浸出液中Au浓度(mg/L), 并选用原子吸收光谱仪测定, 最终可计算浸出率(%), 结果列表 2。
| 表 2 SG-100金试样酸性水溶液氯化浸出结果 |
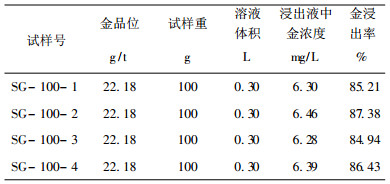 |
| 点击放大 |
从表 2可知, 浸出率为84.94%~87.38%、平均达到85.99%, (兴国留龙金矿采用氰化法浸出率为75%左右), 同时浸出时间也缩短至10h(一般氰化浸出时间为24h)。
2.3 锌丝置换回收金 2.3.1 条件试验在酸性水溶液氯化提金中, 用锌丝置换金还未见报导, 为此试验首要条件是控制酸度, 因为酸性过大, 锌丝与酸作用较快, 消耗锌丝较多, 同时还影响对金的置换; 若酸性较弱, 则[AuCl4]-又不能稳定存在, 由此采取L9(33)安排正交试验, 改变条件如下: pH分别为1.0、2.0、3.0;锌丝用量(mg/L)分别为60、70、80;置换时间(min)分别为50、60、70。获得锌丝置换回收金的最适宜条件: pH为2.0、锌丝用量60mg/L、置换时间为60min。
2.3.2 最适宜条件下锌丝置换回收金在上述最适宜置换条件下, 对SG-100金试样的浸出液进行锌丝置换, 置换结果通过对尾液中Au浓度(mg/L)的测定而获得, 并可计算置换率, 见表 3。
| 表 3 在金试样SG-100浸出液的置换结果 |
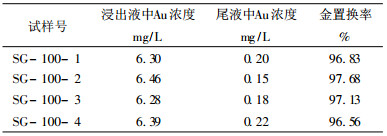 |
| 点击放大 |
从表 3可知, 金置换率为96.56%~97.68%, 平均可达到97.05%, 与一般氰化法相当。一般情况下, 金浸出率高, 置换率也高, 整个工艺回收率也高。但置换率常常受到浸出液中杂质离子的影响, 特别是Cu2+、Hg2+等有害成分。因此, 应控制pH=2左右较为合适。当pH < 1时, 溶液中H+会消耗锌丝, pH>3时, 会使浸出液中Fe3+形成Fe(OH)3沉淀, 影响锌丝置换; 同时[AuCl4]-也不能稳定存在。
3 结语(1) 酸性水溶液氯化法是采用HCl-Cl2体系浸取含Cu、As、C、Pb、Zn等难浸金矿, 是一种有效的湿法冶金工艺, 具有反应时间短、浸出率高、不污染环境等优点。试验取得了金浸出率为85.99%, 置换率为97.05%的较好效果, 为工业生产取代氰化法处理难浸金矿找到了一条新的途径。
(2) 因金在氯化浸出中要求更高的氧化浸出电位[4], 不与其他有价金属同时浸出, 在一般情况下, 即在浸出初期(前5h内), 金几乎不浸出, 而其他有色金属浸出率则已超过80%, 而硫化物在酸性中氧化难易顺序为: FeS> PbS> ZnS> CuFeS2> FeS2> Cu2S> CuS> Ag2S。因此, 该研究将第一段(即初期)浸出液弃去; 进入第二段浸出, 由于杂质离子干扰较少, 故可获得更高的浸出率和置换率。
(3) 对酸性介质下氯化浸出与锌丝置换金工艺, 还有赖于工业试验的进一步开展。
| [1] |
3 Гощ.  [J]. ¼ ĶÀ кк Бщ к щаокГ 3щща, 1989, (10):27-34.
[J]. ¼ ĶÀ кк Бщ к щаокГ 3щща, 1989, (10):27-34.
|
| [2] |
中南矿冶学院冶金研究室.
氯化冶金[M]. 北京: 冶金工业出版社: 222.
|
| [3] |
李希明, 柯家竣. 液氯化法提金的热力学分析[J].
金银专刊, 1991(1): 40–43.
|
| [4] |
谢斌, 胡绪名. 高砷铅阳极泥控制电位浸出金银[J].
贵金属, 1995, 16(1): 6–11.
|
 2000, Vol. 14
2000, Vol. 14
