| 从废旧稀土铁合金材料中回收稀土的研究 |
稀土铁合金材料品种较多, 如镝铁合金, 钕铁硼永磁材料, 重稀土硅铁合金、无硅稀土铁合金、镧基铁合金等, 随着稀土应用领域的拓展, 稀土铁合金材料的用量也日益增大。众所周知, 稀土铁合金材料在生产和加工过程中不可避免地会产生一些次品和加工废料, 因受现有生产和加工技术的制约, 有的稀土铁合金材料产出的次品和废料(统称废旧物)数量还十分可观, 几乎占生产总量的30%。这些废旧稀土铁合金材料所含有的稀土元素有些还是目前市场上十分紧俏和价值较高的, 如镝、钕、钇等。到目前为止, 国内还未见从这类废旧物中回收稀土的研究报导。若能有效地从这类废旧物中回收稀土, 实现资源的再生利用, 将具有十分良好的经济效益和社会效益。
稀土铁合金材料的主要成分是稀土和铁, 其他元素含量较少, 且大多是酸难溶物, 如硅、硼、钴等, 因此除铁是回收稀土的关键。本研究根据稀土铁合金材料上述特点, 首先将其用酸溶解, 使稀土金属转化为稀土离子, 然后将溶解液用双氧水氧化, 稀氨水中和, 使铁以针铁矿沉淀除去, 除铁液再用草酸沉淀稀土的回收工艺, 取得了非常好的效果。回收生产的产品稀土总量大于99%, Fe2O3小于0.02%, 稀土总收率大于91%。由于针铁矿在除铁的同时还可以将硅、铝、砷、氯等杂质元素除去, 因而产品中这些杂质元素含量也较低(均小于0.04%), 产品质量非常好, 本工艺特别适用回收那些质量要求高、价值大的稀土元素。
1 试验原理针铁矿是一种含水氧化铁矿物质, 其化学式为α-FeO(OH)。Fe3+只有在特定条件下才可能生成针铁矿沉淀物。针铁矿属晶型结构, 易于沉淀和过滤。废稀土铁合金材料加酸溶解后, 铁绝大部分转化为二价铁离子, 这样就为实现生成针铁矿沉淀提供了极有利的条件。二价铁离子被双氧水氧化生成针铁矿的化学反应式为:
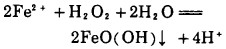
|
(1) |
针铁矿在水溶液中的稳定性可用下式表示:
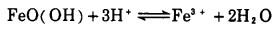
|
(2) |
图 1是95℃时针铁矿的溶解度曲线。从图中可见, 当pH小于3时, 铁离子平衡浓度增加非常迅速; PH大于3后, 变化缓慢; pH=3时, Fe3+浓度最低。由此可见, 为保证铁离子能生成针铁矿沉淀, 除应严格控制氧化反应过程, 保证Fe2+充分氧化外, 及时中和氧化过程产生的H+, 控制体系的pH值在合适范围也是十分关键的。
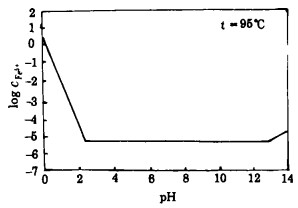 |
| 图 1 针铁矿溶解度曲线 |
2 试验部分 2.1 原料及主要试剂
试验用料主要成分为:REO 28.86%, Fe 51.16%, SiO2 3.52%, 水分13.82%。主要试剂为:工业纯盐酸, 工业纯双氧水, 工业纯氨水, 工业纯草酸。
2.2 工艺流程试验的工艺流程见图 2所示:
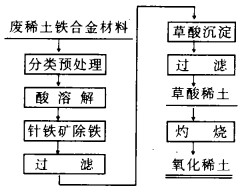 |
| 图 2 工艺流程示意图 |
2.3 主要仪器和设备
试验使用的主要仪器和设备为:
pHS-3型酸度计, 2XZ-1型旋片式真空泵, 1~5L平底烧杯, 2.5L分液漏斗。
2.4 分析方法稀土浓度用EDTA络合滴定法分析; 非稀土杂质元素用原子吸收光谱或比色分析法; 稀土总量用重量法分析。
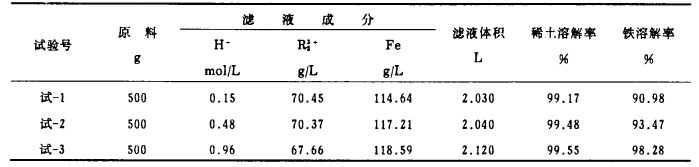
3 结果与讨论 3.1 废稀土铁合金材料酸溶解取上述原料3份各500g, 加酸溶解, 反应完全后过滤, 量取滤液体积(以10mL为单位, 不足部分用纯水补充, 下同), 测定滤液的酸度、稀土和铁的浓度。试验结果见表 1。可见在保证最终酸度大于0.1mol/L时, 稀土溶解基本完全, 铁的溶解率也在90%以上, 且随着最终酸度的提高而增大。
| 表 1 酸溶结果 |
 |
| 点击放大 |
3.2 针铁矿除铁试验 3.2.1 H2O2加入量的影响
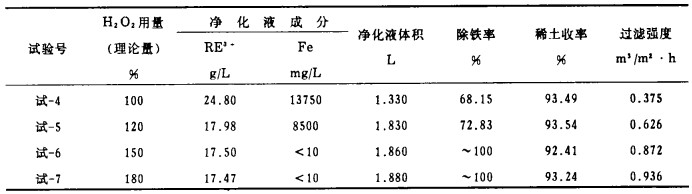
取试-1溶解液4份, 每份500mL, 分别按理论量的100%、120%, 150%、180%加入H2O2氧化, 用稀氨水控制氧化过程pH=3~4.5, 反应完全后抽滤, 测定滤液中稀土和铁的浓度, 抽滤时调节真空度为5×104Pa左右, 并记录时间。试验结果如表 2所示。
| 表 2 H2O2用量的试验结果 |
 |
| 点击放大 |
从试验结果可以看出, H2O2用量对铁的净化率影响较大, 对过滤性能也有一定影响, 对稀土收率的影响则较小, 随H2O2用量的增大, 除铁效果和过滤性能都有提高。试验表明, 欲要除铁彻底, H2O2用量必须保证在理论量的150%以上。
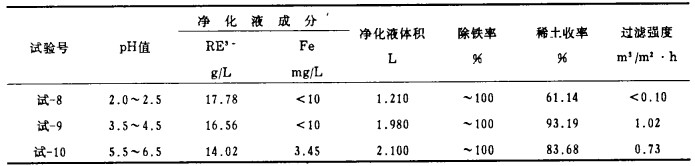
3.2.2 酸度的影响取试-2溶解液3份每份为0.5L, 均按理论计算量的160%加H2O2, 控制3份净化反应的酸度分别为pH=2~2.5, PH=3.5~4.5, PH=5.5~6.5, 反应完成后均在5×104Pa左右的真空下抽滤, 量取滤液体积, 测定滤液中稀土和铁的浓度, 试验结果见表 3。
| 表 3 酸度对净化效果的影响 |
 |
| 点击放大 |
从表 3可见, 在H2O2用量为理论量的160%的情况下, 只要保证体系的pH>2即可达到良好的除铁效果, 但体系的酸度不同, 对稀土的收率和净化渣的过滤性能有较大的影响。在pH≤2.5时, 过滤性能极差, 造成净化液抽滤不完全, 使稀土收率也大大下降, 原因是在该酸度下, 铁不完全以针铁矿沉淀, 有很大部分是以Fe(OH)3形式沉淀, 而Fe(OH)3是一种胶体, 其沉降和过滤性能极差。当体系pH≥5.5时, 稀土收率和过滤性能也有所下降, 因为在该pH值下部分稀土离子会水解生成氢氧化稀土而进入针铁矿中, 因而降低了稀土收率, 也影响了针铁矿的过滤性能。
3.2.3 温度的影响试验表明, 温度升高有利于提高净化效果, 尤其对过滤性能有较大的改善。但温度过高(大于90℃), 则会造成H2O2的损失, 甚至影响到除铁效果, 合理的净化温度应50~80℃。由于稀土铁合金材料中含铁较高, 氧化产生的H+较多, 中和反应产生的热也较多, 故可以借助反应本身放出的热来保证体系所需温度, 试验证明中和反应产生的热量一般可保证体系的温度在40℃以上, 因而无需另外的加热设施, 这在工业化生产时将可节省大量的投资和成本。
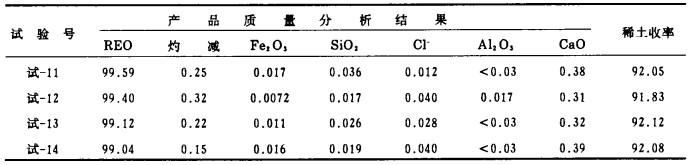
3.3 验证试验表 4为验证试验结果, 试验控制条件为:酸溶反应控制最终酸度0.1~0.5mol/L, H2O2用量为理论计算量的160%, 净化过程体系pH=3.5~4.5, 净化液按稀土:草酸=1:1.8加草酸沉淀稀土, 草酸稀土的灼烧温度为800~1000℃。表中的稀土收率为从原料到产品的稀土总收率。
| 表 4 验证试验的产品质量和收率 % |
 |
| 点击放大 |
4 结语
本工艺能够有效地从废稀土铁合金材料中回收稀土元素。回收产品稀土总量大于99%, Fe2O3小于0.02%, SiO2、A12O3、Cl-均小于0.04%。稀土总收率大于91%。开创了一条稀土元素再生利用的新途径, 具有良好的推广价值。
废稀土铁合金材料酸溶时只要保证最终酸度大于0.1mol/L即可使稀土金属的溶解率大于99%。
双氧水用量, 体系pH值、温度等因素对针铁矿法除铁效果和稀土收率有影响。最佳工艺条件是:双氧水用量为理论量的150%~180%, PH=3.5~4.5, 温度50~80℃。
| [1] |
陈家镛, 于淑秋, 伍志春, 等.
湿法冶金中铁的分离与利用[M]. 北京: 冶金工业出版社, 1981: 132-163.
|
| [2] |
钟竹前, 梅光贵.
湿法冶金过程[M]. 长沙: 中南工业大学出版社, 1988: 14-29.
|
 1998, Vol. 12
1998, Vol. 12
