2. 江苏农牧科技职业学院, 泰州 225300;
3. 江苏省动物重要疫病与人畜共患病防控协同创新中心, 扬州 225009
2. Jiangsu Agri-animal Husbandry Vocational College, Taizhou 225300, China;
3. Jiangsu Co-innovation Center for Prevention and Control of Important Animal Infections Diseases and Zoonoses, Yangzhou 225009, China
烯丙孕素是一种应用广泛的甾类孕激素,有明显的孕激素和抗促性腺激素作用,可抑制排卵。在国外兽医临床实践中,烯丙孕素主要用于母猪[1]、母马[2]的同期发情;而在国内兽医临床实践中,烯丙孕素主要用于促进母猪同期发情,还可用于促进乏情母猪的发情、延迟后备母猪的发情、延迟母猪的分娩时间[3]。但有关动物试验表明,烯丙孕素可导致死胎率增加、产仔数下降、卵巢畸形[4]。若人类长期食用含有此激素的食品,不仅会干扰人体正常的激素平衡,还会有明显的致癌效应,可导致女性及其后代生殖器官畸形和癌变,对于儿童则更明显。欧美等国家已对该药的使用和最高残留限量(MRL)作了严格规定(皮下脂肪为4 μg·kg-1,肝为2 μg·kg-1),国内尚未见有关规定。食品安全问题越来越受我国人民的重视,鉴于人们经常食用猪肉、猪肾、猪肝,本研究开展了烯丙孕素在猪肌肉、肾、肝、脂肪中的残留检测。
目前,国内外关于烯丙孕素的残留检测方法主要是液相色谱串联质谱法,文献报道了在河豚鱼、鳗鱼[5]、猪肉[6]中烯丙孕素的检测,但是这些研究都是通过结合固相萃取小柱来完成的,前处理复杂,用时较长,不适合快速检测,且运行成本较高。本研究对宁波第二激素厂自主研制的烯丙孕素口服液开展烯丙孕素在猪肌肉、肾、肝、脂肪中的残留检测,采用乙腈提取,饱和正己烷脱脂,10%碳酸钠溶液净化,高效液相色谱串联质谱法测定了猪可食性组织(肉、脂肪、肝、肾)中的烯丙孕素残留,探索其在猪体内的残留规律,以期能填补国内对该激素的残留消除规律的研究空缺,并为新兽药在我国临床上的合理应用和休药期制订提供理论依据。
1 材料与方法 1.1 主要仪器ACQUITY TM超高效液相色谱仪:美国Waters公司产品;Q-trap 5500三重四级杆串联质谱仪:美国AB公司产品;Eppendorf 5810R Centrifuge高速冷冻离心机:德国Eppendorf公司产品;BS124S分析天平:德国赛多利斯天平公司产品;Pacific RO纯水仪:北京五洲东方科技发展有限公司产品;SI可调速漩涡混合器VORTEX-GENIE2:上海思伯明仪器设备有限公司产品;氮吹仪:美国Organomation公司。
1.2 标准品、主要试剂与配制烯丙孕素(altrenogest)标准品(纯度为99.2%):宁波第二激素厂产品。乙腈、甲酸铵:色谱纯,美国Tedia公司产品;碳酸钠、乙酸钠、正已烷、乙酸乙酯:分析纯,国药集团化学试剂有限公司;β-葡萄糖醛酸酶/芳基硫酸酯酶:德国默克公司;乙酸:HPLC级,美国Tedia公司产品。
烯丙孕素口服液:含量规格为1 mL:4 mg,包装规格为450 mL·瓶-1,批号:160415;宁波第二激素厂产品。
烯丙孕素标准工作液的配制:准确称取10 mg烯丙孕素标准品于10 mL棕色容量瓶中,用乙腈溶解并定容至刻度,即配成烯丙孕素标准储备液(1 000 μg·mL-1)。准确吸取1 mL储备液,用流动相(5 mmol·L-1甲酸铵溶液:乙腈=6:4)定容到1 L,即得1 μg·mL-1烯丙孕素标准工作液。
5 mmol·L-1甲酸铵溶液的配制:准确称取0.315 g甲酸铵至1 000 mL容量瓶中,用超纯水溶解并定容,即配成5 mmol·L-1甲酸铵溶液。0.45 μm无机滤膜负压过滤, 超声波振荡20 min。现用现配。
0.2 mol·L-1乙酸钠缓冲溶液:称取16.4 g乙酸钠溶解于800 mL水中,用乙酸调节pH至5.2,用水定容至1 L。
乙腈饱和正已烷:取500 mL正已烷,加入适量乙腈,充分振摇后,待两相分层,上层即为乙腈饱和正已烷溶液。
1.3 试验动物选取22头达到性成熟的商品后备母猪(平均体重为50 kg),随机分为两组,分别为烯丙孕素推荐剂量组(简称试验组,20头)、空白对照组(简称对照组,2头)。试验猪均圈养,给药前分别称重、编号。试验前试验猪在新环境经过至少1周的适应期。给药前禁食过夜12 h,2 h后恢复正常饮食。饲料为不含任何药物的全价饲料。
1.4 给药剂量、途径及样品采集试验组猪按0.4 mg·kg-1内服给药(相当于每头猪20 mg烯丙孕素),每天定时给药一次,连用18 d。给药时烯丙孕素口服液按推荐剂量洒在受试动物的饲料表层,让动物经口自由摄入。于停药后6 h、1 d、5 d、10 d和18 d共5个时间点分别屠宰各试验组猪4头,分别取肌肉(背最长肌)、全肝、全肾、脂肪(皮下脂肪)。样本采集后立即做好标记、包装,于-20 ℃冰箱中保存待测。
1.5 色谱-质谱条件 1.5.1 色谱条件色谱柱:Thermo C18(3×100 mm,1.7 μm);流动相:A为5 mmol·L-1甲酸铵溶液,B为乙腈,梯度洗脱条件见表 1;流速:0.4 mL·min-1;柱温:30 ℃;进样量:10 μL。
|
|
表 1 梯度洗脱条件 Table 1 Gradient elution conditions |
离子源:电喷雾离子源;扫描方式:正离子扫描;检测方式:多反应监测(MRM);电喷雾电压:5.5 kV;去簇电压:126.8 U·V-1;离子化温度:550 ℃;气帘气:20.0 Psi;碰撞气:8 Psi。定性离子对、定量离子对、保留时间、锥孔电压和碰撞能量参考值见表 2。
|
|
表 2 烯丙孕素质谱检测参数 Table 2 Altrenogest and testosterone mass spectrometry |
① 称取试样2 g(精确至0.01 g),置于50 mL离心管中,加入5 mL乙酸钠溶液,再加入20 μL β-葡萄糖醛酸酶/芳基硫酸酯酶,然后盖盖涡旋混合1 min,在37 ℃±1 ℃振荡酶解12 h,取出冷却至室温,加入2 g氯化钠,振摇30 s后加入8 mL乙腈,涡旋提取1 min,5 000 r·min-1离心5 min,取乙腈层。②试样中再加入8 mL乙腈,重复上述提取过程。合并2次提取液,加入8 mL乙腈饱和正已烷,涡旋提取1 min,5 000 r·min-1下离心2 min,弃去正已烷后取乙腈层40 ℃下氮吹至近干。
1.6.2 肌肉、脂肪样品称取试样2 g(精确至0.01 g),置于50 mL离心管中,加入8 mL乙腈,振荡提取30 min,5 000 r·min-1离心5 min,取乙腈层。此后同“1.6.1 ”步骤②操作。
1.6.3 净化将以上所得残渣用10 mL乙酸乙酯复溶,涡旋30 s,然后加入10%碳酸钠溶液2 mL,涡旋混合30 s后5 000 r·min-1离心5 min,取上清液40 ℃水浴中氮气吹至近干后用样品定容溶液(5 mmol·L-1甲酸铵水溶液:乙腈=6:4)1.0 mL溶解,旋涡混匀后过0.22 μm滤膜。滤液供液相色谱串联质谱测定。
1.7 基质匹配标准曲线的制备精密量取适量烯丙孕素标准溶液,先用流动相配制质量浓度为1、5、10、50、100、200 ng·mL-1系列标准溶液,然后加1 mL标准溶液到经提取净化吹干后的不同空白基质残渣中,旋涡混匀后过0.22 μm滤膜,供液相色谱串联质谱测定,以定量离子对峰面积为纵坐标,标准溶液浓度为横坐标,绘制基质校准标准曲线。
1.8 检测限、定量限的测定取空白的猪肝、皮下脂肪、肌肉、肾样品,按照“1.6”所述方法处理,均设20个平行样品,测得基线噪音值,取信噪比S/N≥3确定为检测限,S/N≥10确定为定量限,并计算LOQ质量浓度点的回收率及相对标准偏差(RSD),验证其可靠性。
1.9 回收率、精密度的测定准确称取空白试验样品(猪肝、皮下脂肪、肌肉、肾)2.00 g±0.05 g,准确加入适量标准工作液,使样品中药物的添加浓度为1、100和200 μg·kg-1。同时进行空白样品处理。每个浓度分别设6个平行。添加样品经“1.6”所述方法提取净化后进行LC-MS/MS测定;空白样品经同样步骤处理后按照“1.6.3 ”方法制备与2、200和400 μg·L-1基质匹配标准溶液,然后进行LC-MS/MS测定,根据添加样品中烯丙孕素定量离子对峰面积和相应基质标准溶液(1、100和200 μg·kg-1添加浓度分别选择2、200和400 μg·L-1基质匹配标准溶液进行单点定量)中定量离子对峰面积的比值计算回收率。每种样品在一周内完成3个批次重复测定。据此求出各批内与批间变异系数。
1.10 稳定性试验对浓度水平为1、100、200 μg·L-1的5个平行稳定性样品执行分析,从而评估烯丙孕素标准工作液中烯丙孕素的稳定性。采用流动相稀释的方法分别制备上述3个浓度的标准工作液后立刻对样品执行分析,以得到第0天数据;在室温(约22 ℃)下放置2、6、8 h后执行样品分析。将标准工作液中检出的烯丙孕素浓度与理论加标浓度做比较(烯丙孕素标准工作液现配现用)。
将5 ng·mL-1烯丙孕素溶液(甲醇溶解)放置在太阳光下,室温25 ℃,分别于45 min、2 h、4 h、6 h后测定烯丙孕素浓度,检验其光照稳定性。
1.11 猪组织中烯丙孕素残留量的测定检测“1.4”采集的背最长肌肉、皮下脂肪、肝、肾组织样品中烯丙孕素的浓度。
2 结果 2.1 基质匹配标准曲线以烯丙孕素定量离子对的色谱峰面积(A)对烯丙孕素的质量浓度(C,μg·kg-1)作图,得到其基质标准曲线。烯丙孕素在1~200 ng·mL-1的浓度范围内,该药物的定量离子峰面积与浓度呈良好线性关系,线性回归方程:y=5.34e4X+6.87e4,相关系数0.999。
2.2 检测限和定量限向空白组织中添加一系列低浓度的烯丙孕素溶液,以信燥比(S/N)为3计算检测限(LOD),以信燥比为10计算定量限(LOQ)。结果显示:该药物的检测限为0.5 μg·kg-1,定量限为1.0 μg·kg-1。
2.3 回收率和精密度烯丙孕素在猪肌肉、皮下脂肪、肝、肾中回收率和相对标准偏差测定结果见表 3。
|
|
表 3 烯丙孕素加标回收率与相对标准偏差(n=6) Table 3 The recoveries and RSD of altrenogest(n=6) |
由表 3可知,本方法的平均添加回收率在68.9%~78.9%,日内相对标准偏差和日间相对标准偏差分别为3.92%~10.49%和4.92%~9.95%,相对标准偏差均小于11%。由此可见,在低浓度样品加标下,LC-MS/MS法测定猪组织中烯丙孕素残留具有良好的回收率和精密度,该方法适用于复杂基质中痕量化合物的定量和定性分析。
2.4 烯丙孕素标准工作液稳定性对于烯丙孕素标准工作液中的烯丙孕素而言,于室温条件(约22 ℃)下储存时可保持稳定达6 h。
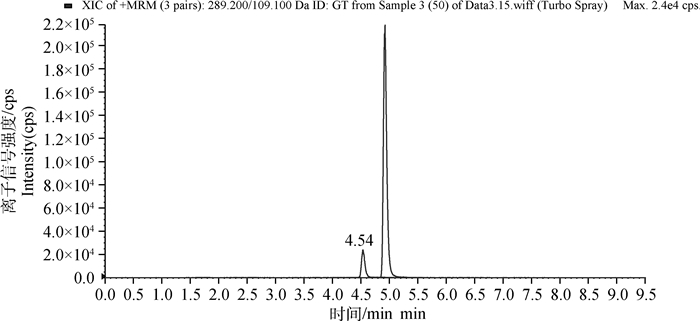
2.5 光照稳定性结果显示,6 h时烯丙孕素降解了35%。烯丙孕素和它的初级光解产物在Thermo C18反相色谱柱上的出峰时间分别为4.54、4.99 min,见图 1、图 2。在不严格避光的条件下,烯丙孕素在猪组织中部分会光解为其同分异构体,色谱图中会有两个药物峰出现,计算含量时要对两个峰同时定量,面积和即为烯丙孕素的真实含量。

|
图 1 对照溶液中烯丙孕素特征离子质量色谱图(5 μg·kg-1) Figure 1 Standard sample of altrenogest(5 μg·kg-1) |
|
图 2 光照2 h后对照溶液中烯丙孕素特征离子质量色谱图(5 μg·kg-1) Figure 2 Standard sample of altrenogest after the sun shined for two hours(5 μg·kg-1) |
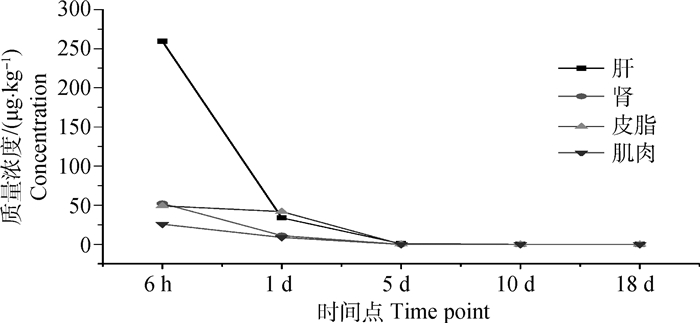
以0.4 mg·kg-1 (按体重给药)剂量内服给药18 d后,对背最长肌肉、皮下脂肪、肝、肾样品中烯丙孕素浓度进行测定,对照组均未检出烯丙孕素残留,给药组背最长肌肉、皮下脂肪、肝、肾中烯丙孕素浓度随时间变化见图 3,各个组织中残留量测定结果见表 4。
|
图 3 猪组织中烯丙孕素残留消除曲线 Figure 3 Residues eliminate curve of altrenogest in swine tissues |
|
|
表 4 给药后猪可食性组织中烯丙孕素残留量 Table 4 Residues of altrenogest in swine tissues |
烯丙孕素溶液按推荐给药方案给药,停药后6 h各组织均达到最高药物浓度,其中肝残留最高,平均残留量为259.25 μg·kg-1,其次依次是肾、皮下脂肪、肌肉,平均残留量分别为52.33、49.22、25.85 μg·kg-1;停药至第1天后,肝、肾、皮下脂肪和肌肉中烯丙孕素的平均残留量分别降至33.93、11.27、41.95和9.56 μg·kg-1。至停药第5天时,4头猪中仅1头猪的肝中烯丙孕素的残留量高于MRLs(2 μg·kg-1),达到2.81 μg·kg-1;另3头猪中,来自1头猪的肝中烯丙孕素的残留量高于定量限(1.0 μg·kg-1),其他组织中烯丙孕素的残留量均低于定量限;至停药第10天时,猪所有组织中烯丙孕素的残留量都低于检测限。
2.7 烯丙孕素在猪体内的休药期依据EMA发布的烯丙孕素在猪的肝组织中的残留限量,将停药后烯丙孕素在猪的肝组织中实测的残留量数据采用WT1.4休药期软件拟合,如按双单侧95%置信区间计算休药期为7.59 d,如按双单侧99%置信区间计算则休药期为8.67 d,如图 4、5所示。因此宁波第二激素厂提供的烯丙孕素溶液按推荐给药方案使用,建议休药期定为9 d。

|
图 4 按双单侧95%置信区间拟合的休药期拟合曲线 Figure 4 Plot of withdrawal time calculation for swine liver at the time when the one-sided 95% upper tolerance limit was below the EU MRL |

|
图 5 按双单侧99%置信区间拟合的休药期拟合曲线 Figure 5 Plot of withdrawal time calculation for swine liver at the time when the one-sided 99% upper tolerance limit was below the EU MRL |
烯丙孕素结构中有1, 2环戊烷并多氢菲基本母核,甾核由A、B、C和D环稠合而成,A、B、C为六元环,D为五元环,D环C-17有烯丙基侧链,环中有双键,这使得它在紫外-可见光照射下吸收一定波长的光,从而发生直接光解。Wammer等[7]报道,在太阳辐射能为250 w·m-2,室温30 ℃,pH=6的条件下,10 μmol·L-1烯丙孕素溶液(10%甲醇水溶解)迅速降解为1.6 nmol·L-1,光解半衰期为27 s(kobs=2.58±0.04×10-2);光解速率随着烯丙孕素浓度的升高而升高,随氧气浓度的升高而降低,不随pH和温度的变化而变化。此外,光解速率还与烯丙孕素溶液的组成有关,有机物浓度越高光解速率越慢,在上述相同条件下,40和80 mg·L-1腐殖酸中烯丙孕素光解半衰期分别为6和10 min。为避免失去药理学活性,烯丙孕素溶液应避光保存。
烯丙孕素的初级光解产物是烯丙孕素通过环内加成反应得到的,它是烯丙孕素的同分异构体[8]。烯丙孕素和它的初级光解产物性质差异很大,据国外文献报道,在C18反相色谱柱上,烯丙孕素和它的同分异构体出峰时间分别为4.3、7 min。本试验中发现,烯丙孕素和它的初级光解产物在Thermo C18反相色谱柱上的出峰时间分别为4.54、4.99 min,这与国外报道的结果一致。在不严格避光的条件下,烯丙孕素在猪组织中部分会光解为其同分异构体,色谱图中会有两个药物峰出现,计算含量时要对两个峰同时定量,面积和即为烯丙孕素的真实含量。
3.2 酶解条件的优化有研究者用β-葡糖苷酸/芳基硫酸酯酶对动物肌肉、内脏等样品进行酶解,使药物与组织解离,以提高药物萃取效率[9]。但有学者认为孕激素类药物主要以游离态的形式存在,不需要酶解。EMEA[10]报道了给药后30 d内样品(猪和马肝、肾)中烯丙孕素/总残留物。在猪和马的肝样品中,总残留物的80%不可逆地结合在组织大分子上因而失去药理学活性;其余残留物在肝中游离并且具有药理学活性,烯丙孕素/总残留物最大(为25%);在第15天,烯丙孕素/总残留物最小(0.5%)。在猪和马的肾样品中,总残留物的20%与组织大分子结合,总残留物的80%游离出来并且具有药理学活性。在肌肉和皮下脂肪样品中因总残留量太低无法计算出烯丙孕素/总残留物,因此将肌肉和皮下脂肪组织中所有的残留物都认为是烯丙孕素。报道中显示,烯丙孕素在肝、肾中代谢物主要是烯丙孕素的谷胱甘肽和葡萄糖苷酸结合物,故本试验用β-葡萄糖醛酸/芳基硫酸酯酶酶解的方法处理肝、肾样品,直接提取处理肌肉、脂肪样品。
3.3 动物试验方案本研究中的给药周期、给药剂量、给药途径是根据欧洲原研厂家提供的给药方案(英特威烯丙孕素产品概要[11])和二期临床试验结果制定的。给药周期与母猪发情周期有关,我国母猪发情周期一般为18 d,为了实现同一批母猪同步发情,给药周期必须与母猪发情周期保持一致;给药剂量0.4 mg·kg-1为临床推荐剂量,也与欧洲原研厂家提供的剂量相一致;EMEA与FDA批准的给药途径为口服,经口灌服操作繁琐,容易引起动物的应激反应,不利于饲养员的操作,因此本研究采用将药洒在饲料表面的方式给药。实际给药时一头动物与其他动物的饲料槽是分开的,并且每次给药后饲料基本上被吃光,这样确保了烯丙孕素全部被利用。
3.4 提取条件的优化烯丙孕素属于脂溶性化合物,烯丙孕素为弱极性化合物,难溶于水,易溶于乙醇、乙腈、丙酮、叔丁基甲醚等有机溶剂。常用于提取烯丙孕素的溶剂有叔丁基甲醚、甲醇[12]、乙腈[13]和乙酸乙酯。本试验比较了不同提取剂对回收率的影响,结果表明:用叔丁基甲醚提取时,烯丙孕素回收率高,为70%左右,但共提的脂肪较多,且药物易与脂肪结合,影响提取效果;用乙酸乙酯提取时,烯丙孕素回收率63%,对烯丙孕素提取效果较差;甲醇乙腈提取效率较好,回收率都在80%左右,但是乙腈的除蛋白能力强于甲醇,而且用乙腈提取,共提杂质较少,因此本研究选用乙腈作为前处理的提取试剂。考察了提取剂的体积(分别采用8、10、15 mL乙腈进行提取)和提取次数对提取效率的影响,试验结果表明,提取剂量为8 mL提取两次和提取剂量为15 mL提取两次,两者回收率相同,为了减少溶剂用量最终确定用8 mL乙腈提取两次。
3.5 净化条件的优化由于猪组织中含有大量的脂肪,因此有必要进行脱脂。试验考察了8 mL乙腈饱和正己烷除脂与-20 ℃冷冻除脂这两种方法的脱脂效果。结果表明:乙腈饱和正己烷能有效除去猪肌肉、皮下脂肪、肝、肾提取液中脂类和非极性杂质的干扰,但会造成烯丙孕素在前处理过程中的损失,导致回收率偏低;冷冻除脂药物回收率较高,但除脂量较少。乙腈饱和正己烷除脂之后,回收率达70%,可选用乙腈饱和正己烷作为除脂溶剂。
为了达到理想的净化效果,脱脂后的溶液须进一步净化。试验比较了HLB、C18这2种甾类孕激素常用的柱子对提取液的净化效果。研究发现,Oasis HLB是最符合本试验的SPE柱。将Oasis HLB柱依次用3 mL甲醇、3 mL水活化平衡,将提取液氮吹复溶后过柱,用3 mL 20%乙腈水、3 mL水淋洗,真空抽10 s后,用3 mL乙腈洗脱,收集洗脱液于10 mL离心管中。由于固相萃取耗时,过程繁琐,且费用较高。据报道,萃取前用pH 9~10碳酸盐溶液碱化样品液可除去碱性杂质,且净化效果较好[14]。试验又继续考察了10%、15%、20%碳酸钠溶液的净化效果,结果显示,10%碳酸钠溶液净化效果较好,回收率较高。通过比较固相萃取和碳酸钠溶液净化的目标药物的峰面积发现差异不显著,本研究采用10%碳酸钠溶液净化。
3.6 基质效应利用ESI离子源对目标物进行分析时会产生较强的基质效应,试验中采用提取后添加法评估基质效应。计算阴性基质匹配标准溶液与流动相标准溶液响应值的比值,当比值接近1时说明不存在基质效应的影响;当比值大于或小于1时,说明基质对待测组分的响应有增强或抑制效应。本试验测定了质量浓度为1、2、5 ng·mL-1的基质匹配标准工作液和流动相标准溶液。结果显示,肝、肾中两个响应值之比为0.50~0.54,肌肉、皮下脂肪中两个响应值之比为0.65~0.69,说明肝、肾中的基质抑制效应强于肌肉、皮下脂肪。为消除基质效应的干扰,本试验采用空白基质匹配标液定量校正。
3.7 烯丙孕素在猪组织中的残留消除规律及休药期的确定对肌肉、皮下脂肪、肝、肾中的烯丙孕素残留量进行分析比较,结果显示,在同一采样时间点,猪组织中烯丙孕素的残留量规律为肝>肾>皮下脂肪>肌肉,这与EMEA[15]报道的国外同类产品在猪可食性组织中的残留量检测结果一致。药物在肝中代谢,而且药物在猪体内主要经胆汁、粪便、尿液排泄,在肾中不会造成蓄积,因此,在同一采样时间点,烯丙孕素残留量,肝>肾;脂肪中烯丙孕素残留量远远高于肌肉中的残留量,这是脂肪为亲脂性化合物的缘故。由猪组织中烯丙孕素残留消除曲线可以看出,除肝外其他组织在5 d后药物浓度低于MRL,肝在10 d后药物浓度低于MRL,表明烯丙孕素在猪体内代谢较快,且在各组织无蓄积。肝中的药物残留量最高,消除时间最长,故肝是烯丙孕素在猪可食性组织中的残留靶组织。
根据烯丙孕素在猪组织中的残留检测值,采用WT1.4软件按99%置信区间计算烯丙孕素在猪肝中的休药期,结果显示,休药期为9 d,这一结果与欧洲原研厂家生产的烯丙孕素在猪体内休药期相同[11],而美国等国家报道同类产品在猪体内休药期为21 d[16],这可能与不同产品的生产工艺、猪的种类不同有关。参照欧盟和美国规定的烯丙孕素在猪组织中的最高残留限量标准,当母猪按0.4 mg·kg-1(按体重给药)内服给药18 d后其休药期为9 d。
4 结论采用乙腈提取,乙腈饱和正己烷溶液除脂,10%碳酸钠溶液净化,建立高效液相色谱串联质谱法测定猪可食性组织(肉、脂肪、肝、肾)中的烯丙孕素残留情况,该方法的检测限为0.5 μg·kg-1,定量限为1.0 μg·kg-1,相对标准偏差均小于11%。猪按0.4 mg·kg-1剂量经口给药,每天1次,连续给药18 d。各组织烯丙孕素残留量在休药6 h后最高,休药后第5天脂肪中的残留量低于最大残留限量,肌肉、肾中残留量低于定量限,休药第10天所有组织中烯丙孕素残留量均低于定量限。组织残留量由高到低依次为肝>肾>脂肪>肌肉,肝中烯丙孕素消除缓慢且消除时间最长。建议此种给药方式休药期为9 d。
| [1] | VAN LEEUWEN J J J, MARTENS M R T M, JOURQUIN J, et al. Variation in LH pulsatility during 24 h after a postweaning altrenogest treatment in relation to follicle development in primiparous sows[J]. Anim Reprod Sci, 2011, 126(1-2): 101–107. DOI: 10.1016/j.anireprosci.2011.04.015 |
| [2] | HODGSON D, HOWE S, JEFFCOTT L, et al. Effect of prolonged use of altrenogest on behaviour in mares[J]. Vet J, 2005, 169(1): 113–115. DOI: 10.1016/j.tvjl.2004.04.020 |
| [3] |
VANDERHAEGHE C.烯丙孕素对母猪早产和繁殖性能的影响[J].志强, 译.中国畜牧业, 2012(12): 66.
VANDERHAEGHE C. Effects of altrenogest on premature delivery and reproductive performance of sows[J]. Zhiqiang, translate. China Animal Industry, 2012(12): 66. (in Chinese) http://kns.cnki.net/KCMS/detail/detail.aspx?filename=MYTX201212029&dbname=CJFD&dbcode=CJFQ |
| [4] | WILLMANN C, SCHULER G, HOFFMANN B. Effects of age and altrenogest treatment on conceptus development and secretion of LH, progesterone and eCG in early-pregnant mares[J]. Theriogenology, 2011, 75(3): 421–428. DOI: 10.1016/j.theriogenology.2010.05.009 |
| [5] |
康海宁, 谢丽琪, 肖来龙, 等. 超高效液相色谱-串联质谱法对河豚鱼、鳗鱼及烤鳗中烯丙孕素与氯地孕酮残留的同时测定[J]. 分析测试学报, 2009, 28(10): 1180–1184.
KANG H N, XIE L Q, XIAO L L, et al. Determination of altrenogest and chlormadinone residues in swellfish, eel, roasted eel by ultra performance liquid chromatography-tandem mass spectrometry[J]. Journal of Instrumental Analysis, 2009, 28(10): 1180–1184. DOI: 10.3969/j.issn.1004-4957.2009.10.015 (in Chinese) |
| [6] | ZHANG D, PARK J A, KIM S K, et al. Determination of residual levels of naloxone, yohimbine, thiophanate, and altrenogest in porcine muscle using QuEChERS with liquid chromatography and triple quadrupole mass spectrometry[J]. J Sep Sci, 2016, 39(5): 835–841. DOI: 10.1002/jssc.201501206 |
| [7] | WAMMER K H, ANDERSON K C, ERICKSON P R, et al. Environmental photochemistry of altrenogest:Photoisomerization to a bioactive product with increased environmental persistence via reversible photohydration[J]. Environ Sci Technol, 2016, 50(14): 7480–7488. DOI: 10.1021/acs.est.6b02608 |
| [8] | KENYON P. Analytical methods for the detection and quantification of trenbolone acetate metabolites, altrenogest and related photoproducts via liquid chromatography tandem mass spectrometry[D]. Washington: University of Washington, 2015. |
| [9] |
中华人民共和国国家质量监督检验检疫总局. SN/T 1980-2007进出口动物源性食品中孕激素类药物残留量的检测方法高效液相色谱-质谱/质谱法[S].北京: 中国标准出版社, 2007.
General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. SN/T 1980-2007 Determination of progestogens residues in food of animal origin for import and export-HPLC-MS/MS method[S]. Beijing: Standards Press of China, 2007. (in Chinese) |
| [10] | EMEA. Committee for veterinary medicinal products: Altrenogest summary report(2)[R]. EMEA/MRL/831/01-FINAL, London: EMEA, 2002. |
| [11] | MORGAN S, MACKAY A. Summary of product characteristics[M]//STOLERMAN I P. Encyclopedia of Psychopharmacology. Berlin, Heidelberg: Springer, 2010. |
| [12] | LAMPINEN-SALOMONSSON M, BECKMAN E, BONDESSON U. Detection of altrenogest and its metabolites in post administration horse urine using liquid chromatography tandem mass spectrometry-increased sensitivity by chemical derivatisation of the glucuronic acid conjugate[J]. J Chromatogr B, 2006, 833(2): 245–256. DOI: 10.1016/j.jchromb.2006.02.014 |
| [13] | JANSEN E H J M, ZOONTJES P W, BOTH-MIEDEMA R, et al. Screening of parts-per-billion levels of diethylstilbestrol in bovine urine by high-performance liquid chromatography with ultraviolet detection[J]. J Chromatogr A, 1985, 347: 379–383. DOI: 10.1016/S0021-9673(01)95509-8 |
| [14] | ZIECIK A J, KLOS J, PRZYGRODZKA E, et al. Aberrant effects of altrenogest and exposure to exogenous gonadotropins on follicular cysts appearance in gilts[J]. Theriogenology, 2017, 89: 250–254. DOI: 10.1016/j.theriogenology.2016.10.028 |
| [15] | EMEA. Committee for veterinary medicinal products: Altrenogest summary report[R]. EMEA/MRL/487/477, London: EMEA, 2012. |
| [16] | Freedom of information summary original abbreviated new animal drug application[R]. ANADA, 2017: 200-621. |



