2. 江苏农牧科技职业学院, 泰州 225300
2. Jiangsu Agri-animal Husbandry Vocational College, Taizhou 225300, China
黄体期短期营养水平处理能够显著影响绵羊情期[1],并推测卵泡内葡萄糖是影响卵母细胞质量和卵泡发育能力的主要因素之一[2]。体外培养液中添加生糖物质能够显著提高卵母细胞发育能力[3]。葡萄糖是颗粒细胞增殖分化最佳的能量底物,添加葡萄糖能够增强颗粒细胞增殖和雌激素合成能力[4]。卵母细胞首先通过卵丘细胞的葡萄糖转运蛋白(GLUT)系统吸收葡萄糖,再转运至卵母细胞[5]。葡萄糖作为卵泡发育的重要能量来源,其在卵泡细胞内的代谢途径主要包括多元醇途径(Polyol pathway)、糖酵解途径(Glycolysis pathway)、己糖胺生物合成途径(Hexosamine biosynthesis pathway)和磷酸戊糖途径(Pentose phosphate pathway),上述途径共同参与调节能量供应,细胞稳态,细胞核成熟等过程[6]。其中,糖酵解途径是细胞糖代谢的主要能量供给途径[7],与卵母细胞发育能力正相关[8],以丙酮酸和乳酸[9]或其他代谢中间产物的形式为卵泡发育直接[7]或间接[10]供能;糖酵解与卵母细胞发育能力正相关[8]。己糖胺代谢是主要的能量感应通路,其关键限速酶透明质酸合成酶2(HAS2)的表达与卵母细胞发育能力密切相关[11],透明质酸酶是胞外基质(ECM)基本骨架,而葡萄糖和葡萄糖胺是透明质酸酶合成的主要底物[6],并进一步影响LH释放波峰和表皮生长因子/FSH的分泌[12],参与卵巢周期性排卵过程,并已被证明参与介导了卵泡内环境对营养水平的应答过程[13]。磷酸戊糖途径为卵母细胞减数分裂各阶段中核成熟和氧化还原反应提供了必要的底物来源[14],并被认为其通过核质成熟调控参与卵泡发育过程[8]。多元醇途径的增强被认为通过促进山梨醇和果糖的胞内累积等引发糖尿病[15]。葡萄糖途径对卵丘卵母细胞生长和卵泡发育均具有重要的作用。此外,黄体溶解前补饲4~6 d促进绵羊卵泡发育,限饲抑制卵泡发育。黄体期卵泡更易闭锁,而颗粒细胞凋亡对卵泡闭锁具有重要的作用。补饲期升高的葡萄糖直接作用于卵巢,增加黄体溶解时逃脱闭锁的卵泡数,进而促进卵泡发育。然而,黄体期营养处理组试验羊发情周期、卵巢组织不同直径卵泡分布、卵巢组织细胞凋亡率;卵泡细胞GLUT蛋白及葡萄糖代谢途径中部分关键基因表达量的变化关系至今未有报道。本研究以葡萄糖代谢途径中部分基因为研究对象,探索其在不同营养条件下在卵泡细胞中的表达情况,并分析其与卵泡发育和卵巢组织凋亡的关系,有助于进一步探寻葡萄糖代谢在黄体期营养水平对绵羊卵泡发育的调控作用,丰富黄体期卵泡发育的“急性效应”分子机制,为科学饲养空怀母羊,提高绵羊繁殖力提供参考。
1 材料与方法 1.1 试验设计本试验与2015年10月-12月在江苏省泰州市海伦羊业有限公司开展,选择体况良好,体重((43.69±1.27) kg)和月龄((29±4.5)月)相近的经产湖羊30只,预饲7 d后,使用孕酮海绵栓埋置法进行同期发情,12 d后下午撤栓并颈部皮下注射PGF2α(30 mg,宁波三生药业有限公司),次日清晨起使用经调教的成年公羊进行试情(06:00和18:00),发情结束当日定义为下一个情期的第0天,参照《肉羊饲养标准NY/T816-2004》中推荐的营养需要量标准,在随后6 d对所有试验羊按照1.0倍维持需要量水平(1.09 kg·d-1)饲喂全价颗粒饲料(TMR,表 1),在此情期的第7~14天,将所有试验羊随机分为1.0倍维持需要组(1.0M;1.09 kg·d-1);0.5倍维持需要量组(0.5M;0.55 kg·d-1),和1.5倍维持需要量组(1.5 M;1.65 kg·d-1);第15天分别从3组随机挑选屠宰6只试验羊,并取卵巢组织待用,剩下的12只湖羊按1.0倍维持需要量词喂, 并对原有各组试验羊进行发情鉴定观察,用以统计发情周期。试验动物的饲养管理完全参照由南京农业大学动物福利伦理委员会制定的《实验动物福利伦理指南(SYXK 2011-0036)》中的相关动物福利执行标准进行。
|
|
表 1 TMR日粮组成及营养成分 Table 1 Ingredient and chemical composition of the total mixed ration |
屠宰后摘取卵巢组织,用低温生理盐水冲洗3遍以上,置于装有冰预冷D-PBS的塑料培养皿中,随机选取一侧卵巢在体视镜下使用眼科剪镊钝性剥除其结缔组织,并根据方格纸栅格测量结果,分离直径>1.0 mm的卵泡,放入含D-PBS的塑料培养皿中,剥离下的可视卵泡根据其卵泡直径进一步分为 < 2.5 mm和≥2.5 mm卵泡两个大小等级,随后将剥离下的卵泡用眼科剪对半剖开,使用接种环沿卵泡内壁刮下卵泡细胞,连同卵泡液一同置于含红细胞裂解液的预冷PBS中, 孵育3~5 min,随后将每只试验羊同大小等级卵泡缓慢移入2 mL离心管中,4 ℃13 000 r·min-1离心10 min,-20 ℃保存待用。每头羊卵泡液在30 min内分离完成,且在生物冰上操作。另一侧卵巢组织经4%多聚甲醛固定后常规石蜡包埋, 4 μm切片待检。
1.3 卵巢组织细胞凋亡检测使用原位细胞凋亡检测试剂盒(货号:11684817910, 罗氏, 美国)进行检测卵巢组织细胞凋亡情况。通过TUNEL法检测细胞核染色的棕黄色为阳性细胞。经TUNEL染色及苏木精复染后凋亡细胞核呈棕色,正常细胞核染蓝色。结果根据凋亡阳性细胞分布情况,每张切片拍摄10个阳性视野,每视野记数30个卵泡细胞中阳性细胞数,以平均计算阳性细胞所占的百分比作为细胞凋亡率(Apoptosis rate,AR),相应的结果表示为“平均值±标准误(Mean±SE)”。
1.4 免疫组织化学检测将石蜡切片梯度脱蜡脱水,随后抗原修复液在微波炉内高火煮沸,然后将切片放入其中,中低火修复10 min后,自然冷却至室温,3%甲醇-H2O2孵育20 min,以消除内源性过氧化氢酶的活性, 蒸馏水冲洗, PBS浸洗5 min,滴加正常山羊血清封闭液,室温孵育15 min,分别滴加GLUT-4(博士德生物科技有限公司,武汉)蛋白多克隆抗体, 4 ℃孵育过夜(对照组用1% BSA代替),用0.1% PBST洗涤,滴加二抗37 ℃孵育2 h,随后使用0.05% DAB和0.01% H2O2混合显色3 min(根据具体着色情况可适当缩短或延长显色时间),随后对所有石蜡切片进行脱水透明处理并用中性树脂封片,干燥后观察。
1.5 Western blot检测用RIPA裂解法提取卵巢组织蛋白,并应用BCA蛋白分析试剂盒测定蛋白浓度;根据所测浓度用RIPA裂解液调节蛋白浓度,保证各样品的蛋白浓度一致,进行蛋白变性,变性后蛋白置于-20 ℃保存。将蛋白样品使用上样缓冲液进行稀释(> 1.5 μg·μL-1),依据试剂盒说明书的要求分别进行分离胶和浓缩胶的制备,胶孔加样20 μL的蛋白样本,在聚丙烯酰胺凝胶电泳仪(SDS-PAGE)中分别电泳30和120 min,剪取PVDF膜,在转膜缓冲液中完成整个转膜过程。将转膜后的PVDF膜放入预先加入2 mL 5%的BSA的自封袋中,封口,置于摇床上,室温孵育2 h。TBST洗膜3次,加入2 mL GLUT4一抗(1:750稀释;货号:21619;南京建成生物工程研究所),封口,置于摇床上,4 ℃过夜孵育,TBST洗膜5次,放入新的自封袋中,加入2 mL稀释好的二抗(1:1 000,HRP标记的羊抗兔IgG),置于摇床上,室温孵育2 h。TBST洗膜5次后加入适量ECL显影液,避光静置2 min后,用Image Quant LAS 4000仪器进行显影。
1.6 实时荧光定量分析按照罗氏试剂盒说明,提取卵泡细胞总RNA,取2.5 μL RNA样品,在微量分光光度计下测定样本的OD值及总RNA浓度。以制备的cDNA为模板,利用设计合成的特异性引物(表 2),通过RT-PCR扩增目的基因,检测卵巢组织中HAS2、AR、ECM1、G6PDH、GFPT1、GFPT2、HK1、OGT、PFK、SDH mRNA的表达,每个样品设3个重复,β-actin为内参基因,基因的相对表达水平采用2-ΔΔCT方法进行分析。使用SPSS 18.0软件进行单因素方差统计学分析,以P < 0.05为差异显著。反应体系:2 μL cDNA、10 μL SYBR green PCR master mix,6.8 μL双蒸水,上下游引物各0.6 μL,共计20 μL;反应程序:预变性95 ℃ 10 min;变性95 ℃ 10 s,退火60 ℃30 s,延伸72 ℃ 30 s,40个循环。
|
|
表 2 荧光定量PCR引物信息 Table 2 Information of quantitative PCR primer sequences |
数据使用SPSS16.0软件进行统计分析,结果以“平均值±标准误”表示,不同试验组试验羊的发情周期、卵巢组织凋亡率、卵泡细胞糖代谢相关基因表达水平和Western blot等数据采用One-way方差分析(Duncan’s法多重比较);不同大小卵泡数采用卡方分析(Fisher’s精确检验)。
2 结果 2.1 黄体期营养水平对发情周期及卵泡发育的影响黄体期不同营养水平对试验羊发情周期和不同直径卵泡数量的影响见表 3。0.5M组试验羊的平均发情周期为(19.25±0.48)d,显著高于1.0M组((17.75±0.63)d)和1.5M组((17.25±0.48)d;P < 0.05),该结果表明,黄体期0.5倍维持需要量饲喂水平显著抑制了湖羊的发情。此外,营养水平处理显著影响了卵巢组织大卵泡(卵泡直径:≥ 2.5 mm)和小卵泡(卵泡直径:1.0~2.5 mm)数量,其中0.5M组试验羊大卵泡和小卵泡数量分别显著低于和高于1.0M与1.5M组(P < 0.05);但3组试验羊总卵泡数差异不显著(卵泡直径:≥ 1.0 mm),此外,0.5M组试验羊小卵泡数/总卵泡数、大卵泡/总卵泡数分别高于和低于1.0M与1.5M组(P < 0.05)。
|
|
表 3 黄体期不同营养水平饲喂试验羊发情周期及卵巢组织不同大小卵泡数量情况 Table 3 Estrous cycle and distribution of the ovarian follicles from ewes under different nutritional treatments during the luteal phase |
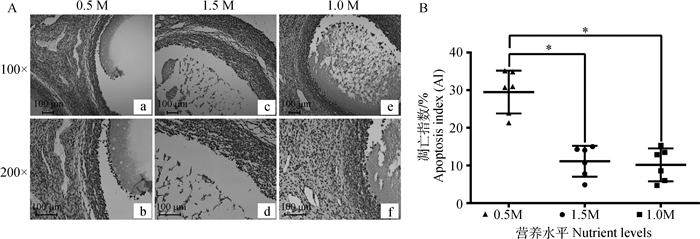
黄体期营养水平对卵巢组织细胞凋亡的影响如图 1所示;结果表明,0.5M组试验羊卵巢组织颗粒细胞凋亡指数(29.50%±2.37%)显著高于1.0M(11.11%±1.68%)与1.5M组(10.16%±1.82%;P < 0.05)。
|
A.不同营养水平处理试验羊卵巢TUNEL检测结果;B.卵巢细胞凋亡指数(▲.0.5M组;●.1.5M组;■.1.0M组);*.P < 0.05 A.TUNEL results of ovarian from ewes among different nutritional treatments; B.Apoptosis index (▲. 0.5M group; ●. 1.5M group; ■.1.0M group); *.P < 0.05 图 1 不同营养水平组湖羊卵巢细胞凋亡 Figure 1 Cell apoptosis of ovarian in different nutrient treatments |
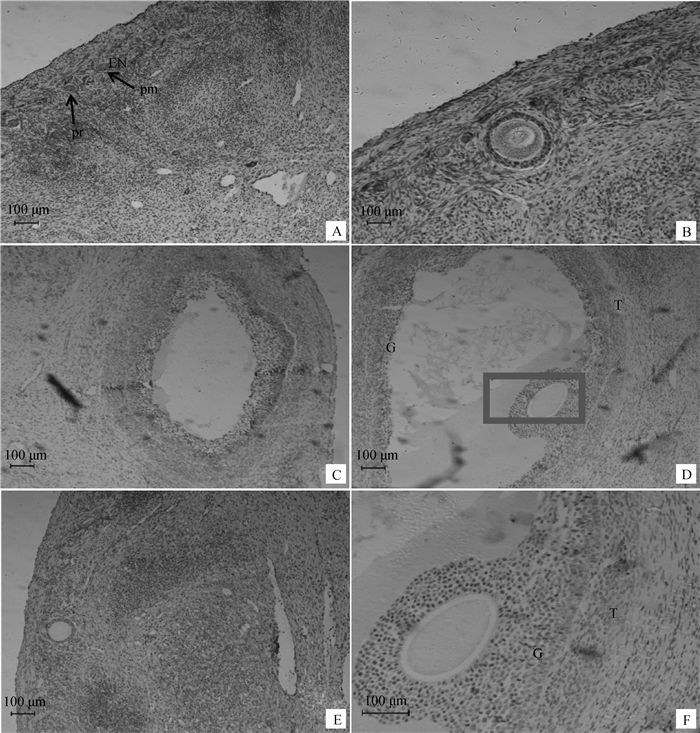
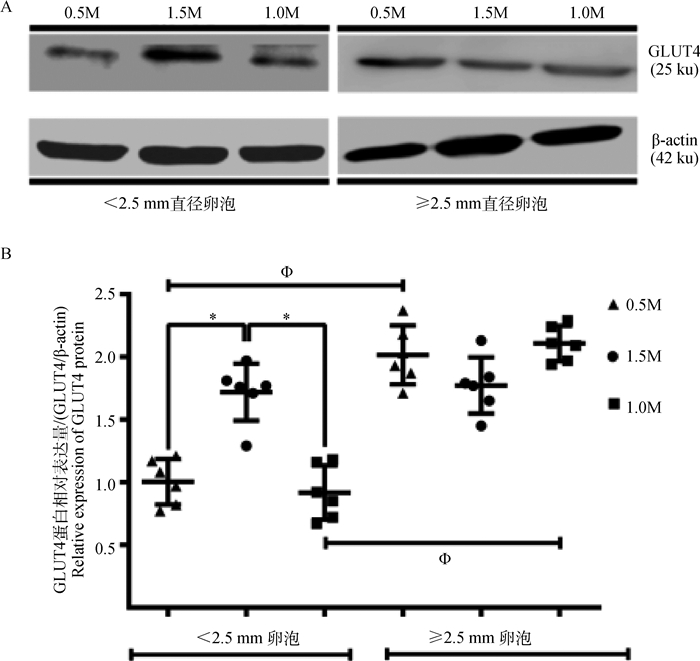
及其在卵泡细胞中的定量研究葡萄糖转运蛋白-4(GLUT4)在卵巢组织中的表达定位见图 2,如图 2所示,GLUT4蛋白主要在原始和初级卵泡(图 2A)、次级卵泡(图 2B)卵母细胞胞质中表达;在三级卵泡(图 2C)和排卵前卵泡(图 2D和E)颗粒细胞和膜细胞中均有表达。GLUT4在不同营养水平试验羊卵巢组织 < 2.5 mm及≥2.5 mm卵泡中的表达变化情况如图 3所示,对0.5M和1.0M组而言,GLUT4蛋白表达量随卵泡直径的增加而显著升高(P < 0.05),其在1.5M组不同直径卵泡间差异不显著(P > 0.05);且1.5M组 < 2.5 mm卵泡中GLUT4蛋白表达量显著高于1.0M和0.5M组(P < 0.05),但不同营养水平组在≥2.5 mm卵泡中GLUT4蛋白表达量差异不显著(P > 0.05)。
|
A.初级卵泡;B.次级卵泡;C.三级卵泡;D.排卵前卵泡; F.D中长方形框标注所在区域的高倍视野下的排卵前卵泡;E.空白对照。EN.卵母细胞巢;G.颗粒细胞;T.膜细胞 A.The primordial follicle (pr) and primary follicle (pm); B. The secondary follicle; C.The tertiary follicle; D.The preovulatory follicle; F. The preovulatory follicle in the higher multiples of vision based on the frame marked area within the D; E.Blank control. EN. Egg nests; G.Granulosa cells; T.Thecal cells 图 2 葡萄糖转运蛋白(GLUT4)在卵巢组织中的定位(A、B、C、D和E 100×;F 200×) Figure 2 Immunohistochemical localization glucose transporter 4 (GLUT4) in ovarian tissues (A, B, C, D and E 100×; F 200×) |
|
A.GLUT4在不同营养水平处理组试验羊不同直径卵泡细胞Western blot检测结果;B.GLUT4蛋白表达量;*.相同卵泡直径中不同营养水平处理组卵泡GLUT4表达差异显著(P < 0.05);Φ.相同营养水平处理组中不同直径卵泡GLUT4表达差异显著(P < 0.05) A.Western blot band of GLUT4 within different follicle size of ewes under different nutrition al treatments; B.GLUT4 protein expression levels; *.Significant differences of GLUT4 expression between different nutrient levels within the same follicle size (P < 0.05); Φ.Significant differences of GLUT4 expression between different follicle sizes within the same nutrient level (P < 0.05) 图 3 黄体期营养水平对卵泡细胞葡萄糖转运蛋白(GLUT4)表达量的影响 Figure 3 Effect of nutrient levels treatment during luteal phase on glucose transporter 4 (GLUT4) expression in follicular cells |
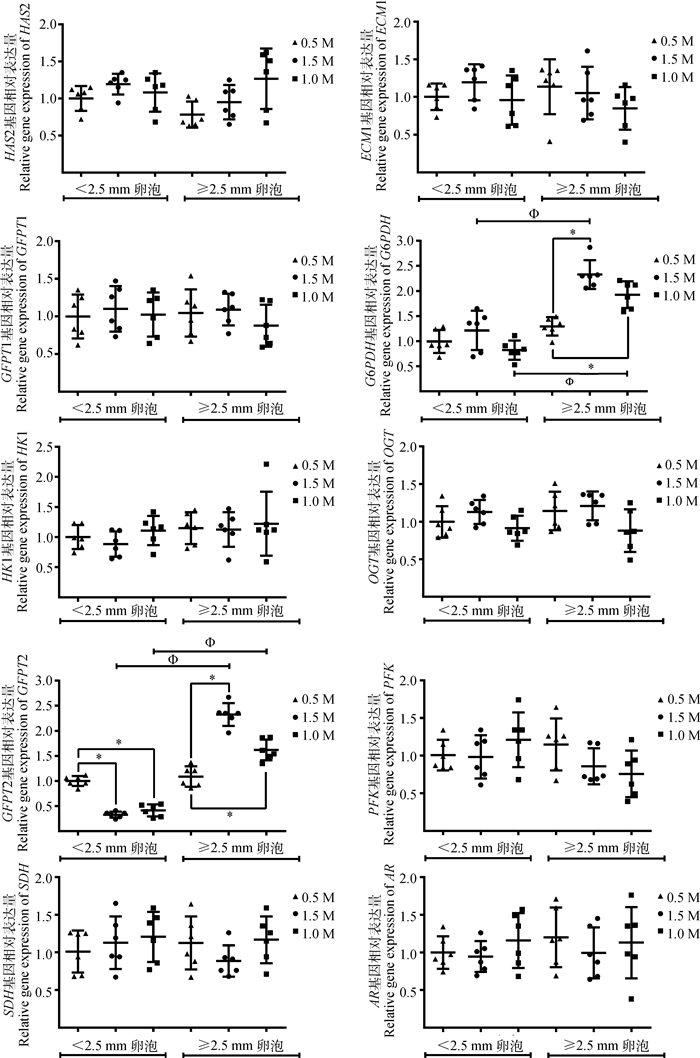
黄体期营养水平对不同直径卵泡细胞糖代谢途径关键基因表达量的影响如图 4所示:本研究中所检测的卵泡细胞HAS2、ECM1、AR、GFPT1、HK1、OGT、PFK、SDH的基因表达量在 < 2.5 mm和≥2.5 mm卵泡细胞中的表达量在不同营养水平处理组间差异均不显著(P > 0.05);己糖胺途径关键酶GFPT2基因表达量在不同直径卵泡中随营养水平变化趋势完全相反,表现为 < 2.5 mm卵泡中随采食量水平升高而降低(P < 0.05),而其在≥2.5 mm卵泡中则随采食量水平的升高而显著升高(P < 0.05);此外,0.5M组≥2.5 mm卵泡细胞的戊糖磷酸途径关键酶G6PDH基因显著低于1.0M组和1.5M组(P < 0.05),而不同营养水平组G6PDH基因表达量在 < 2.5 mm卵泡中差异不显著(P > 0.05)。
|
*.相同卵泡直径中不同营养水平处理组卵泡基因表达差异显著(P < 0.05);Φ.相同营养水平处理组中不同直径卵泡基因表达差异显著(P < 0.05) *.Significant differences of genes expression between different nutrient levels within the same follicle size (P < 0.05);Φ.Significant differences of genes expression between different follicle sizes within the same nutrient level (P < 0.05) 图 4 黄体期营养水平对卵泡细胞糖代谢途径关键基因表达的影响 Figure 4 Effect of nutrient levels treatment during luteal phase on key genes involved in glucose metabolic pathway of follicular cells |
随着细胞凋亡研究的深入,人们逐渐认识到次级卵泡的闭锁主要是颗粒细胞的凋亡所致[16]。由细胞凋亡诱导的颗粒细胞死亡已在小鼠[17], 奶牛[18], 绵羊[19]和猪[20]等物种证实。在哺乳动物黄体期卵泡发育过程中,仅有少数卵泡能够逃脱闭锁命运而发育至排卵。卵泡闭锁最初表现为颗粒细胞出现核固缩,到了闭锁后期,大量的颗粒细胞发生凋亡,颗粒细胞碎片充满整个卵泡液。本研究结果表明,0.5M组试验羊卵巢卵泡中细胞凋亡指数显著高于1.0M和1.5M组,由此推测黄体期营养限饲对湖羊卵泡发育的影响与卵泡细胞凋亡有关。
葡萄糖是卵泡发育的能量和代谢底物来源[21]。机体摄入的葡萄糖需通过葡萄糖转运家族蛋白(GLUTs)。其中,GLUT4被认为是具有胰岛素依赖性、具有较强葡萄糖转运能力的功能性蛋白[22]。本研究结果显示,0.5M组试验羊发情延迟,其在卵泡分级和不同直径卵泡分布上表现为 < 2.5 mm卵泡数量的增多和≥2.5 mm卵泡数量的减少,提示0.5倍维持营养水平限饲可能抑制了 < 2.5 mm卵泡向≥2.5 mm卵泡的发育;结合GLUT4蛋白在不同营养水平和不同直径卵泡细胞内的表达变化,笔者进一步猜测 < 2.5 mm卵泡发育的抑制很有可能与GLUT4在 < 2.5 mm卵泡细胞表达量的下调有关,同时已有研究表明黄体期低饲喂水平通过上调血液孕酮、雌二醇、孕酮与雌二醇比值和FSH水平抑制卵泡发育[23],由此,笔者推测黄体期营养限饲对卵泡发育的抑制很可能与卵泡细胞的雌激素分泌能力差异有关。然而,不同营养水平组试验羊≥2.5 mm卵泡细胞GLUT4蛋白表达量无显著差异,提示卵泡细胞葡萄糖转运系统随营养水平的表达变化模式存在卵泡发育阶段依赖性,笔者认为在营养负平衡饲喂条件下,机体优先满足优势或亚优势卵泡的葡萄糖需要,本研究所得卵泡细胞GLUT4蛋白随卵泡直径增加的上升的结果也为上述猜测提供了依据。
己糖胺合成通路(HBP)被认为能量状态的“传感器”[24],6-磷酸葡萄糖(Glucose-6-phosphate)经HBP途径代谢为6-磷酸果糖(Fructose-6-phosphate),并在谷氨酰胺-6-磷酸果糖转移酶(Glucosamine:fructose-6-phosphate transaminase;GFPT)的催化下进一步转化为6-磷酸葡萄糖胺(Glucosamine-6-phosphate),并最终生成细胞的重要糖基供体(UDP-N-乙酰葡糖胺)。HBP途径在正常体细胞糖代谢总量中的占比仅为1%~3%,UDP-N-乙酰葡糖胺除作为糖基供体参与能量供给外,还能够在透明质酸合酶(HAS)催化作用下生成的透明质酸(Hyaluronic acid)是卵丘细胞外基质(ECM)的主要骨架结构。已有研究发现,卵丘细胞中HAS表达量与卵母细胞发育能力的增强有直接关系[11];此外,UDP-N-乙酰葡糖胺还能在O-连接糖基化酶(OGT)催化下发生O-联糖基化,进而通过基因转录、信号转导和细胞生长与分化等多个重要的生物学过程参与卵泡发育[25]。本研究中,OGT和HAS2基因在不同直径卵泡和不同营养水平处理组表达量均无差异,表明黄体期营养水平处理并未影响卵泡细胞在O-联糖基化和透明质酸合成过程。但作为HBP途径的另一关键限速酶,GFPT2基因在≥2.5mm卵泡细胞中的表达量随营养水平的升高而显著升高,而 < 2.5mm卵泡中该基因随营养水平的变化趋势却与之完全相反。由此推测,GFPTs基因表达量的变化趋势反映了卵泡细胞的HBP途径对营养水平应答在不同直径卵泡间存在差异,且主要表现在6-磷酸葡萄糖胺和UDP-N-乙酰葡糖胺等反应中间产物催化效率的差异。GFPT抑制剂(6-重氮-5-氧代-L-正亮氨酸)能够显著降低卵丘细胞葡萄糖摄入量和增殖速率,该结果也佐证了本研究对HBP途径可能参与调控卵泡发育的急性营养调节机制的推测。绵羊黄体期注射葡萄糖胺能够显著增加大卵泡数[26],促进主动脉平滑肌IGFβ[27]以及骨骼肌TGFα基因表达[28],通过抑制芳香化酶的表达[29]和雌二醇的分泌[30]参与调节卵泡发育,上述过程可能与本研究1.5M营养水平处理对试验羊≥2.5mm卵泡发育的促进有关,进而表现为该组试验羊≥2.5mm卵泡数量的增加。
磷酸戊糖途径(Pentose phosphate pathway;PPP)是葡萄糖氧化分解的主要方式之一,由氧化和非氧化过程组成,所摄入的葡萄糖能够以氧化和非氧化反应的形式参与到PPP中。作为磷酸戊糖途径的第一限速酶,6-磷酸葡萄糖脱氢酶(G6PDH)在卵母细胞和卵丘细胞中表达量有所不同,在牛上,卵母细胞G6PDH表达量显著高于卵丘细胞[31]。本研究中,在1.0M和1.5M组中,G6PDH基因在≥2.5 mm卵泡细胞中的表达量显著高于 < 2.5 mm卵泡细胞,这可能维持需要以上饲喂水平试验羊卵巢组织中较大直径卵泡中未成熟卵母细胞的质量提高、卵母细胞核成熟比例增加有关[32],然而,0.5M组试验羊G6PDH基因表达量在不同直径卵泡细胞表达量却无显著差异,基于上述理论,笔者推测0.5M组不同直径卵泡细胞在卵母细胞质量,核成熟比例上亦无显著差异,也侧面验证前文中提及的营养限饲抑制了卵泡由 < 2.5 mm向≥2.5 mm进一步发育的推论。此外,作为PPP途径的主要产物,NADPH作为还原剂、氢负离子的供体能够将氧化型谷胱甘肽(GSSG)转化为还原型谷胱甘肽(GSH),从而发挥清除体内自由基维持氧化平衡的生物学功能[6],因此,PPP途径的增强对机体抗氧化应激能力具有正调控效应。本研究结果表明,0.5M限饲显著降低了G6PDH基因在≥2.5 mm卵泡中的表达量,但其在 < 2.5 mm卵泡中的表达量无显著差异,由此推测黄体期限饲特异性导致≥2.5 mm卵泡氧化应激的发生,与此类似,在利用3-硝基丙酸诱导氧化应激的在体小鼠模型中,与中等和小直径卵泡相比,氧化应激诱导组大直径卵泡闭锁率更高,更易受到氧化应激的影响[33]。因此,笔者进一步推测PPP通路极有可能更倾向于在大直径卵泡中发挥营养应答效应,且此效应很可能与氧化应激发生有关。
4 结论黄体期0.5M限饲导致湖羊发情延迟;此过程很可能与其卵巢细胞凋亡率的升高,< 2.5mm卵泡细胞GLUT4蛋白表达量的降低和HBP途径的增强,以及≥ 2.5 mm卵泡细胞中HBP途径的减弱和PPP途径的增强等有关。
| [1] |
应诗家, 王昌龙, 贾若欣, 等. 湖羊不同发育阶段卵泡内代谢产物和激素含量的比较研究[J]. 畜牧兽医学报, 2012, 43(2): 180–185.
YING S J, WANG C L, JIA R X, et al. A comparative study of metabolites and hormone concentrations in different sized follicles in Hu sheep[J]. Acta Veterinaria et Zootechnica Sinica, 2012, 43(2): 180–185. (in Chinese) |
| [2] | NANDI S, GIRISH K V, MANJUNATHA B M, et al. Follicular fluid concentrations of glucose, lactate and pyruvate in buffalo and sheep, and their effects on cultured oocytes, granulosa and cumulus cells[J]. Theriogenology, 2008, 69(2): 186–196. DOI: 10.1016/j.theriogenology.2007.08.036 |
| [3] | BERLINGUER F, GONZALEZ-BULNES A, CONTRERAS-SOLIS I, et al. Glucogenic supply increases oocyte developmental competence in sheep[J]. Reprod Fertil Dev, 2012, 24(8): 1055–1062. DOI: 10.1071/RD11299 |
| [4] | CAMPBELL B K, ONIONS V, KENDALL N R, et al. The effect of monosaccharide sugars and pyruvate on the differentiation and metabolism of sheep granulosa cells in vitro[J]. Reproduction, 2010, 140(4): 541–550. DOI: 10.1530/REP-10-0146 |
| [5] | WANG Q, CHI M M, SCHEDL T, et al. An intercellular pathway for glucose transport into mouse oocytes[J]. Am J Physiol Endocrinol Metab, 2012, 302(12): E1511–E1518. DOI: 10.1152/ajpendo.00016.2012 |
| [6] | SUTTON-MCDOWALL M L, GILCHRIST R B, THOMPSON J G. The pivotal role of glucose metabolism in determining oocyte developmental competence[J]. Reproduction, 2010, 139(4): 685–695. DOI: 10.1530/REP-09-0345 |
| [7] | HARRIS S E, LEESE H J, GOSDEN R G, et al. Pyruvate and oxygen consumption throughout the growth and development of murine oocytes[J]. Mol Reprod Dev, 2009, 76(3): 231–238. DOI: 10.1002/mrd.v76:3 |
| [8] | DOWNS S M, UTECHT A M. Metabolism of radiolabeled glucose by mouse oocytes and oocyte-cumulus cell complexes[J]. Biol Reprod, 1999, 60(6): 1446–1452. DOI: 10.1095/biolreprod60.6.1446 |
| [9] | HARRIS S E, ADRIAENS I, LEESE H J, et al. Carbohydrate metabolism by murine ovarian follicles and oocytes grown in vitro[J]. Reproduction, 2007, 134(3): 415–424. DOI: 10.1530/REP-07-0061 |
| [10] | HERRICK J R, BRAD A M, KRISHER R L. Chemical manipulation of glucose metabolism in porcine oocytes: Effects on nuclear and cytoplasmic maturation in vitro[J]. Reproduction, 2006, 131(2): 289–298. DOI: 10.1530/rep.1.00835 |
| [11] | ASSIDI M, DUFORT I, ALI A, et al. Identification of potential markers of oocyte competence expressed in bovine cumulus cells matured with follicle-stimulating hormone and/or phorbol myristate acetate in vitro[J]. Biol Reprod, 2008, 79(2): 209–222. DOI: 10.1095/biolreprod.108.067686 |
| [12] | BUCCIONE R, VANDERHYDEN B C, CARON P J, et al. FSH-induced expansion of the mouse cumulus oophorus in vitro is dependent upon a specific factor(s) secreted by the oocyte[J]. Dev Biol, 1990, 138(1): 16–25. DOI: 10.1016/0012-1606(90)90172-F |
| [13] | SCARAMUZZI R J, BROWN H M, DUPONT J. Nutritional and metabolic mechanisms in the ovary and their role in mediating the effects of diet on folliculogenesis: A perspective[J]. Reprod Domest Anim, 2010, 45(S3): 32–41. |
| [14] | SUTTON-MCDOWALL M L, GILCHRIST R B, THOMPSON J G. Effect of hexoses and gonadotrophin supplementation on bovine oocyte nuclear maturation during in vitro maturation in a synthetic follicle fluid medium[J]. Reprod Fertil Dev, 2005, 17(4): 407–415. DOI: 10.1071/RD04135 |
| [15] | CHUNG S S M, HO E C M, LAM K S L, et al. Contribution of polyol pathway to diabetes-induced oxidative stress[J]. J Am Soc Nephrol, 2003, 14(S3): S233–S236. |
| [16] |
梁学超, 蒋明, 罗玉茹, 等. 猪卵巢发育的组织学变化及卵泡闭锁规律研究[J]. 畜牧兽医学报, 2017, 48(10): 1863–1870.
LIANG X C, JIANG M, LUO Y R, et al. Study on histology and patterns of follicular atresia during ovarian development in pig[J]. Acta Veterinaria et Zootechnica Sinica, 2017, 48(10): 1863–1870. (in Chinese) |
| [17] | HUGHES F M Jr, GOROSPE W C. Biochemical identification of apoptosis (programmed cell death) in granulosa cells: Evidence for a potential mechanism underlying follicular atresia[J]. Endocrinology, 1991, 129(5): 2415–2422. DOI: 10.1210/endo-129-5-2415 |
| [18] | JOLLY P D, TISDALL D J, HEATH D A, et al. Apoptosis in bovine granulosa cells in relation to steroid synthesis, cyclic adenosine 3', 5'-monophosphate response to follicle-stimulating hormone and luteinizing hormone, and follicular atresia[J]. Biol Reprod, 1994, 51(5): 934–944. DOI: 10.1095/biolreprod51.5.934 |
| [19] | MURDOCH W J. Programmed cell death in preovulatory ovine follicles[J]. Biol Reprod, 1995, 53(1): 8–12. DOI: 10.1095/biolreprod53.1.8 |
| [20] | SUGIMOTO M, MANABE N, KIMURA Y, et al. Ultrastructural changes in granulosa cells in porcine antral follicles undergoing atresia indicate apoptotic cell death[J]. J Reprod Dev, 1998, 44(1): 7–14. DOI: 10.1262/jrd.44.7 |
| [21] | DOWNING J A, SCARAMUZZI R J. Nutrient effects on ovulation rate, ovarian function and the secretion of gonadotrophic and metabolic hormones in sheep[J]. J Reprod Fertil Suppl, 1991, 43: 209–227. |
| [22] | WILLIAMS S A, BLACHE D, MARTIN G B, et al. Effect of nutritional supplementation on quantities of glucose transporters 1 and 4 in sheep granulosa and theca cells[J]. Reproduction, 2001, 122(6): 947–956. DOI: 10.1530/rep.0.1220947 |
| [23] | YING S J, WANG Z Y, WANG C L, et al. Effect of different levels of short-term feed intake on folliculogenesis and follicular fluid and plasma concentrations of lactate dehydrogenase, glucose, and hormones in Hu sheep during the luteal phase[J]. Reproduction, 2011, 142(5): 699–710. DOI: 10.1530/REP-11-0229 |
| [24] | MARSHALL S, BACOTE V, TRAXINGER R R. Discovery of a metabolic pathway mediating glucose-induced desensitization of the glucose transport system[J]. J Biol Chem, 1991, 226(8): 4706–4712. |
| [25] | WELLS L, WHELAN S A, HART G W. O-GlcNAc: A regulatory post-translational modification[J]. Biochem Biophys Res Commun, 2003, 302(3): 435–441. DOI: 10.1016/S0006-291X(03)00175-X |
| [26] | MUÑOZ-GUTIÉRREZ M, BLACHE D, MARTIN G B, et al. Folliculogenesis and ovarian expression of mRNA encoding aromatase in anoestrous sheep after 5 days of glucose or glucosamine infusion or supplementary lupin feeding[J]. Reproduction, 2002, 124(5): 721–731. DOI: 10.1530/rep.0.1240721 |
| [27] | MCCLAIN D A, PATERSON A J, ROOS M D, et al. Glucose and glucosamine regulate growth factor gene expression in vascular smooth muscle cells[J]. Proc Natl Acad Sci U S A, 1992, 89(17): 8150–8154. DOI: 10.1073/pnas.89.17.8150 |
| [28] | DANIELS M C, KANSAL P, SMITH T M, et al. Glucose regulation of transforming growth factor-alpha expression is mediated by products of the hexosamine biosynthesis pathway[J]. Mol Endocrinol, 1993, 7(8): 1041–1048. |
| [29] | HARLOW C R, CAHILL D J, MAILE L A, et al. Time-dependent effects of transforming growth factor α on aromatase activity in human granulosa cells[J]. Hum Reprod, 1995, 10(10): 2554–2559. DOI: 10.1093/oxfordjournals.humrep.a135744 |
| [30] | SCARAMUZZI R J, DOWNING J A. The in vivo effects of fibroblast growth factor and epidermal growth factor on the secretion of oestradiol, androstenedione and progesterone by the autotransplanted ovary in the ewe[J]. J Endocrinol, 1995, 146(2): 301–311. DOI: 10.1677/joe.0.1460301 |
| [31] | CETICA P, PINTOS L, DALVIT G, et al. Activity of key enzymes involved in glucose and triglyceride catabolism during bovine oocyte maturation in vitro[J]. Reproduction, 2002, 124(5): 675–681. DOI: 10.1530/rep.0.1240675 |
| [32] |
郭延华, 周平, 石国庆, 等. 绵羊不同直径卵泡卵母细胞特征及染色体形态分析[J]. 新疆农业科学, 2012, 49(7): 1307–1314.
GUO Y H, ZHOU P, SHI G Q, et al. The characteristics of ovine oocytes from different diameter follicles and chromatin configuration analysis[J]. Xinjiang Agricultural Science, 2012, 49(7): 1307–1314. DOI: 10.6048/j.issn.1001-4330.2012.07.022 (in Chinese) |
| [33] | ZHANG J Q, SHEN M, ZHU C C, et al. 3-nitropropionic acid induces ovarian oxidative stress and impairs follicle in mouse[J]. PLoS One, 2014, 9(2): e86589. DOI: 10.1371/journal.pone.0086589 |



