哺乳动物的卵巢作为卵子发生、卵泡发育及性激素合成和分泌的场所,对于动物的繁殖特性、繁殖活动的维持起着至关重要的作用。卵泡的生长和黄体的形成是依赖血管形成的,血管形成对维持正常的卵巢生理起重要作用[1]。因此卵子发生和卵泡发育离不开卵巢的动脉血供网络。自20世纪80年代开始,国内外学者就对哺乳动物子宫和卵巢动脉的分布、走形及对卵泡、黄体的供血特性做了大量的研究。研究发现,猪卵巢动脉发出的2~4条一级分支的管径较粗且有轻度螺旋状结构[2],整个卵巢动脉血管网呈卵圆形或肾形, 与子宫动脉前分支有交通[3];大鼠的卵巢动脉既有直行段又有轻度波浪形特征,猴子的卵巢动脉也呈现出螺旋状走形[2]。除此之外,许多学者对大鼠、家兔及猪等动物的卵泡和黄体发育过程中的血液供应、血管网络构筑等作了深入的研究[4-6]。
在人类医学中,产后出血主要通过子宫动脉栓塞术进行治疗,但由于对女性及其他哺乳动物输卵管—卵巢动脉血管网的精细解剖学研究不够深入,导致该手术存在一定的失败率[7]。因此深入研究哺乳动物子宫动脉与卵巢动脉之间的交通吻合方式的解剖学研究是解决以上问题的关键[8]。绵羊作为一种小型反刍家畜,是一种理想的试验动物模型。对其卵巢动脉供血特征的深入研究,可为人类医学研究特别是产科手术治疗奠定研究基础并积累资料。目前,国内外学者对于绵羊卵巢动脉、微动脉的形态学及与卵泡发育功能的相关性研究尚没有相关报道。本研究利用血管铸型标本制作技术,制作绵羊卵巢动脉的立体构筑模型,观察并分析了绵羊卵巢动脉及其分支的基本走形、分布特点及卵泡、黄体微动脉的大体解剖特征,以探讨绵羊卵巢的供血特性与卵泡、黄体发育的相关性。
1 材料与方法 1.1 试验材料从20只屠宰后的成年藏绵羊分离获得卵巢和新鲜子宫及附件。屠宰羊只来源于青海省西宁市乐家湾牛羊定点屠宰场。
1.2 试验药品及器械丙烯腈-丁二烯-苯乙烯共聚物(ABS)、丙酮、丁酮、油画颜料、浓盐酸、解剖工具、自制灌注工具、Canon50D数码相机。
1.3 血管铸型剂配制提前20 d,将ABS溶解于50:50(v/v)的丙酮:丁酮溶液中,并与蓝色或红色油画颜料加热混合,制成8%浓度的单色铸型剂。
1.4 样本处理及灌注对采集到的卵巢样本,快速带至实验室,清洗表层血液、粪便等污物,将绵羊子宫外周其他组织剥离,小心除去生殖器官系膜上的脂肪、板油等残留物,或单独分离卵巢及其周边血管进行单侧灌注,或保留绵羊子宫进行双侧灌注操作,卵巢动脉灌注方法参考文献[8],并进行改良。
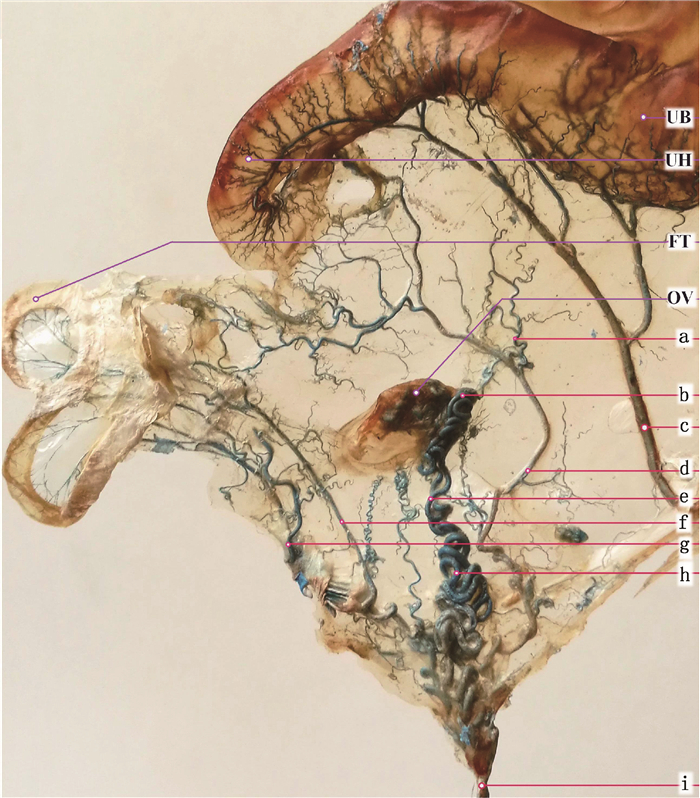
2 结果 2.1 绵羊卵巢动脉及其分支通过ABS灌注的绵羊子宫风干标本(图 1)可见,从腹主动脉发出的卵巢动脉[9]或子宫-卵巢动脉[10]起始段相对平直,之后卵巢动脉主干开始螺旋型环绕,一直延伸到卵巢门并进入,在该螺旋状动脉前1/3行程上,向两侧发出分支,管径变小,一侧伸向子宫方向为卵巢动脉子宫支,沿途发出2~3条二级分支,包括子宫系膜分支及向子宫角前部和输卵管后部的供血支(图 1a,d);另一侧伸向输卵管系膜和卵巢系膜方向的为卵巢动脉输卵管支,其间发出4~6条小分支向卵巢系膜供血,并在前端发出数条小分支指向输卵管系膜供血(图 1f, g)。
|
UB.子宫体;UH.子宫角;FT.输卵管;OV.卵巢. a.卵巢动脉子宫系膜支;b.卵巢动脉卵巢门重螺旋;c.子宫动脉;d.卵巢动脉子宫支;e.卵巢动脉轻螺旋;f.卵巢动脉输卵管支;g.卵巢动脉输卵管系膜支;h.卵巢动脉卵巢支;i.卵巢动脉 UB. Uterine body; UH. Uterine horn; FT. Fallopian tube; OV.Ovary.a.Mesometrium branch of ovarian artery; b.Ovarian hilum intensive spiral of ovarian artery; c. Uterine artery; d. Uterine branch of ovarian artery; e. Slight spiral of ovarian artery; f. Fallopian tube branch of ovarian artery; g.Mesosalpinx branch of ovarian artery; h. Ovarian branch of ovarian artery; i.Ovarian artery 图 1 绵羊卵巢动脉及其分支供血分布(1.5×) Figure 1 The distribution of blood vessels of ovarian artery and its branches in sheep(1.5×) |
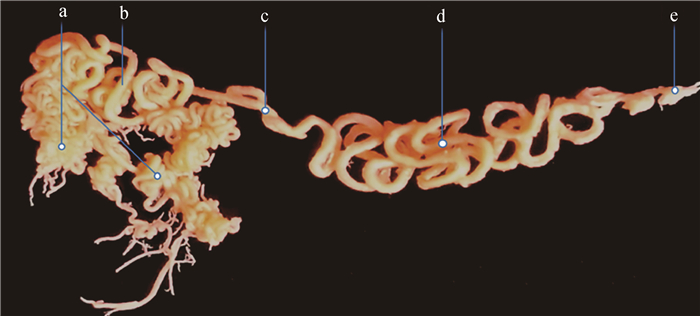
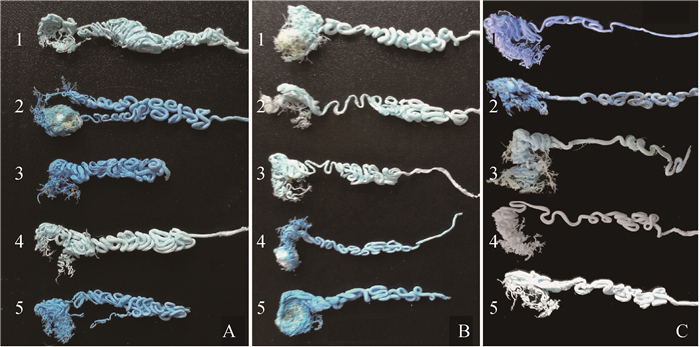
卵巢动脉及其分支被合并称为螺旋动脉或盘曲动脉[2],在本研究中获得的绵羊卵巢动脉卵巢支表现为典型的螺旋状结构,特别在卵巢支的中段动脉盘曲最为明显,而在近卵巢端盘曲减少(图 2)。进入卵巢门后又呈高度螺旋缠绕状,动脉及其分支呈拳头状紧密盘绕在卵巢门髓质部(图 2b),然后再发出微动脉向卵巢皮质部供血(图 2a)。通过对多个样本的观察,发现绵羊卵巢动脉的螺旋形态有一定的差异,主要表现在螺旋线圈的多寡及蟠曲缠结的形式,因此可将绵羊螺旋动脉形态分为重螺旋、螺旋及轻螺旋3种类型(图 3A、B、C)。另外,形成螺旋动脉的形式也各异,有紧密缠绕的弹簧状螺旋(图 3A1、A4),也有交错扭结的链锁状螺旋(图 3B1、B4),以及疏松盘绕的叠纹状螺旋(图 3C1、C2)。关于卵巢门螺旋,则表现为基本一致,呈紧密盘绕缠结的拳头状螺旋,然后从螺旋动脉尾端发出细小微动脉向卵巢内部供血,用于维持卵泡发育及黄体保持的血供(图 3)。绵羊卵巢的螺旋动脉有时候会出现分支,紧靠在主螺旋动脉上,并伴随进入卵巢门协助供血,同时会向卵巢皮质部发出小螺旋分支(图 3A2)。大多数情况是从卵巢螺旋动脉背侧发出的分支会越过卵巢,向输卵管供血。
|
a.卵巢微动脉;b.卵巢动脉卵巢门螺旋;c.卵巢动脉轻螺旋段;d.卵巢动脉重螺旋段;e.卵巢动脉主干 a. Ovarian arteriole; b. Ovarian hilum coiling artery; c. Ovarian slight spiral artery; d. Ovarian intensive spiral artery; e. Ovarian artery trunk 图 2 绵羊卵巢动脉卵巢支立体构筑(4×) Figure 2 Three-dimensional architecture of ovarian branches in sheep(4×) |
|
A.重螺旋动脉;B.螺旋动脉;C.轻螺旋动脉。1~5.样本编号 A. Intensive coiling artery; B. Ordinary coiling artery; C. Slight coiling artery. 1-5. Sample ID 图 3 绵羊卵巢动脉卵巢支不同的螺旋类型(1×) Figure 3 Different spiral types of ovarian arteries in sheep(1×) |
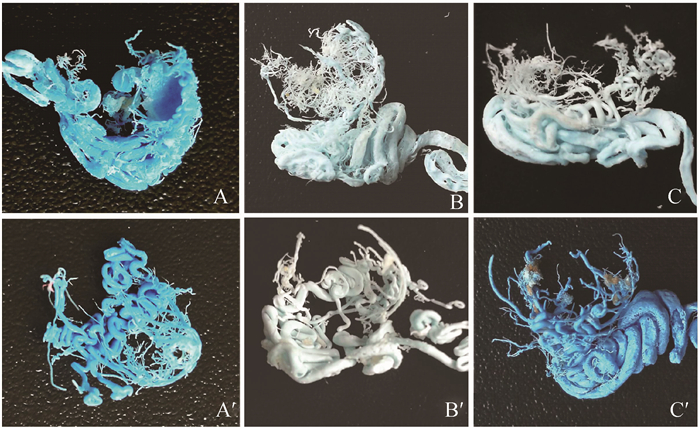
对于成年母羊,卵巢微动脉及其分支主要是供给卵泡成熟及黄体发育所需的养分及类固醇激素。在供给卵泡特别是成熟卵泡时,动脉分支仍然呈螺旋状托举在卵泡底部,然后分出许多微动脉向卵泡膜方向形成杯状网兜,以供给卵泡在充分发育时对营养素及代谢的需要(图 4A~C);在供给黄体特别是成熟黄体时,从卵巢门伸出的螺旋微动脉不仅呈托盘状分布在黄体底部,在黄体顶部也呈桶箍状分布,并发出小动脉供给成熟黄体各部位均衡的营养(图 4 A′~C′)。
|
A、B、C.卵泡微血管构筑;A′、B′、C′.黄体微血管构筑 A, B, C.Follicular arteriole architecture; A′, B′, C′. Luteal arteriole architecture 图 4 绵羊卵巢微动脉血管立体构筑(2.5×) Figure 4 Three-dimensional architecture of ovarian arteriole in sheep(2.5×) |
关于卵巢动脉和子宫动脉的起源,在哺乳动物间略有差别。在人类生殖系统中,卵巢动脉起源于腹主动脉,在肾动脉之下,输尿管的前方[11]。而起源于髂内动脉的子宫动脉在向子宫、输卵管供血行程中,在卵巢部位与卵巢动脉相交通,称为子宫动脉卵巢支[12]。而马、牛及骆驼的卵巢动脉与子宫动脉的交通情况与人类似,所不同的是家畜的子宫动脉起源于髂外动脉[9, 13]。从起源及分布来看,绵羊卵巢动脉与牛的相同,即起源于腹主动脉,在向卵巢供血进程中,发出子宫支和输卵管支,并与起源于髂外动脉的子宫动脉有交通支[9]。绵羊卵巢动脉,有国外学者将其称之为子宫-卵巢动脉[10],因在卵巢动脉走形过程中,亦有分支朝向子宫供血。绵羊的卵巢动脉在向卵巢供血行程中,具有发达的盘曲缠绕的螺旋动脉,且有时可见两条螺旋动脉伴行的状况。
3.2 绵羊卵巢螺旋动脉的特征及其功能哺乳动物卵巢动脉及其分支因其盘曲缠绕的行程被称为螺旋动脉或盘曲动脉,动脉血管的盘曲程度、分支多少等在不同物种间有所差别[2]。人类卵巢动脉的走形呈多个深度弯曲的波纹状[11]。朝向卵巢门的猴卵巢动脉显示了螺旋状走形,而卵巢门的卵巢动脉被分成两条一级分支,其管径较粗且包含螺旋状结构,该螺旋结构持续进入卵巢的髓质部[2]。猪的卵巢动脉在朝向卵巢的走形途中,环绕其长轴形成了螺旋形线圈,并在卵巢门之前发出了多达5~6个细小、紧密环绕的分支,且在卵巢蒂部位有多个吻合支出现[6]。小鼠的卵巢动脉从腹主动脉发出后,基本呈现直行的路径,但其接近卵巢门时趋向于略微卷曲走形[2]。在兔上的研究也显示,其卵巢门和髓质的血管也显示了对血流进行持续调控的螺旋动脉特征[14]。本研究中,绵羊的卵巢动脉显示了显著的螺旋形盘曲的特征,并与猪的卵巢螺旋动脉很类似。
关于螺旋动脉的功能,有研究认为,人、猴和猪卵巢动脉复杂的血管系统及特有的螺旋动脉归因于这些物种具有较长的性周期[15]。绵羊的发情周期为17~18 d,其螺旋动脉的盘曲程度比人发达的多,但性周期时间短于人类,因此螺旋动脉是否与性周期长短有关还需进一步探讨。猪卵巢的螺旋动脉及其分支可将卵巢动脉血压从高的水平降低到有效渗透血压的低水平[2]。本研究中观察到的绵羊卵巢螺旋动脉,在功能上应该与猪的类似。因为卵巢需要通过动脉血获取丰富营养的持续供应,并且必须借助动脉血管传递类固醇激素以调控复杂而精准的性周期的循环。卵泡血流状况与卵子的质量有关, 血流灌注丰富的卵泡中回收到的卵子的质量更好[16]。血管网的丰富程度决定优势卵泡的选择、成熟及排卵, 卵泡建立丰富的血管网可获得充足的营养及足量的激素供应[17]。基础状态下, 如果卵巢储备功能良好, 则卵巢的新陈代谢相对旺盛, 血流丰富, 血管阻力小[18]。绵羊卵巢动脉卵巢支及卵巢门的螺旋盘绕的血流特点,可以在很大程度上降低来自于腹主动脉的高压,从而给予卵巢低压且持续的血液供应,另外还可以缓冲由于运动、情绪波动所引发的血压变化,保证了性腺在动物生殖过程中供血的稳定性及优势卵泡的发育成熟。
3.3 绵羊卵巢微动脉特征及功能国内外许多学者通过不同灌注法对哺乳动物卵巢微血管进行了研究,通过代谢标志物对绵羊的卵巢微血管进行灌注[19],也有使用墨汁灌注来研究容易堵塞的小血管,并发现在灌注中特别是猪卵巢上黄体的存在与卵巢灌注失败密切相关[20]。目前利用血管腐蚀铸型结合扫描电镜的方法特别适合于微血管系统的形态学分析[21],本研究通过血管腐蚀铸型标本技术初步获得了绵羊卵巢微动脉的三维结构,可对其进行形态学观察。研究发现,绵羊卵巢支螺旋动脉在进入卵巢门前,呈弯曲较少的轻螺旋或伸展螺旋,当血管进入卵巢门后,又立即高度扭曲盘绕为重螺旋形态,且集中在卵巢髓质部,然后才逐步发出树枝状分支,向卵泡或黄体供血。在猪上的类似研究发现,卵巢动脉支进入卵巢门后,在髓质中呈扭曲、螺旋状走形,形成了众多螺旋状的小分支,但在皮质部是一些粗大的、盘曲少的分支[6]。而猴卵巢动脉的螺旋结构持续进入卵巢的髓质部,髓质被复杂的直径较粗的螺旋动脉丛所占据[2]。比较而言,绵羊卵巢门微动脉的螺旋形态与猪、猴两种哺乳动物十分类似,不同的是绵羊卵巢门微动脉在髓质部有更多蟠曲并呈拳头状紧密缠绕。
卵巢内微动脉主要负责卵泡发育、黄体生成过程中的血液及激素运送,特别在成熟卵泡和黄体上,动脉血管分布十分明显。例如在卵泡上,微动脉分布类似一个光滑表面的托盘状,黄体的动脉供应呈现不规则的桶箍状。这在其它哺乳动物上也有类似的发现,如兔卵巢门有主卵巢血供穿入卵巢,环绕卵泡和黄体微血管的表面看起来像血管球[4]。从卵巢看间质、卵泡及黄体铸型的微血管是非常丰富的,营养卵巢的大血管从卵巢门穿入实质[5]。在猪和牛的卵巢皮质部观察到与不同发育阶段卵泡相关的、多种规格及构造的血管网兜状结构[22]。而猪的成熟黄体一般通过直接起源于皮质动脉的单个分支来供血,当它到达黄体表面时,从中分出2条以上主血管网状分布在黄体表面,形成了一个环绕着黄体表面的类似于花冠状的血管环[6]。在绵羊的成熟黄体上,也发现了类似的花冠状结构及桶箍状动脉网络,成熟卵泡和黄体均有密集的毛细血管网,说明二者能够获得大量的血供。有研究显示,为响应雌激素和孕激素的分泌,一些重要的微血管重建会发生在黄体期[23],但这些微血管在未孕状态下又会随着孕激素的减少而收缩[24]。另外在妇女的超数排卵中, 卵巢动脉血主要供给募集后卵泡的持续发育,因此保证了优势卵泡的成熟[18], 这与在本研究观察到的卵泡微血管分布特征相似,即与绵羊卵泡的血供特点是一致的。
4 结论绵羊卵巢动脉的血管分布与普通牛类似,其分支包括卵巢支、子宫支及输卵管支;卵巢动脉卵巢支的螺旋盘绕形式可分为重螺旋、螺旋及轻螺旋3种,形态略有差异,部分个体有分支螺旋动脉伴行;卵巢支进入卵巢后,在卵巢门髓质部呈拳头状重螺旋折叠,末端发出卵泡或黄体微动脉,呈托盘状供血网络。绵羊卵巢动脉卵巢支的螺旋状盘绕特征,推测可降低来自于腹主动脉的高压,缓冲运动、情绪波动所引发的血压的变化,保证卵巢供血的稳定性及优势卵泡的成熟。
| [1] |
吴献青. 卵巢血管形成与卵巢生理[J]. 国外医学(计划生育分册), 2002, 21(2): 94–97.
WU X Q. Ovarian angiopoiesis and physiology[J]. Foreign Medical Sciences (Family Planning Fascicle), 2002, 21(2): 94–97. (in Chinese) |
| [2] | TAKADA S I, SHIMADA T, NAKAMURA M, et al. Vascular pattern of the mammalian ovary with special reference to the three-dimensional architecture of the spiral artery[J]. Arch Histol Jpn, 1987, 50(4): 407–418. DOI: 10.1679/aohc.50.407 |
| [3] |
陈春林, 黄睿, 刘萍, 等. 猪泌尿生殖系统动脉血管网模型的构建[J]. 中国实用妇科与产科杂志, 2008, 24(12): 906–909.
CHEN C L, HUANG R, LIU P, et al. Construction of the arterial vascular network models of pigs genitourinary system[J]. Chinese Journal of Practical Gynecology and Obstetrics, 2008, 24(12): 906–909. (in Chinese) |
| [4] | MURAKAMI T, IKEBUCHI Y, OHTSUKA A, et al. The blood vascular wreath of rat ovarian follicle, with special reference to its changes in ovulation and luteinization:a scanning electron microscopic study of corrosion casts[J]. Arch Histol Cytol, 1988, 51(4): 299–313. DOI: 10.1679/aohc.51.299 |
| [5] |
雷琦, 韩云明, 侯广琪, 等. 家兔卵巢血管立体构筑扫描电镜研究-甲基丙烯酸甲酯注射腐蚀铸型法[J]. 生殖与避孕, 1985, 5(3): 22–23.
LEI Q, HAN Y M, HOU G Q, et al. SEM studies on microvasculature of the rabbit ovary using methyl methacrylate injection-corrosion casts[J]. Reproduction & Contraception, 1985, 5(3): 22–23. (in Chinese) |
| [6] | HOSSAIN M I, O'SHEA J D. The vascular anatomy of the ovary and the relative contribution of the ovarian and uterine arteries to the blood supply of the ovary in the guinea-pig[J]. J Anat, 1983, 137(Pt 3): 457–466. |
| [7] | BIKO D M, SPANIER J F, NAGAMINE M, et al. Persistent secondary postpartum hemorrhage after uterine artery embolization[J]. J Vasc Interv Radiol, 2009, 20(2): 279–281. DOI: 10.1016/j.jvir.2008.10.016 |
| [8] |
欧阳振波. 数字化输卵管-卵巢动脉血管网模型的构建及其对PPH-UAE的意义[D]. 广州: 南方医科大学, 2010.
OUYANG Z B. Construction of digital fallopian tube-ovarian arterial vascular network model and the significance on PPH-UAE[D]. Guangzhou:Southern Medical University, 2010. (in Chinese) |
| [9] |
董常生.
家畜解剖学[M]. 北京: 中国农业出版社, 2015: 128.
DONG C S. Anatomy of domestic animal[M]. Beijing: China Agriculture Press, 2015: 128. (in Chinese) |
| [10] | STEVEN D H. Placental vessels of the foetal lamb[J]. J Anat, 1968, 103(Pt 3): 539–552. |
| [11] | AGUR A M R, DALLEY A F Ⅱ. Grant's atlas of anatomy[M]. 12th ed. Philadelphia:Lippincott Williams & Wilkins, 2008:243. |
| [12] |
彭裕文.
局部解剖学[M]. 北京: 人民卫生出版社, 2013: 177.
PENG Y W. Regional anatomy[M]. Beijing: People's Medical Publishing House, 2013: 177. (in Chinese) |
| [13] | HORST E K, HANS G L. Veterinary anatomy of domestic mammals:Textbook and color Atlas[M]. 6th ed. Stuttgart:Schattauer Press, 2014:463. |
| [14] | MACCHIARELLI G. The microvasculature of the ovary:A review by SEM of vascular corrosion casts[J]. J Reprod Dev, 2000, 46(4): 207–225. DOI: 10.1262/jrd.46.207 |
| [15] | JIANG J Y, MACCHIARELLI G, MIYABAYASHI K, et al. Follicular microvasculature in the porcine ovary[J]. Cell Tissue Res, 2002, 310(1): 93–101. DOI: 10.1007/s00441-002-0565-4 |
| [16] |
张燕, 杨菁, 徐望明, 等. 卵泡周围血流与体外受精-胚胎移植关系的研究[J]. 中华超声影像学杂志, 2007, 16(2): 145–147.
ZHANG Y, YANG J, XU W M, et al. Study on relationship between perifollicular blood flow and in vitro fertilization-embryo transfer[J]. Chinese Journal of Ultrasonography, 2007, 16(2): 145–147. (in Chinese) |
| [17] | AUGUSTIN H G. Vascular morphogenesis in the ovary[J]. Best Pract Res Clin Obstet Gynaecol, 2000, 14(6): 867–882. DOI: 10.1053/beog.2000.0132 |
| [18] |
王颖, 杨贵忠, 王丽萍, 等. 卵巢动脉血流与卵巢储备功能关系的研究[J]. 中国妇女健康研究, 2008, 19(5): 429–431.
WANG Y, YANG G Z, WANG L P, et al. A study on relationship between basal blood flow of ovarian artery and ovarian reserve function of women[J]. Chinese Journal of Woman and Child Health Research, 2008, 19(5): 429–431. (in Chinese) |
| [19] | TORRE A, BRAHIM F B, POPOWSKI T, et al. Factors related to unstained areas in whole ewe ovaries perfused with a metabolic marker[J]. Hum Reprod, 2013, 28(2): 423–429. DOI: 10.1093/humrep/des390 |
| [20] | GERRITSE R, BEERENDONK C C M, TIJINK M S, et al. Optimal perfusion of an intact ovary as a prerequisite for successful ovarian cryopreservation[J]. Hum Reprod, 2008, 23(2): 329–335. |
| [21] |
李忠华. 我国大体解剖技术学研究概况[J]. 解剖科学进展, 1996, 2(3): 249–253.
LI Z H. Research overview of gross anatomical technology in China[J]. Progress of Anatomical Sciences, 1996, 2(3): 249–253. (in Chinese) |
| [22] | SATO E, KAWAHARA M, SAKURAI M. Follicular microvasculature in the porcine and bovine ovary visualized by SEM of vascular corrosion casts[J]. Morphology, 2008, 3: 1–6. |
| [23] | DELIGDISCH L. Hormonal pathology of the endometrium[J]. Mod Pathol, 2000, 13(3): 285–294. DOI: 10.1038/modpathol.3880050 |
| [24] | KELLY R W, KING A E, CRITCHLEY H O D. Cytokine control in human endometrium[J]. Reproduction, 2001, 121(1): 3–19. DOI: 10.1530/rep.0.1210003 |



