2. 甘肃农业大学动物科学技术学院, 兰州 730070;
3. 北京百年栗园生态农业有限公司, 北京 101500;
4. 北京畜牧总站, 北京 102200
2. College of Animal Science and Technology, Gansu Agricultural University, Lanzhou 730070, China;
3. Beijing Bainianliyuan Ecological Agriculture Co., LTD, Beijing 101500, China;
4. Beijing General Station of Animal Husbandry Service, Beijing 102200, China
随着人类生活水平的逐步提高,对肉类产品的需求量也逐渐增加。鸡肉是全球产量最大的肉品,市场需求吸引众多养殖者投资到肉鸡养殖行业中,也促进了肉种鸡行业的发展。根据中国畜牧业协会监测数据,1~12月全国父母代肉种鸡平均存栏量约4 447.36万套。促进种鸡适时性成熟,对于提高肉种鸡生产力,降低鸡苗生产成本具有重要意义。影响肉种鸡生产力的诸多因素中,环境条件占50%~95%[1],其中,光环境是重要因素之一,对繁殖性能具有调控作用。鸡下丘脑在接受光照刺激后分泌促性腺激素释放激素[2],进而刺激下丘脑—垂体—性腺轴中诸多激素释放,促进卵泡生成和排卵,使种鸡适时开产[3-5]。因此,光环境合理调控对肉种鸡性成熟及后期繁殖性能发挥尤为重要。
肉种鸡在18周龄接受光照刺激(Photostimulation,PS)能加快性成熟,促进卵泡形成[6],但产蛋期的小蛋和脏蛋偏多[7-8],且个体间达到开产体重、体成熟的时间不同,较早光照刺激会降低群体整齐性[9];也有研究表明,与18周龄光照刺激时间比较,22周龄光照刺激可使肉种鸡开产整齐性提高,但会推迟性成熟时间[6, 9-10],导致累积产种蛋数减少,种鸡利用周期缩短。不同光照刺激时间对肉种鸡性成熟和繁殖性能存在影响,需要进一步优化。本试验以AA父母代肉种鸡为对象,从生长发育、激素水平、性成熟和早期蛋品质的角度研究肉种鸡性成熟对光照刺激时间的差异化响应,并对光照刺激后肉种鸡性腺发育和激素水平等动态跟踪,为肉种鸡光环境调控和光照刺激方案的选择提供科学依据。
1 材料与方法 1.1 试验动物与试验设计选取中国农业科学院北京畜牧兽医研究所昌平基地试验鸡场600只1日龄AA父母代种母雏。1~13周龄阶段网上平养。14周龄选取体重相近、健康的母鸡384只,随机分为4个处理,每个处理2个重复,每个重复饲养在独立空间内。种母鸡单笼饲养,全期依据《爱拔益加父母代肉种鸡饲养管理手册》进行限制饲喂,自由饮水。采用LED光源,0~3 d光照节律为24 h光照:0 h黑暗(24L:0D),通过照度计(型号:DT-1301,深圳,华盛昌)测定鸡背高度的光照强度40 lx。2~15周龄保持光照节律8L:16D,光照强度10 lx。各处理光照刺激时间分别为16(PS16)、18(PS18)、20(PS20)和22周龄(PS22)。
光照刺激程序:PS16在16周龄初,光照强度由10 lx增加至80 lx,17周龄初光照时长由8 h直接提高至12 h,随后每周初增加1 h,至光照节律保持14L:10D为止。PS18、PS20和PS22光照刺激程序均参照PS16,但光照刺激时间分别为18、20和22周龄初,其他条件一致。试验参照中华人民共和国农业行业标准《鸡饲养标准》(NY/T33-2004)配制白羽肉种鸡饲粮,依据《爱拔益加AA+父母代饲养管理手册》在光照刺激当日更换产蛋期饲料。
1.2 测定指标与方法各处理在光照刺激前1 d,随机挑出6只健康种鸡,屠宰测定生长发育指标,另选30羽测定血清激素水平。光照刺激后,每隔2周进行屠宰试验和采集血样,用以追踪各处理光照刺激后6周内的指标数据。
1.2.1 生长发育指标肉种鸡每周称重,饲养至15周龄末,各处理按上述计划屠宰。屠宰前1 d,每个重复挑选15只鸡用游标卡尺测量髋骨宽度。每个重复随机挑选3只鸡,断料12 h。记录宰前活重,宰后称量屠体重。参照《家禽生产性能名词术语和度量统计方法》(NY/T823-2004)对胴体分割,称量屠体重、净膛重、腹脂重、卵巢重和输卵管重,计算腹脂率和性腺指数[11]。鸡冠和输卵管拍照记录,使用Digimizer软件计算鸡冠面积和输卵管长度。
1.2.2 激素指标屠宰当天每个重复挑选15只鸡,翅静脉采集血样离心(3 000 r·min-1×20 min,4 ℃)分离血清,并保存于-20 ℃。通过放免法测定雌二醇(E2)水平。
1.2.3 性成熟指标各处理光照刺激后详细记录产蛋数,统计见蛋日龄、开产日龄(5%产蛋率日龄)、见蛋~开产的间隔时间和光照刺激~开产的间隔时间。
1.2.4 产蛋初期蛋品质指标试验期内,收集5%产蛋率时连续3 d的蛋。通过蛋形指数测定仪(型号:NFN383,日本,FHK)测量蛋的长径和短径,计算蛋形指数(长径/短径);通过蛋壳厚度测试仪(型号:ESTG-1,以色列,ORKA)测定蛋锐端、中部、钝端的蛋壳厚度并计算平均值;蛋壳强度测试仪(型号:EFR-01,以色列,ORKA)测定蛋壳强度;鸡蛋全功能测定仪(型号:EA-01,以色列,ORKA)测定蛋重、蛋白高度、蛋黄颜色和哈氏单位。电子天平称量蛋黄重和蛋壳重量,同时计算蛋黄比率和蛋壳比率。
1.3 数据分析采用SAS8.1对数据进行单因素方差分析,各处理均数之间采用Duncan’s多重比较检验估计,P < 0.05认为差异显著。其中蛋黄比率和蛋壳比率数据通过反正弦转换后,再进行方差分析和Duncan’s多重比较检验。数据以“平均值±标准差”的形式表示。
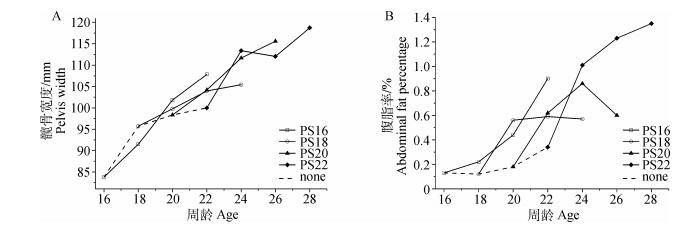
2 结果 2.1 不同光照刺激时间对肉种鸡生长发育的影响如图 1A所示,在16~18周龄时,PS16光照刺激后髋骨宽度的增长速度慢于PS18未加光刺激状态。由图 1B所示,肉种鸡未接受光照刺激时腹脂沉积缓慢;加光刺激后,腹脂率上升,且PS22在光照刺激6周后的腹脂率高于其他组。
|
none、PS16、PS18、PS20和PS22分别代表加光刺激前、16周龄、18周龄、20周龄和22周龄加光刺激。下同 none, PS16, PS18, PS20, PS22 mean before photostimulation, and photostimulation at 16, 18, 20 and 22 wk of age respectively. The same as below 图 1 不同光照刺激时间下肉种鸡生长发育 Figure 1 Growth of broiler breeders from different photostimulation groups |
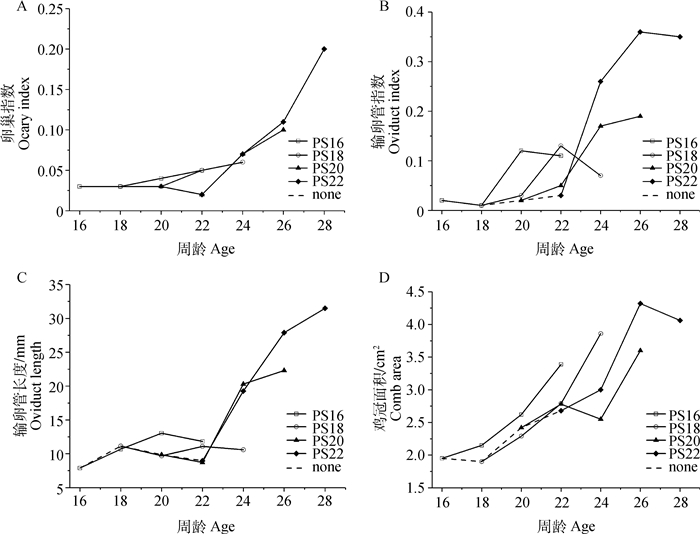
由图 2A可见,PS16和PS18在光照刺激后6周内,卵巢指数无明显变化,PS20和PS22在加光刺激2周时卵巢指数已明显增长;加光刺激6周时,PS22的卵巢指数高出其他组1~2倍。如图 2B、2C所示,肉种鸡未接受光照刺激时,输卵管指数和输卵管长度较低。加光刺激4周后,各处理输卵管指数均见明显增长,PS22输卵管指数的增长速度快于其他3组;光照刺激6周时,PS22的输卵管长度是PS16和PS18的2.5倍。由图 2D所示,未加光刺激时,肉种鸡18周龄鸡冠面积开始增长,而PS16在光照刺激后鸡冠面积迅速增加。
|
图 2 不同光照刺激时间下肉种鸡生殖器官发育 Figure 2 Reproductive organ characteristics of broiler breeders from different photostimulation groups |
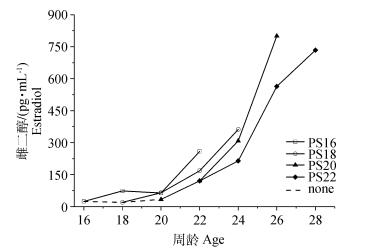
如图 3所示,肉种鸡未加光刺激时,各处理E2水平较低;PS16在光照刺激后4周时,E2水平略高于其他处理未加光阶段;加光刺激6周内,PS20和PS22的E2浓度增长明显快于PS16和PS18;加光刺激6周时,PS20和PS22的E2浓度是PS16和PS18的2倍。
|
图 3 不同光照刺激时间下血清雌二醇水平 Figure 3 Plasma estradiol concentration of broiler breeders from different photostimulation groups |
由表 1可见,光照刺激时间对AA肉种鸡见蛋日龄和开产日龄无显著影响(P>0.05)。PS16见蛋~开产的间隔时间和光照刺激~开产的间隔时间均多于其他3组(P=0.007 9,P=0.000 1)。
|
|
表 1 光照刺激时间对肉种鸡性成熟的影响 Table 1 Effect of age at photostimulation on sexual maturity of broiler breeders |
由表 2所示,PS16的开产体重显著高于其他3组(P=0.000 1)。PS18的蛋壳重显著低于PS16和PS22(P=0.005 1)。PS16的蛋壳厚度和蛋壳强度有高于其他组的趋势(P=0.083 4,P=0.066 2)。PS22平均蛋重有高于其他3组的趋势(P=0.062 4)。其他蛋品质指标不受光照刺激时间的影响(P>0.05)。
|
|
表 2 光照刺激时间对肉种鸡产蛋初期蛋品质的影响 Table 2 Effect of age at photostimulation on egg quality of broiler breeders in early laying period |
雌性动物与繁殖相关的一系列活动均与卵巢的机能密切相关。光照刺激之前母禽的卵巢较小,光照刺激后会加速性腺发育[12]。肉种鸡具有吃得快、消化快、吸收好和增重快等特点,所以育成期必须采用有效的限饲程序来控制体重。限饲还使性成熟适时化、同期化。本试验发现,肉种鸡未接受光照刺激时,性腺发育极为缓慢。早期光照刺激如16和18周龄补充光照,虽对性腺有刺激作用,但并未使性腺发育加速。这可能是肉种鸡体成熟未达标所引起。22周龄光照刺激,能促进肉种鸡性腺发育,进一步解释体成熟是否达标对性成熟具有一定的限制作用。因此,实际生产中,合理调控肉种鸡体成熟和性成熟关系,对其繁殖性能的发掘具有重要意义。具有刺激作用的光照能够促进肉种鸡体内激素变化,进而促进其性发育和性成熟。解美娜等[13]研究发现,卵泡刺激素和E2协同作用能刺激鸡卵巢生殖细胞增殖。R. L. Walzem[14]研究发现,E2可促进肝合成卵黄前体物质,随后进入卵泡并沉积在卵巢上。
禽类的输卵管不仅是运送卵子和受精的场所,同时也担负着形成蛋的卵白、壳膜、蛋壳、角质薄膜,并具有较长时间贮存精子的功能。本试验中,光照刺激时间对输卵管发育的影响与卵巢的相似。R. A. Renema等[15]研究也发现,在肉种鸡性成熟时,22周龄加光刺激的输卵管重>18周龄加光刺激组。本试验各处理未加光时,输卵管指数较低,即可能处于缓慢发育期。肉种鸡在16或18周龄加光刺激时,输卵管指数在加光刺激两周后增长,而输卵管长度维持稳定。这种输卵管指数与长度增长的延迟差异可能与输卵管在发育缓慢期的机制有关。输卵管在发育缓慢期主要进行细胞的增殖活动,并不涉及细胞的分化过程。而在发育快速期,则开始出现细胞分化,同时伴随细胞的增殖[16]。本试验20和22周龄加光刺激的输卵管发育状态与其E2水平增长相似。研究表明,雌激素可刺激输卵管细胞增殖和上皮细胞的分化[17]。外源注射雌激素可使母鸡输卵管在3 d内快速增大[18]。本试验发现,各处理光照刺激后输卵管均优先于卵巢发育。V. L. Melnychuk等[19]研究表明,卵巢排出的第一枚卵能否被输卵管漏斗部接纳,这与输卵管成熟和活动密切相关。若输卵管与卵巢成熟不协调,则在性成熟时容易发生内部排卵,这也反映了输卵管在排卵一刻的接纳能力。
本试验中,不同光照刺激时间对AA肉种鸡见蛋日龄和开产日龄统计无差异,但16周龄光照刺激的开产日龄比22周龄光照刺激晚9.27 d。造成此情况的原因主要与早期光照刺激导致肉种鸡开产整齐性差有关。R. A. Renema[15]和T. Yuan等[8]研究发现,肉种鸡延迟光照刺激时间,可导致开产日龄明显推迟,与本研究结果的不同,可能是试验品种不同。V. L. Melnychuk等[20]研究发现,肉种鸡在21与24周龄加光刺激的见蛋日龄无显著差异。本试验中,16或18周龄加光刺激的见蛋日龄邻近,与A. A. Idris[21]的研究结果一致。16周龄光照刺激的见蛋~开产的间隔时间和光照刺激~开产的间隔时间长于其他3组,与R. A. Renema[15]和T. Yuan等[8]研究结果一致。可能是肉种鸡在16周龄时未达到体成熟,过早光照刺激致使体况发育停止,换为产蛋期饲料后营养用于生产储备和脂肪沉积,从而导致性腺发育和E2增长缓慢。虽个别体况较佳,个体性成熟提前,但大部分个体体况变差,致使开产整齐性变差。光照刺激数周后,即使达到体成熟,鸡群也处于光失敏状态,即对光照刺激不再具有反应能力,因此性成熟明显延迟[22]。由此可知,肉种鸡过早接受光照刺激并不一定能促进性成熟。若早期体成熟未达标时进行光照刺激,容易导致鸡群光失敏。反之,适当推迟光照刺激时间能够提高肉种鸡开产整齐性。
肉种鸡开产后所产蛋尽快达到种蛋标准对于提高种鸡利用率具有重要意义。本试验中18、20和22周龄加光组,随着光照刺激时间的推迟,肉种鸡产蛋初期平均蛋重逐渐增加,与T. Yuan等[8]的研究结果一致。在20和22周龄加光刺激的肉种鸡产蛋早期平均蛋重大于52 g,最快达到作为种蛋的标准[23]。16周龄加光刺激并没有促进性成熟,肉种鸡开产时间反而最晚,可能是用以生产为主的能量提供体重增长,使开产体重显著高于其他各处理,这也导致了平均蛋重的增加。18周龄加光刺激的蛋壳重量低于16和22周龄加光刺激,但蛋壳重主要与蛋重有关,试验中的蛋壳比率无显著差异,16周龄光照刺激时的蛋壳厚度和蛋壳强度有高于其他3组的趋势。蛋壳主要在输卵管子宫部形成,且卵形成蛋的过程中,在输卵管子宫部形成蛋壳所耗时间最长,约19~29 h[24]。16周龄光照刺激时可能输卵管发育未完全成熟,输卵管机能还未完善,钙分泌异常,致使蛋在输卵管子宫部停留时间较长,这一现象还需进一步深入研究。本试验发现,不同光照刺激时间对肉种鸡产蛋初期蛋品质存在影响,且22周龄光照刺激时间可改善肉种鸡产蛋初期蛋品质。
脂肪组织是动物重要的储能器官[25]。同时,卵黄中65%的固体成分是脂蛋白复合体,其中88%为脂类,这也是母鸡沉积一定量体脂有利于开产和持续产蛋的原因[26-28]。M. N. Katanbaf等[29]指出,在限饲条件下,影响家禽性成熟的主要因素是体重,当家禽体重增长到某一阈值时就会启动性腺的发育。而越来越多的人指出“关键体重”的实质是“关键脂肪水平”[30]。本试验中,各处理腹脂率在加光刺激后均快速增加。肉种鸡在22周龄加光刺激的腹脂沉积速度最快,与M. J. Zuidhof等[23]的研究结果一致。R. A. Renema等[6]研究发现,18和22周龄加光刺激对腹脂率没有影响。对于雌禽,E2可增加血脂和脂肪在组织中的储存[31],本研究中也发现22周龄加光刺激后,E2水平增长最高。这可能是本试验中22周龄加光刺激腹脂率较高的原因。因此,22周龄光照刺激可能更有利于肉种鸡开产前脂肪沉积。
4 结论光照刺激时间对AA肉种鸡性腺发育速度、开产日龄和产蛋初期蛋品质存在影响。肉种鸡过早接受光照刺激,易引起群体发生光失敏情况。在16周龄光照刺激对肉种鸡性腺发育和E2分泌等刺激作用较差,开产时间延迟。在22周龄进行光照刺激,既可保证肉种鸡性腺和E2水平对光刺激的敏感性,又能改善开产整齐性,促进产蛋前期种蛋尽快达到种用标准,可提高肉种鸡种用性能。
| [1] |
杨宁.
家禽生产学[M]. 北京: 中国农业出版社, 2002.
YANG N. Poultry science[M]. Beijing: China Agriculture Press, 2002. (in Chinese) |
| [2] | DUNN I C, SHARP P J. Photo-induction of hypothalamic gonadotrophin releasing hormone-I mRNA in the domestic chicken:A role for oestrogen?[J]. J Neuroendocrinol, 1999, 11(5): 371–375. |
| [3] | LEWIS P D, PERRY G C, MORRIS T R, et al. Effect of constant and of changing photoperiod on plasma LH and FSH concentrations and age at first egg in layer strains of domestic pullets[J]. Br Poult Sci, 1998, 39(5): 662–670. DOI: 10.1080/00071669888548 |
| [4] | LEWIS P D, CIACCIARIELLO M, CICCONE N A, et al. Lighting regimens and plasma LH and FSH in broiler breeders[J]. Br Poult Sci, 2005, 46(3): 349–353. DOI: 10.1080/00071660500098509 |
| [5] | SHARP P J. Photoperiodic regulation of seasonal breeding in birds[J]. Ann N Y Acad Sci, 2005, 1040(1): 189–199. DOI: 10.1196/annals.1327.024 |
| [6] | RENEMA R A, ROBINSON F E, GOERZEN P R. Effects of altering growth curve and age at photostimulation in female broiler breeders. 1. Reproductive development[J]. Can J Anim Sci, 2001, 81(4): 467–476. DOI: 10.4141/A00-109 |
| [7] | RENEMA R A, SIKUR V R, ROBINSON F E, et al. Effects of nutrient density and age at photostimulation on carcass traits and reproductive efficiency in fast-and slow-feathering turkey hens[J]. Poult Sci, 2008, 87(9): 1897–1908. DOI: 10.3382/ps.2007-00431 |
| [8] | YUAN T, LIEN R J, MCDANIEL G R. Effects of increased rearing period body weights and early photostimulation on broiler breeder egg production[J]. Poult Sci, 1994, 73(6): 792–800. DOI: 10.3382/ps.0730792 |
| [9] | ROBINSON F E, WAUTIER T A, HARDIN R T, et al. Effects of age at photostimulation on reproductive efficiency and carcass characteristics. 1. Broiler breeder hens[J]. Can J Anim Sci, 1996, 76(3): 275–282. DOI: 10.4141/cjas96-042 |
| [10] | HOCKING P M. Role of body weight and food intake after photostimulation on ovarian function at first egg in broiler breeder females[J]. Br Poult Sci, 1996, 37(4): 841–851. DOI: 10.1080/00071669608417913 |
| [11] |
李云雷, 孙研研, 华登科, 等. 不同光色对黄羽肉鸡生产性能、胴体性能及性征发育的影响[J]. 畜牧兽医学报, 2015, 46(7): 1169–1175.
LI Y L, SUN Y Y, HUA D K, et al. Effects of light color on production and carcass performance and sexual characteristics in Yellow-feathered broilers[J]. Acta Veterinaria et Zootechnica Sinica, 2015, 46(7): 1169–1175. (in Chinese) |
| [12] | JOSEPH N S, ROBINSON F E, RENEMA R A, et al. Responses of two strains of female broiler breeders to a midcycle increase in photoperiod[J]. Poult Sci, 2002, 81(6): 745–754. DOI: 10.1093/ps/81.6.745 |
| [13] |
解美娜, 张才乔, 米玉玲, 等. 卵泡刺激素和雌激素对培养的鸡胚卵巢生殖细胞增殖的影响[J]. 动物学研究, 2004, 25(1): 53–56.
XIE M N, ZHANG C Q, MI Y L, et al. Effects of follicle-stimulating hormone and estrogen on development of embryonic chicken germ cell in vitro[J]. Zoological Research, 2004, 25(1): 53–56. (in Chinese) |
| [14] | WALZEM R L. Lipoproteins and the laying hen:Form follows function[J]. Avlan Poult Biol Rev, 1996, 7(1): 31–64. |
| [15] | RENEMA R A, ROBINSON F E, ZUIDHOF M J. Reproductive efficiency and metabolism of female broiler breeders as affected by genotype, feed allocation, and age at photostimulation. 2. Sexual maturation[J]. Poult Sci, 2007, 86(10): 2267–2277. DOI: 10.1093/ps/86.10.2267 |
| [16] | JOENSUU T K, YLIKOMI T J, TOFT D O, et al. Progesterone-induced Avidin as a marker of cytodifferentiation in the oviduct:Comparison to ovalbumin[J]. Endocrinology, 1990, 126(2): 1143–1155. DOI: 10.1210/endo-126-2-1143 |
| [17] | COMSTOCK J P, ROSENFELD G C, O'MALLEY B W, et al. Estrogen-induced changes in translation, and specific messenger RNA levels during oviduct differentiation[J]. Proc Natl Acad Sci U S A, 1972, 69(9): 2377–2380. DOI: 10.1073/pnas.69.9.2377 |
| [18] | SONG G, SEO H W, CHOI J W, et al. Discovery of candidate genes and pathways regulating oviduct development in chickens[J]. Biol Reprod, 2011, 85(2): 306–314. DOI: 10.1095/biolreprod.110.089227 |
| [19] | MELNYCHUK V L, ROBINSON F E, RENEMA R A, et al. Carcass traits and reproductive development at the onset of lay in two lines of female turkeys[J]. Poult Sci, 1997, 76(9): 1197–1204. DOI: 10.1093/ps/76.9.1197 |
| [20] | MELNYCHUK V L, KIRBY J D, KIRBY Y K, et al. Effect of strain, feed allocation program, and age at photostimulation on reproductive development and carcass characteristics of broiler breeder hens[J]. Poult Sci, 2004, 83(11): 1861–1867. DOI: 10.1093/ps/83.11.1861 |
| [21] | IDRIS A A, ROBBINS K R. Light and feed management of broiler breeders reared under short versus natural day length[J]. Poult Sci, 1994, 73(5): 603–609. DOI: 10.3382/ps.0730603 |
| [22] | LUPICKI M E. Ovarian morphology and steroidogenesis in domestic fowl (Gallus domesticus):Effects of aging, strain, photostimulation program and level of feeding[D]. Alberta:University of Alberta, 1994. |
| [23] | ZUIDHOF M J, RENEMA R A, ROBINSON F E. Reproductive efficiency and metabolism of female broiler breeders as affected by genotype, feed allocation, and age at photostimulation. 3. Reproductive efficiency[J]. Poult Sci, 2007, 86(10): 2278–2286. DOI: 10.1093/ps/86.10.2278 |
| [24] |
刘龙. 蛋鸡输卵管膨大部在自然发育过程中各阶段转录组变化情况研究[D]. 北京: 中国农业大学, 2014.
LIU L. The transcriptional landscape of natural developmental magnum in chickens[D]. Beijing:China Agricultural University, 2014. (in Chinese) |
| [25] | FANTUZZI G. Adipose tissue, adipokines, and inflammation[J]. J Allergy Clin Immunol, 2005, 115(5): 911–919. DOI: 10.1016/j.jaci.2005.02.023 |
| [26] |
李云雷. 北京油鸡不同阶段脂肪沉积与繁殖性能的相关性研究[D]. 北京: 中国农业科学院, 2016.
LI Y L. Correlation analysis between fat deposition and reproductive performance of beijing you chickens at different stages[D]. Beijing:Chinese Academy of Agricultural Sciences, 2016. (in Chinese) |
| [27] | GRIFFIN H D, WHITEHEAD C C. Identification of lean or fat turkeys by measurement of plasma very low density lipoprotein concentration[J]. Br Poult Sci, 1985, 26(1): 51–56. DOI: 10.1080/00071668508416786 |
| [28] | BORNSTEIN S, PLAVNIK I, LEV Y. Body weight and/or fatness as potential determinants of the onset of egg production in broiler breeder hens[J]. Br Poult Sci, 1984, 25(3): 323–341. DOI: 10.1080/00071668408454873 |
| [29] | KATANBAF M N, DUNNINGTON E A, SIEGEL P B. Restricted feeding in early and late-feathering chickens.:1. Growth and physiological responses[J]. Poult Sci, 1989, 68(3): 344–351. DOI: 10.3382/ps.0680344 |
| [30] | FOSTER D L, NAGATANI S. Physiological perspectives on leptin as a regulator of reproduction:Role in timing puberty[J]. Biol Reprod, 1999, 60(2): 205–215. DOI: 10.1095/biolreprod60.2.205 |
| [31] |
王建辰, 章孝荣.
动物生殖调控[M]. 合肥: 安徽科学技术出版社, 1998.
WANG J C, ZHANG X R. Animal reproductive regulation[M]. Hefei: Anhui Science & Technology Publishing House, 1998. (in Chinese) |



