土壤的重金属污染是世界范围内普遍存在的环境问题之一,主要由采矿、冶炼、废物处理、农药和化肥应用等人类活动引起[1-3],给生态环境和人类健康造成严重威胁。目前,重金属污染土壤的处理方法可分为分离和钝化2类[4],前者以降低土壤重金属含量为目标,如植物萃取[5]、淋洗[6-8],后者以降低土壤重金属活性和迁移能力为目标,如固化、稳定化[9]。植物修复成本低,但周期长[6],淋洗修复效率高,周期短,适用性广,但如果处理不当则易造成二次污染[10-11]。
乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)对多种重金属具有很强的螯合能力,对土壤重金属的洗脱能力较强[12]。但EDTA难于生物降解,在土壤中残留时间长,可能导致土壤功能退化[13]。乙二醇双(2-氨基乙基醚)四乙酸〔ethylenebis (oxyethylenenitrilo) tetraacetic acid,EGTA〕易生物降解且对铅、镉的螯合能力与EDTA相当,但很少研究关注其对土壤重金属的洗脱效果以及淋洗后土壤中残留重金属的环境风险[14-15]。对于螯合剂,通常优先洗脱毒性强、易移动、生物有效性大的活性组分[16],残留于土壤中的螯合剂可能活化土壤中的非活性组分[17],导致残留重金属的移动性和生物有效性增加,浸出风险加大[18-19]。
与淋洗不同,固化/稳定化的主要目的是钝化土壤重金属,降低其迁移能力和生物有效性,从而降低土壤环境的潜在风险。含磷材料可通过诱导土壤中重金属形成稳定的磷酸盐沉淀而降低活性态重金属浓度,使其生物可利用性下降[9],但过量使用磷酸盐也可能导致其通过降雨径流或淋溶进入地下水或周边地表水[20]。此外,钝化处理后重金属元素仍残留在土壤中,环境条件的变化可能引起重金属的再次活化和释放[21]。
针对以上分析,笔者综合利用淋洗与钝化的优势,首先采用可生物降解螯合剂洗脱部分土壤重金属,然后采用含磷材料进行钝化处理以降低残留重金属的生物有效性,通过毒性浸出法(toxicity characteristic leaching procedure,TCLP)评价各重金属的稳定化效果。研究了EGTA对土壤重金属洗脱率和浸出浓度的影响以及重过磷酸钙(triple super phosphate,TSP)对重金属浸出浓度的影响;采用响应面中心组合设计法,模拟淋洗与钝化联合处理对重金属的淋洗效果和TCLP浸出毒性的影响;采用综合考虑土壤重金属残留量、生物有效性和毒性的环境风险削减率评价方法,拟合环境风险削减率与修复条件之间的关系并进行优化,为重金属污染土壤修复和风险管控提供科学依据。
1 材料与方法 1.1 供试材料干净土壤样品取自常州科教城明行楼附近的菜地(31°41′11″ N,119°57′24″ E),取样深度为0~20 cm,在室温条件下(25±2) ℃风干,研磨过2 mm孔径筛后,分别加入一定量CuSO4·5H2O、ZnSO4·7H2O、Pb(NO3)2和CdCl2·5H2O进行染土并静置1 a。采用四分法取部分土样,研磨后过0.15 mm孔径筛,供重金属全量分析用。供试土壤重金属质量含量:Cu,583.29 mg·kg-1;Zn,768.92 mg·kg-1;Pb,803.00 mg·kg-1;Cd,15.83 mg·kg-1。TCLP浸出质量浓度:Cu,14.42 mg·L-1;Zn,24.45 mg·L-1;Pb,0.83 mg·L-1;Cd,0.47 mg·L-1。供试土壤基本理化性质:pH为6.18,阳离子交换量(cation exchange capacity,CEC)为20.50 cmol·kg-1,w(有机质)为2.64%,w(黏粒)为32.80%,w(粉粒)为42.27%,w(砂粒)为24.93%。
1.2 实验设计首先研究淋洗条件的影响,包括EGTA投加量、液固比和淋洗时间3个对重金属洗脱率影响较大的因素,确定最佳淋洗条件,然后研究钝化剂投加量的影响。根据前期实验结果和相关研究[22-23]报道,确定EGTA投加量、液固比、淋洗时间和TSP投加量4个因素的取值范围。其中,EGTA投加量分别为0.1、0.2、0.5、1.0和2.0 g·L-1,淋洗时间分别为0.5、1、2和4 h,液固比分别为2.5、5和10,TSP投加量w分别为0%、1%、2%和5%。
在上述单因素实验基础上,进一步以EGTA投加量、液固比和TSP投加量为主要考察因素,并以+1、0和-1分别代表因素的高、中和低3个水平(表 1),采用响应面法中Box-Behnken模型设计中心复合实验,共得到17个实验处理。每个处理称取5 g土于100 mL离心管中,加入一定量淋洗剂,按实验条件控制各因素,于恒温振荡箱中以180 r·min-1振荡淋洗相应时间后,在4 000 r·min-1条件下离心(相对离心力为1 776)10 min,取上清液用火焰原子吸收分光光度计测定重金属离子浓度。在淋洗后的土壤中加入一定量TSP,保持质量含水率为50%,将钝化剂与土壤搅拌均匀,风干10 d后测定TCLP浸出液浓度,每个实验处理重复3次,最后取平均值作为对应处理的最终值。
|
|
表 1 响应面设计实验因素及水平 Table 1 Factors and levels of response surface methodology (RSM) |
土壤样品中重金属Cu、Zn、Pb和Cd经HNO3-HClO4-HF法消解,采用火焰原子吸收分光光度计测定重金属含量,测定条件见表 2,消解过程中所用的化学试剂均为优级纯。精密度(RSD)和回收率测定实验结果见表 3。采用TCLP评价处理前后土壤中残留重金属的浸出性能[24]。TCLP提取条件:将5.7 mL冰醋酸溶于去离子水中,定容至1 L(pH为2.88±0.05),m(土):V(缓冲液)为1:20,以(30±2) r·min-1在常温条件下振荡(18±2) h,离心,过滤后用火焰原子吸收分光光度计测定TCLP提取液浓度。土壤pH采用玻璃电极法测定,V(液): m(土)为2.5:1,供试土壤pH均大于5。其他土壤理化性质指标参照《土壤农业化学分析方法》的常规方法[25]测定。
|
|
表 2 火焰原子吸收光谱的工作条件 Table 2 Working condition of flame atomic absorption spectrometry |
|
|
表 3 精密度和回收率的实验结果 Table 3 The results of precision and recovery experiment |
采用SPSS 25统计软件对实验数据进行回归分析、ANOVA方差显著性分析和LSD检验(取对数),其中显著性检测限为P < 0.05,采用Origin 9.0软件制图。
1.5 环境风险评价环境风险削减率由修复前后土壤重金属环境风险指数的差值占修复前土壤重金属环境风险指数的比例来确定,计算公式为
| $ \beta = 1 - R/{R_0} \times 100\%。$ | (1) |
式(1)中,β为总环境风险削减率,%;R0和R分别为处理前后土壤重金属环境风险指数。
土壤重金属环境风险评价应综合考虑土壤重金属污染水平及残留重金属的二次污染风险,计算公式为
| $ R = \sqrt {\sum\limits_{i = 1}^n {{P_i} {\times T}_i} } 。$ | (2) |
式(2)中,Pi为第i种重金属富集系数,反映土壤残留重金属的污染程度,计算公式为
| $ {P_i} = \frac{{{C_{{\rm{S}}, i}}}}{{{C_{{\rm{B}}, i}}}}。$ | (3) |
式(3)中,CS,i为土壤中第i种重金属残留量,mg·kg-1;CB,i为土壤中第i种重金属背景值,采用江苏省土壤重金属背景值[26],w(Cu)、w(Zn)、w(Pb)和w(Cd)分别为23.40、64.80、22.00和0.085 mg·kg-1。
土壤重金属的二次污染风险首先源于土壤重金属的有效性和迁移能力,其次与重金属自身的毒性差异有关,采用土壤重金属浸出毒性指数(Ti)来评价,计算公式为
| $ {T_i} = \frac{{{G_{{\rm{S}}, i}}}}{{{G_{{\rm{B}}, i}}}}。$ | (4) |
式(4)中,GS,i为第i种重金属的TCLP浸出浓度,mg·L-1;GB,i为地下水环境质量三级标准限值[27],w(Cu)、w(Zn)、w(Pb)和w(Cd)分别为1、1、0.01和0.005 mg·L-1,以其倒数反映重金属生理毒性的相对差异。
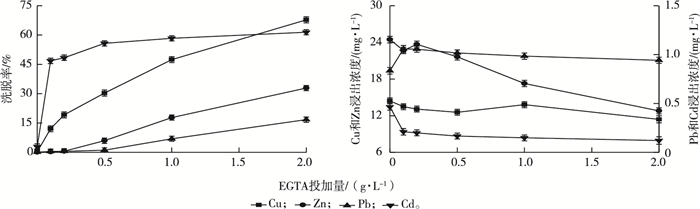
2 结果与讨论 2.1 EGTA对土壤重金属洗脱率和浸出浓度的影响 2.1.1 EGTA投加量的影响液固比为5:1、振荡时间为2 h时EGTA投加量对土壤重金属洗脱率的影响见图 1。Cu、Zn、Pb和Cd洗脱率总体上随着EGTA投加量的增加而增加。ρ(EGTA)为0~0.5 g·L-1时,Cu和Cd洗脱率随着EGTA投加量的增加显著提高(P < 0.05),而Zn和Pb洗脱率增幅较小;随着EGTA投加量的增大,Cu、Zn和Pb洗脱率逐渐提高,而Cd洗脱率逐渐趋于平稳。ρ(EGTA)为2.0 g·L-1时Cu、Zn、Pb和Cd 4种重金属洗脱率分别为67.78%、32.89%、16.71%和61.40%。
|
图 1 EGTA投加量对土壤重金属洗脱率和浸出浓度的影响 Fig. 1 Effect of EGTA dosage on removal rate and leaching concentration of heavy metals in soil |
EGTA对土壤中Cu和Cd具有较高的洗脱能力,对Zn和Pb的洗脱率较低,其中,Pb洗脱率低于20%。这是因为Cu的稳定常数为18.4,高于其他重金属,当EGTA投加量较小时具有较大的竞争优势;Cd化学性质活泼,与Cu、Zn和Pb等其他重金属相比,其在土壤中的吸附能力最弱[28],进入土壤中的大部分Cd2+仍处于活性状态,与EGTA形成Cd-EGTA络合物,在土壤淋洗过程中很容易被去除。另外,供试土壤中Cd总含量为15.83 mg·kg-1,江苏省土壤中Cd背景值为0.085 mg·kg-1,供试土壤中Cd含量较高可能是其去除率较大的另一个原因;Zn去除率为32.89%,可能是因为土壤中Zn含量相对较低(江苏省土壤中Zn背景值为64.80 mg·kg-1)。Zn和Cd化学性质相似,在土壤淋洗过程中,两者可以相互竞争吸附位点[11],当EGTA投加量较低时,Zn在与Cd的竞争关系中处于劣势;Pb的稳定常数为12.7,低于Cu和Zn,因此对于螯合剂投加量的依赖性较大,当EGTA投加量较低时,Pb在与其他重金属间的竞争关系中处于劣势。此外,Pb在土壤中通常很稳定,较难洗脱[29]。
EGTA投加量对土壤重金属TCLP浸出浓度的影响见图 1。EGTA投加量增加可显著降低Zn和Cd的浸出浓度(P < 0.05),当EGTA投加量为2.0 g·L-1时,ρ(Zn)和ρ(Cd)分别从淋洗前的24.45和0.46 mg·L-1降低到12.78和0.12 mg·L-1,下降幅度分别为47.73%和73.91%;对Cu浸出浓度的降幅为20.87%;EGTA淋洗可提高土壤中Pb浸出浓度,这可能是因为Pb洗脱率较低,土壤中仍有较多的Pb,残留于土壤中的EGTA活化了残留Pb,使得Pb浸出浓度升高,生物有效性和环境风险也随之增加。
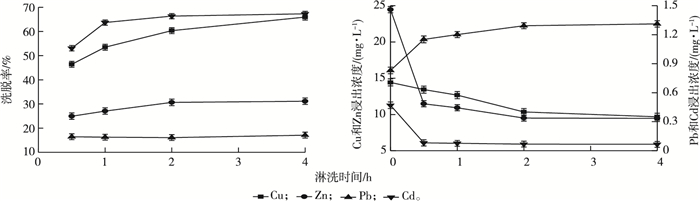
2.1.2 淋洗时间的影响当ρ(EGTA)为2.0 g·L-1,液固比为5:1时,淋洗时间对土壤重金属洗脱率的影响见图 2。反应2 h内,Cu、Zn和Cd淋洗效果较明显,之后趋于平稳。而Pb洗脱率在整个淋洗阶段基本稳定。这可能是因为Pb在反应初期就已经达到吸附解吸平衡,而Cu、Zn和Cd在2 h之后其解吸速度变缓,逐渐达到平衡,在螯合过程达到平衡后,反应时间增加对重金属洗脱率的影响不大[30]。
|
图 2 淋洗时间对土壤重金属洗脱率和浸出浓度的影响 Fig. 2 Effect of washing time on removal rate and leaching concentration of heavy metals in soil |
淋洗时间对土壤重金属TCLP浸出浓度的影响见图 2。反应2 h内,淋洗时间增加可显著降低Zn和Cd浸出浓度(P < 0.05),分别由淋洗前的24.45和0.47 mg·L-1降低到9.45和0.07 mg·L-1,下降幅度分别为61.35%和85.11%;淋洗时间对Cu浸出浓度的影响较小,与淋洗前相比,Cu浸出浓度下降幅度仅为28.29%;淋洗时间对Pb浸出浓度的影响较大,Pb浸出浓度随着淋洗时间的增加而增加,淋洗2 h后Pb浸出浓度趋于稳定,比淋洗前增加57.83%。
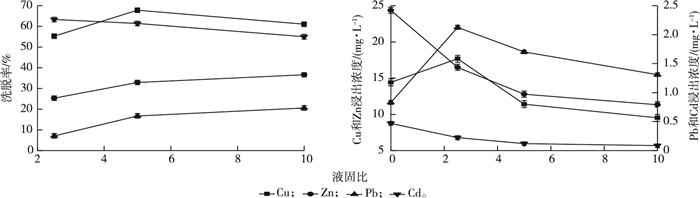
2.1.3 液固比的影响ρ(EGTA)为2.0 g·L-1条件下,振荡淋洗2 h后液固比对土壤重金属洗脱率和TCLP浸出浓度的影响见图 3。
|
图 3 液固比对土壤重金属洗脱率和浸出浓度的影响 Fig. 3 Effect of liquid-solid ratio on removal rate and leaching concentration of heavy metals in soil |
图 3显示,液固比增加可使Zn和Pb洗脱率分别从25.33%和7.07%提高到36.60%和20.59%;Cu洗脱率先增大后减小,Cd洗脱率呈下降趋势。提高液固比可显著降低Zn和Cd浸出浓度(P < 0.05),当液固比为10时,Zn和Cd浸出浓度分别由淋洗前的24.35和0.47 mg·L-1降低到淋洗后的11.32和0.08 mg·L-1,降低幅度分别为53.51%和82.98%;Cu和Pb浸出浓度随着液固比的增加呈先上升后下降趋势,可能是由于EGTA浓度恒定,液固比较低时,EGTA投加量较少,洗脱率较低,土壤中Cu和Pb残留量较高,容易被残留于土壤中的EGTA活化。当液固比较高时,EGTA投加量较大,对Cu和Pb洗脱率较高,使得土壤中Cu和Pb残留量较少,因而其浸出浓度较小。
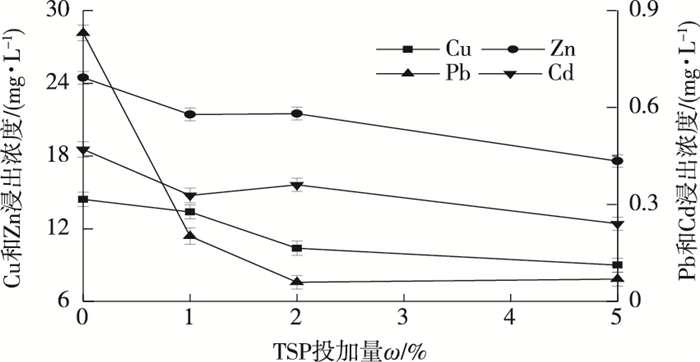
2.2 TSP对土壤重金属的钝化效果TSP投加量对土壤重金属浸出浓度的影响见图 4。图 4显示,TSP投加量增加显著降低Pb和Cd浸出浓度(P < 0.05),其中,TSP投加量为2%时,Pb浸出浓度由淋洗前的0.83 mg·L-1降低到0.07 mg·L-1,降幅达91.57%;Cu和Zn浸出浓度降幅相对较低,分别为37.59%和28.14%,这与CAO等[31]和BROWN等[32]的研究结果一致。
|
图 4 TSP投加量对土壤重金属浸出浓度的影响 Fig. 4 Effect of TSP dosage on leaching concentration of heavy metals in soil |
由于TSP对不同重金属钝化机制不同,因而钝化效果也不同。将TSP加入土壤后,其与Pb形成类似磷氯铅矿〔Pb5(PO4)3Cl〕的难溶物,从而降低Pb有效性[33],而对Cu、Zn和Cd等重金属的钝化可能是因为表面吸附和络合作用[31],TSP加入增加了土壤表面负电荷,增强其对Cd、Zn和Cu等重金属离子的吸附,从而降低其浸出浓度,提高稳定性。
2.3 EGTA/TSP联合处理的响应面分析与优化采用Design-Expert 8.0软件的Box-Behnken响应面分析进行实验设计,共得到17个处理,经计算得到Cu、Zn、Pb和Cd残留量,对淋洗土壤做钝化处理后进行TCLP浸提实验,得到Cu、Zn、Pb和Cd的TCLP浸出浓度,不同处理各重金属残留量和TCLP浸出浓度见表 4。
|
|
表 4 不同处理各重金属残留量和TCLP浸出浓度 Table 4 Heavy metal residues and TCLP leaching concentration in different treatments |
采用各重金属的环境风险削减率和总环境风险削减率(β)2个指标反映修复效果,将表 4中的数据代入式(1)~(4),计算得到Cu、Zn、Pb和Cd的环境风险削减率和总环境风险削减率(表 5)。
|
|
表 5 不同处理条件下重金属环境风险削减率 Table 5 Reduction rate of heavy metal environmental risk under different treatment conditions |
采用Design-Expert 8.0的二次多项式和逐步回归法拟合各重金属环境风险削减率和总环境风险削减率与修复条件之间的关系,其二次多项式模型及方差分析结果见表 6。模型方差分析结果显示,各模型F值较大,P值均小于0.01,模型达极显著水平,失拟项P>0.05,失拟项未达显著水平,说明回归模型能很好地拟合实验结果。R2均在0.90以上,表明该模型可信度高,可用于实际预测。
|
|
表 6 模型回归方程及方差分析 Table 6 Model regression equation and analysis of variance |
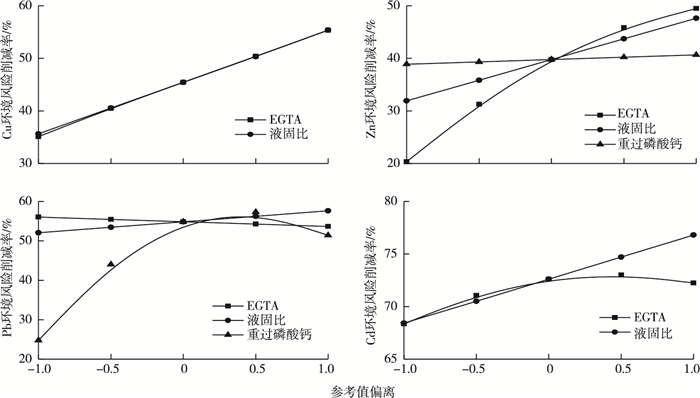
Cu、Zn和Cd的环境风险削减率主要受EGTA投加量和液固比的影响,液固比和EGTA投加量的增加均能提高3者的环境风险削减率(图 5)。一方面,这是因为EGTA对土壤中Cu和Cd的洗脱率较高,另一方面,EGTA淋洗能显著降低Zn和Cd浸出浓度;因此单独淋洗就可以大幅度降低Cu、Zn和Cd的环境风险。
|
横坐标中-1和1分别表示最小值和最大值,-0.5和0.5分别表示最小值与中值的均值以及最大值与中值的均值。 图 5 各重金属环境风险削减率与修复条件的关系 Fig. 5 The relationship between environmental risk reduction rate and various factors |
Pb环境风险削减率主要受TSP投加量的影响,随着TSP投加量的增加,Pb环境风险削减率显著提高,但过高的TSP投加量对其具有抑制作用(图 5)。这是因为TSP投加量在0~2%之间时,TSP投加量增加可显著降低土壤中Pb浸出浓度,当TSP投加量超过2%时,其对Pb浸出浓度的影响很小。
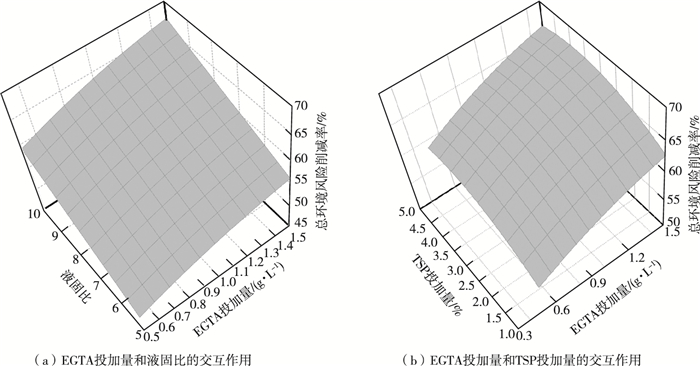
2.3.2 因素互作响应面分析TSP投加量取中值(3%)时,EGTA投加量和液固比的交互作用对重金属总环境风险削减率(β)的影响见图 6(a)。图 6(a)显示,β随着EGTA投加量和液固比的增加而增加,两者呈现较好的协同作用。液固比取中值(7.5)时,EGTA投加量和TSP投加量的交互作用对β的影响见图 6(b)。当TSP投加量一定时,随着EGTA投加量的增加,β先增大后趋于平稳。当EGTA投加量一定时,随着TSP投加量的增加,β先增大后趋于稳定;当EGTA投加量为1.1~1.5 g·L-1时,β高于61%。总体上,增加EGTA投加量对β的影响幅度更大。
|
图 6 因素互作对重金属总环境风险削减率的影响 Fig. 6 Effect of the interaction of factors on the total environmental risk reduction rate |
以总环境风险削减率为响应值,采用Design-Expert 8.0软件在实验因素水平范围内预测的最优处理条件:EGTA投加量为1.0 g·L-1,液固比为10,TSP投加量w为2%。在该条件下,总环境风险削减率模拟值达到最大,为62.80%,其中,Cu、Zn、Pb和Cd环境风险削减率模拟值分别为52.72%、41.06%、44.70%和77.24%。
为了验证上述拟合结果的可靠性,进行3组平行实验,得到土壤中Cu、Zn、Pb和Cd的环境风险削减率分别为50.28%、42.71%、46.74%和79.16%,总环境风险削减率为63.08%,Cu、Zn、Pb和Cd环境风险削减率与预测值的偏差分别为4.63%、4.02%、4.56%和2.49%,偏差较小,表明模型方程具有较高的拟合精度。
3 结论(1) EGTA对土壤中Cu和Cd具有较高的洗脱能力,洗脱率均在60%以上,对Zn和Pb的洗脱率较低,其中Pb洗脱率低于20%。
(2) EGTA淋洗可显著降低土壤中Zn和Cd浸出浓度(P < 0.05),对Cu浸出浓度的影响较小,但可提高Pb浸出浓度。TSP钝化可降低土壤中Cu、Zn、Pb和Cd浸出浓度,其中Pb浸出浓度降幅在90%以上。
(3) 采用涵盖土壤重金属含量、浸出浓度和毒性的土壤重金属环境风险评价方法,能较好地反映土壤重金属富集程度和二次污染风险,可以对不同类型重金属污染土壤修复效果进行综合评价。
(4) 总环境风险削减率与EGTA投加量、液固比和TSP投加量呈显著的二次方关系,提高EGTA投加量和液固比可以大幅度降低Cu、Zn和Cd的环境风险,TSP钝化处理对Pb环境风险的削减作用较好。
| [1] |
苏彬彬, 崔红标, 樊恒亮, 等. 改良剂对铜镉污染土壤的修复效果及健康风险评估[J]. 生态与农村环境学报, 2017, 33(5): 446-452. [ SU Bin-bin, CUI Hong-biao, FAN Heng-liang, et al. Long-Term Remediate Effect of Three Amendments on Polluted Soil Near Guixi Smelter and Health Risk Assessment[J]. Journal of Ecology and Rural Environment, 2017, 33(5): 446-452.] (  0) 0) |
| [2] |
JINGZI B Y, LI J S, TSANG D C W, et al. Fate of Arsenic Before and After Chemical-Enhanced Washing of an Arsenic-Containing Soil in Hong Kong[J]. Science of the Total Environment, 2017, 599/600: 679-688. DOI:10.1016/j.scitotenv.2017.04.208 (  0) 0) |
| [3] |
陆素芬, 宋波, 伏凤艳, 等. 南丹矿业活动影响区蔬菜重金属含量及健康风险[J]. 生态与农村环境学报, 2016, 32(3): 478-485. [ LU Su-fen, SONG Bo, FU Feng-yan, et al. Heavy Metal Content in Vegetable and Its Health Risk as Affected by Mining Activities in Nandan County[J]. Journal of Ecology and Rural Environment, 2016, 32(3): 478-485.] (  0) 0) |
| [4] |
BOLAN N, KUNHIKRISHNAN A, THANGARAJAN R, et al. Remediation of Heavy Metal(Loid)s Contaminated Soils:To Mobilize or to Immobilize?[J]. Journal of Hazardous Materials, 2014, 266: 141-166. DOI:10.1016/j.jhazmat.2013.12.018 (  0) 0) |
| [5] |
JIANG J P, WU L H, LI N, et al. Effects of Multiple Heavy Metal Contamination and Repeated Phytoextraction by Sedum plumbizincicola on Soil Microbial Properties[J]. European Journal of Soil Biology, 2010, 46(1): 18-26. DOI:10.1016/j.ejsobi.2009.10.001 (  0) 0) |
| [6] |
DERMONT G, BERGERON M, MERCIER G, et al. Soil Washing for Metal Removal:A Review of Physical/Chemical Technologies and Field Applications[J]. Journal of Hazardous Materials, 2008, 152(1): 1-31. DOI:10.1016/j.jhazmat.2007.10.043 (  0) 0) |
| [7] |
WEI M, CHEN J J, WANG X W. Removal of Arsenic and Cadmium With Sequential Soil Washing Techniques Using Na2-EDTA, Oxalic and Phosphoric Acid:Optimization Conditions, Removal Effectiveness and Ecological Risks[J]. Chemosphere, 2016, 156: 252-261. DOI:10.1016/j.chemosphere.2016.04.106 (  0) 0) |
| [8] |
BEIYUAN J Z, TSANG D C W, VALIX M, et al. Combined Application of EDDS and EDTA for Removal of Potentially Toxic Elements Under Multiple Soil Washing Schemes[J]. Chemosphere, 2018, 205: 178-187. DOI:10.1016/j.chemosphere.2018.04.081 (  0) 0) |
| [9] |
祝振球, 周静, 徐磊, 等. 不同重金属钝化材料对土壤胶体的影响[J]. 生态与农村环境学报, 2017, 33(2): 188-192. [ ZHU Zhen-qiu, ZHOU Jing, XU Lei, et al. Effects of Different Heavy Metal Amendments on Soil Colloid[J]. Journal of Ecology and Rural Environment, 2017, 33(2): 188-192.] (  0) 0) |
| [10] |
HOU D Y, AL-TABBAA A, GUTHRIE P, et al. Using a Hybrid LCA Method to Evaluate the Sustainability of Sediment Remediation at the London Olympic Park[J]. Journal of Cleaner Production, 2014, 83: 87-95. DOI:10.1016/j.jclepro.2014.07.062 (  0) 0) |
| [11] |
ZHAI X Q, LI Z W, HUANG B, et al. Remediation of Multiple Heavy Metal-Contaminated Soil Through the Combination of Soil Washing and in Situ Immobilization[J]. The Science of the Total Environment, 2018, 635: 92-99. DOI:10.1016/j.scitotenv.2018.04.119 (  0) 0) |
| [12] |
尹雪, 陈家军, 吕策. 螯合剂复配对实际重金属污染土壤洗脱效率影响及形态变化特征[J]. 环境科学, 2014, 35(2): 733-739. [ YIN Xue, CHEN Jia-jun, LV Ce. Impact of Compounded Chelants on Removal of Heavy Metals and Characteristics of Morphologic Change in Soil From Heavy Metals Contaminated Sites[J]. Environmental Science, 2014, 35(2): 733-739.] (  0) 0) |
| [13] |
GUO X F, WEI Z B, WU Q T, et al. Effect of Soil Washing With Only Chelators or Combining With Ferric Chloride on Soil Heavy Metal Removal and Phytoavailability:Field Experiments[J]. Chemosphere, 2016, 147: 412-419. DOI:10.1016/j.chemosphere.2015.12.087 (  0) 0) |
| [14] |
冯静, 张增强, 李念, 等. 铅锌厂重金属污染土壤的螯合剂淋洗修复及其应用[J]. 环境工程学报, 2015, 9(11): 5617-5625. [ FENG Jing, ZHANG Zeng-qiang, LI Nian, et al. Washing of Heavy Metal Contaminated Soil Around a Lead-Zinc Smelter by Several Chelating Agents and the Leached Soil Utilization[J]. Chinese Journal of Environmental Engineering, 2015, 9(11): 5617-5625. DOI:10.12030/j.cjee.20151177] (  0) 0) |
| [15] |
陈亚慧, 李君, 王明新, 等. EGTA和酒石酸对蓖麻Cd胁迫与积累的调控作用[J]. 西北植物学报, 2014, 34(5): 1025-1031. [ CHEN Ya-hui, LI Jun, WANG Ming-xin, et al. Regulation of EGTA and Tartaric Acid on Cd Stress and Accumulation in Ricinus communis L.[J]. Acta Botanica Boreali-Occidentalia Sinica, 2014, 34(5): 1025-1031.] (  0) 0) |
| [16] |
WANG G Y, ZHANG S R, XU X X, et al. Heavy Metal Removal by GLDA Washing:Optimization, Redistribution, Recycling, and Changes in Soil Fertility[J]. Science of the Total Environment, 2016, 569/570: 557-568. DOI:10.1016/j.scitotenv.2016.06.155 (  0) 0) |
| [17] |
UDOVIC M, LESTAN D. Pb, Zn and Cd Mobility, Availability and Fractionation in Aged Soil Remediated by EDTA Leaching[J]. Chemosphere, 2009, 74(10): 1367-1373. DOI:10.1016/j.chemosphere.2008.11.013 (  0) 0) |
| [18] |
TSANG D C W, OLDS W E, WEBER P. Residual Leachability of CCA-Contaminated Soil After Treatment With Biodegradable Chelating Agents and Lignite-Derived Humic Substances[J]. Journal of Soils and Sediments, 2013, 13(5): 895-905. DOI:10.1007/s11368-013-0662-x (  0) 0) |
| [19] |
IM J, YANG K, JHO E H, et al. Effect of Different Soil Washing Solutions on Bioavailability of Residual Arsenic in Soils and Soil Properties[J]. Chemosphere, 2015, 138: 253-258. DOI:10.1016/j.chemosphere.2015.06.004 (  0) 0) |
| [20] |
PARK J H, BOLAN N S, CHUNG J W, et al. Environmental Monitoring of the Role of Phosphate Compounds in Enhancing Immobilization and Reducing Bioavailability of Lead in Contaminated Soils[J]. Journal of Environmental Monitoring, 2011, 13(8): 2234-2242. DOI:10.1039/c1em10275c (  0) 0) |
| [21] |
祝振球, 周静, 徐磊, 等. 模拟酸雨对微米和纳米羟基磷灰石稳定化污染土壤的铜和镉淋溶效应[J]. 生态与农村环境学报, 2017, 33(3): 265-269. [ ZHU Zhen-qiu, ZHOU Jing, XU Lei, et al. Release of Cu and Cd From Contaminated Soil Amended by Nanoparticle and Microparticle Hydroxyapatite in the Condition of Acid Deposition[J]. Journal of Ecology and Rural Environment, 2017, 33(3): 265-269.] (  0) 0) |
| [22] |
荀志祥, 王世泽, 王明新, 等. 超声强化EDDS/EGTA淋洗修复重金属污染土壤[J]. 环境工程学报, 2018, 12(6): 1766-1774. [ XUN Zhi-xiang, WANG Shi-ze, WANG Ming-xin, et al. Remediation of Heavy Metal Contaminated Soil by Ultrasound-Enhanced Washing With EDDS and EGTA[J]. Chinese Journal of Environmental Engineering, 2018, 12(6): 1766-1774.] (  0) 0) |
| [23] |
张春雷, 费小通, 李婷, 等. 利用超声波辅助去除污染土壤中重金属的研究[J]. 环境科学与技术, 2014, 37(增刊1): 121-124. [ ZHANG Chun-lei, FEI Xiao-tong, LI Ting, et al. Ultrasound Assisted Removal of Heavy Metals From Contaminated Soil[J]. Environmental Science & Technology, 2014, 37(Suppl. 1): 121-124.] (  0) 0) |
| [24] |
LIANG Y, CAO X D, ZHAO L, et al. Biochar- and Phosphate-Induced Immobilization of Heavy Metals in Contaminated Soil and Water:Implication on Simultaneous Remediation of Contaminated Soil and Groundwater[J]. Environmental Science and Pollution Research, 2014, 21(6): 4665-4674. DOI:10.1007/s11356-013-2423-1 (  0) 0) |
| [25] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000: 205-214.
(  0) 0) |
| [26] |
中国环境监测总站. 中国土壤元素背景值[M]. 北京: 中国环境科学出版社, 1990: 93-493.
(  0) 0) |
| [27] |
GB/T 14848—2017, 地下水质量标准[S]. [GB/T 14848-2017, Standard for Groundwater Quality[S].]
(  0) 0) |
| [28] |
SHAHEEN S M, TSADILAS C D, RINKLEBE J. A Review of the Distribution Coefficients of Trace Elements in Soils:Influence of Sorption System, Element Characteristics, and Soil Colloidal Properties[J]. Advances in Colloid and Interface Science, 2013, 201/202: 43-56. DOI:10.1016/j.cis.2013.10.005 (  0) 0) |
| [29] |
LABANOWSKI J, MONNA F, BERMOND A, et al. Kinetic Extractions to Assess Mobilization of Zn, Pb, Cu, and Cd in a Metal-Contaminated Soil:EDTA vs.Citrate[J]. Environmental Pollution, 2008, 152(3): 693-701. DOI:10.1016/j.envpol.2007.06.054 (  0) 0) |
| [30] |
WU Q, CUI Y R, LI Q L, et al. Effective Removal of Heavy Metals From Industrial Sludge With the Aid of a Biodegradable Chelating Ligand GLDA[J]. Journal of Hazardous Materials, 2015, 283: 748-754. DOI:10.1016/j.jhazmat.2014.10.027 (  0) 0) |
| [31] |
CAO X D, MA L Q, RHUE D R, et al. Mechanisms of Lead, Copper, and Zinc Retention by Phosphate Rock[J]. Environmental Pollution, 2004, 131(3): 435-444. DOI:10.1016/j.envpol.2004.03.003 (  0) 0) |
| [32] |
BROWN S, CHRISTENSEN B, LOMBI E, et al. An Inter-Laboratory Study to Test the Ability of Amendments to Reduce the Availability of Cd, Pb, and Zn in Situ[J]. Environmental Pollution, 2005, 138(1): 34-45. DOI:10.1016/j.envpol.2005.02.020 (  0) 0) |
| [33] |
MIRETZKY P, FERNANDEZ-CIRELLI A. Phosphates for Pb Immobilization in Soils:A Review[J]. Environmental Chemistry Letters, 2008, 6(3): 121-133. (  0) 0) |




