铬(Cr)是倍受关注的环境污染物之一,通常以Cr6+或Cr3+形式存在于冶金、电镀、制革等行业排放的废水中。其中Cr6+毒性是Cr3+的100倍,被列为对人体危害最大的八大化学物质之一[1-3]。我国GB 8979—1996《污水综合排放标准》要求排放废水中ρ(Cr6+)不得超过0.5 mg·L-1。因此,控制废水中Cr6+排放浓度至关重要。目前,含Cr6+废水处理方法主要有生物法[4]、化学还原法[5-6]和物理吸附法[7-8]等,其中物理吸附法对于低浓度含Cr6+废水具有操作简单、成本低、去除效率高等优点。
近年来,以农林、生活废弃物为原料,酸、碱或金属离子为活化剂制备生物质炭类吸附剂引起了研究者的兴趣[9-11]。生物质炭具有较大的比表面积、发达的孔隙结构和丰富的表面官能团,对水体中的金属离子有较好的吸附能力[12-14],且生物质炭原料易得,制备简单,有望作为一种廉价的吸附剂应用于实际废水治理。目前国内外在该领域的研究多集中在生物质炭的制备、吸附条件的优化以及吸附过程的热力学和动力学研究上[13, 15-16],对吸附机理的研究相对较少。因此系统考察生物质炭对Cr6+的吸附性能及吸附机制十分必要。
中国是龙虾养殖和食用大国,每年产生的龙虾壳质量高达1万t以上,这些虾壳常被当作废弃物,给生态环境造成了极大的危害。实际上,龙虾壳中含有大量的有用化学物质,其中约30%~35%为甲壳素,25%~30%为蛋白质,40%为碳酸钙及少量脂类物质。目前虾壳的利用大多限于甲壳素的提取,要减少龙虾壳的丢弃,必须寻求新的资源化途径。该研究以龙虾壳为原料,KOH为活化剂制备生物质炭,并将其应用于低浓度含铬废水的处理,考察了溶液pH值、Cr6+初始浓度、生物质炭用量及温度对吸附容量的影响,利用Zeta电位、红外光谱(FT-IR)、X-射线光电子能谱(XPS),原子吸收光谱仪等手段研究虾壳生物质炭吸附Cr6+的作用机制。
1 材料与方法 1.1 仪器与试剂仪器:OTF-1200X型管式炉(合肥科晶材料技术有限公司);380型红外光谱仪(美国尼高力仪器公司),扫描范围为400~4 000 cm-1;Zetasizer Nano ZSP系列Zeta电位仪(英国马尔文仪器有限公司);TU-1900型紫外可见分光光度计(北京普析通用);A3F-13型原子吸收光谱仪(北京普析通用);Kratos-ultra DLD型X射线光电子能谱仪(日本岛津公司);ZNCL-BS型磁力搅拌器(科华仪器设备有限公司);BSA224S型电子天平(北京赛多利斯仪器系统有限公司);Sartorius PB-10 pH计(北京赛多利斯仪器系统有限公司)。
试剂:重铬酸钾,优级纯;氢氧化钾、氢氧化钠、盐酸、硫酸、丙酮、二苯基碳酰二肼、氯化铵,均为分析纯。
1.2 虾壳生物质炭的制备将一定量预处理的虾壳(来源于湖北孝感水产市场的小龙虾)置于石墨盒并加入一定量的KOH,在氮气气氛下于管式炉中以5 ℃·min-1升温至700 ℃,保温2 h,冷却后用蒸馏水洗至中性,抽滤,80 ℃条件下干燥24 h,制得虾壳生物质炭。
1.3 吸附实验采用优级纯重铬酸钾配制实验所用含Cr6+模拟废水,溶液初始pH值通过1 mol·L-1 NaOH或1 mol·L-1 H2SO4溶液调节。向溶液中投加待用的虾壳生物质炭,设置不同的Cr6+溶液初始浓度、虾壳生物质炭用量和吸附温度,吸附量计算方法为
| $ {q_{\rm{e}}} = \frac{{({C_0} - {C_t})V}}{W} 。$ | (1) |
式(1)中,qe为吸附量,mg·g-1;C0和Ct分别为溶液中Cr6+的初始质量浓度和t时刻的质量浓度,mg·L-1;V为溶液体积,L;W为吸附剂用量,g。
1.4 检测方法溶液中Cr6+和总Cr浓度分别采用二苯基碳酰二肼分光光度法[17]和火焰原子吸收法[18]测定。利用Malvern-Zetasizer Nano型Zeta电位仪测定不同pH值条件下生物质炭表面Zeta电位。采用KBr压片法制样,用Nicolet-380型傅里叶变换红外光谱仪对样品表面官能团进行分析。样品表面元素形态用Thermol-Escalab 250Xi型X射线光电子能谱仪(XPS)进行表征。
1.5 动力学模型吸附动力学主要是用来表述Cr6+在虾壳生物质炭表面的吸附速率。准一级动力学模型的线性与非线性拟合方程如式(2)~(3)所示,准二级动力学模型的线性与非线性拟合方程如式(4)~(5)所示。
| $ \lg ({q_{\rm{e}}} - {q_t}) = \lg {q_{\rm{e}}} - \frac{{{k_1}}}{{2.303}}t, $ | (2) |
| $ {q_t} = {q_{\rm{e}}}(1 - {k_1}t), $ | (3) |
| $ \frac{t}{{{q_t}}} = \frac{1}{{{k_2}{q_{\rm{e}}}^2}} + \frac{t}{{{q_{\rm{e}}}}}, $ | (4) |
| $ {q_t} = \frac{{{k_2}{q_{\rm{e}}}^2t}}{{1 + {k_2}{q_{\rm{e}}}t}} 。$ | (5) |
式(2)~(5)中,k1为准一级动力学反应速率常数,min-1;k2为准二级动力学反应速率常数,g·mg-1·min-1;qt为t时刻虾壳生物质炭对Cr6+的吸附量,mg·g-1;qe为平衡吸附量,mg·g-1。
1.6 吸附等温模型吸附等温曲线是研究固体吸附剂与吸附质之间相互作用以及吸附剂吸附能力的重要依据,常用Langmuir和Freundlich方程进行拟合。
| $ \frac{{{C_{\rm{e}}}}}{{{Q_{\rm{e}}}}} = \frac{1}{{{K_{\rm{L}}}{Q_{{\rm{max}}}}}} + \frac{{{C_{\rm{e}}}}}{{{Q_{{\rm{max}}}}}}, $ | (6) |
| $ \ln {q_{\rm{e}}} = \ln {K_{\rm{F}}} + \frac{1}{n}\ln {C_{\rm{e}}} 。$ | (7) |
式(6)~(7)中,Ce为达到吸附平衡时溶液中剩余Cr6+质量浓度,mg·L-1;qe为平衡吸附量,mg·g-1;Qmax为理论饱和吸附量,mg·g-1;KL为Langmuir常数,L·mg-1;KF为Freundlich常数,L·mg-1。
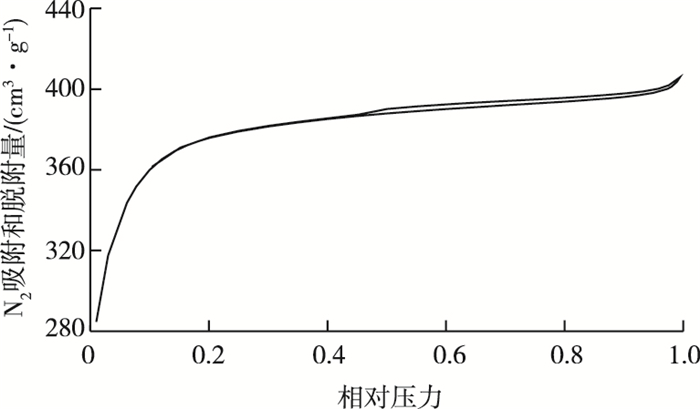
2 结果与讨论 2.1 虾壳生物质炭的表征 2.1.1 比表面积、孔容和孔径分析制备的虾壳生物质炭的比表面积高达1 123.59 m2·g-1,孔容为0.11 cm3·g-1,平均孔径为2.22 nm。较大的比表面积有利于虾壳生物质炭对Cr6+的吸附。如图 1所示,虾壳生物质炭的N2吸附脱附等温线属于典型H4型滞后环,表明虾壳生物质炭具有窄的狭缝状孔,也可能存在嵌入式大孔。
|
图 1 虾壳生物质炭的吸附脱附等温线 Fig. 1 N2 adsorption and desorption isotherms curves of shrimp shell-derived biochar |
对虾壳生物质炭进行元素分析,结果显示虾壳生物质炭中w(C)为60.44%,w(H)、w(N)和w(O)分别为3.04%、3.06%和22.10%,(N+O)/C比值为0.42,相对于大多植物系生物质炭,虾壳生物质炭(N+O)/C比值较大,O含量有利于形成丰富的官能团,促进生物质炭对Cr6+的吸收。
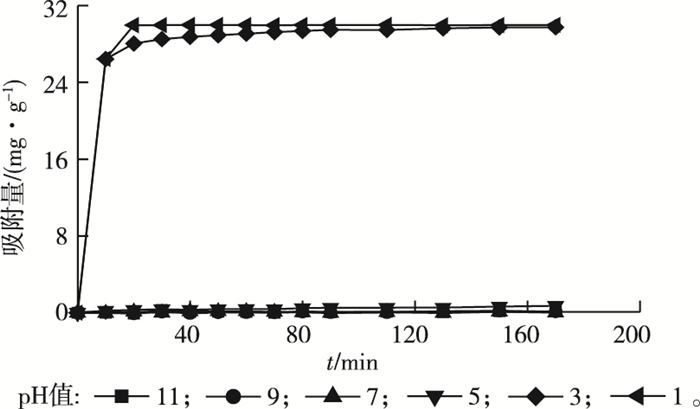
2.2 Cr6+吸附影响因素 2.2.1 pH值对吸附效果的影响虾壳生物质炭对不同初始pH值溶液中Cr6+的吸附量随时间变化情况如图 2所示。pH值在5.0及以上时生物质炭对Cr6+几乎没有吸附,而随着pH值降低虾壳生物质炭对Cr6+的平衡吸附量增大。当pH值降低至3.0时,1 g·L-1生物质炭对30 mg·L-1的Cr6+吸附量可达29.14 mg·g-1。进一步降低溶液pH值至1.0,达到吸附平衡所需时间缩短,但平衡吸附量增加不明显。研究表明,Cr6+在水溶液中有3种存在形式,分别是Cr2O72-、HCrO4-和Cr2O42-,3者间存在解离平衡[19]。因此当溶液pH值为1~3时,Cr6+主要以Cr2O72-形式存在,在pH值>3~6及>6的溶液中,Cr6+的存在形式分别以HCrO4-和CrO42-为主[19-22]。在相同的静电引力下,吸附剂对Cr2O72-具有更高的吸附效率[22]。pH值不仅影响Cr6+在溶液中的存在形态,也能改变吸附剂表面官能团的特性。由于Cr6+在溶液中均以阴离子形式存在,吸附剂表面正电荷位点越多,越有利于Cr6+在其表面的吸附[23]。虾壳中所含丰富的C、N、O元素在炭化过程中可能形成—OH、—COOH以及—NH2等基团,其中—OH和—NH2官能团在酸性条件下会质子化形成—OH2+和—NH3+,从而有利于生物质炭对Cr2O72-的吸附[24-25]。而随着pH值增大,虾壳生物质炭表面的质子化吸附位点减少,同时—COOH会逐渐失去质子变成—COO-,生物质炭表面的负电荷增加,不利于其对HCrO4-和CrO42-的吸附。因此当溶液的pH值较大时,虾壳生物质炭对Cr6+基本不吸附。考虑到pH值为1.0时溶液酸度过大,因此后续实验设定溶液初始pH值为3.0。
|
图 2 pH值对虾壳生物质炭吸附Cr6+的影响 Fig. 2 The effect of pH on the adsorption of Cr6+ by shrimp shell-derived biochar |
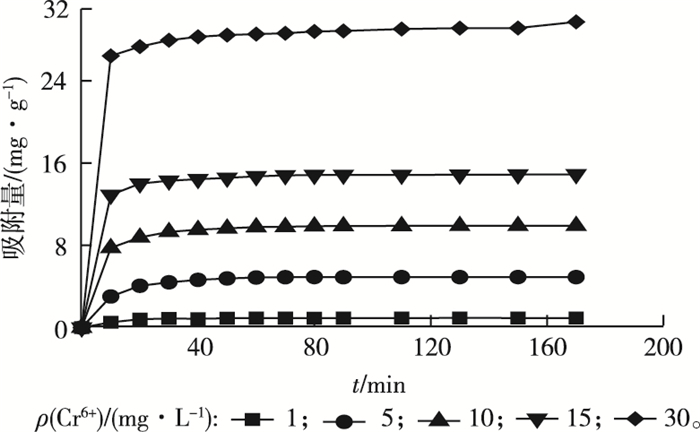
图 3为Cr6+初始浓度对Cr6+吸附量的影响。当溶液初始pH=3,虾壳生物质炭用量为1 g·L-1,溶液初始ρ(Cr6+)分别为1、5、10、15和30 mg·L-1时,平衡吸附量分别为0.93、4.91、9.91、14.91、29.73 mg·g-1。可以看出,在初始ρ(Cr6+)为1~30 mg·L-1时虾壳生物质炭对Cr6+的去除率达90%以上,平衡吸附量随着溶液初始ρ(Cr6+)增加而增加相应的倍数,水中剩余ρ(Cr6+)均低于0.5 mg·L-1,达到GB 8978—1996《污水综合排放标准》中Cr6+的排放要求。此外,虾壳生物质炭对Cr6+的吸附较快,前20 min的吸附量即可达到平衡状态的80%以上。吸附速率是衡量吸附剂性能好坏的重要因素之一,在实际应用中,通常选择吸附速度快、平衡时间短的吸附剂。因此利用虾壳生物质炭去除废水中的Cr6+既可达到排放要求,同时也满足动力学要求。
|
图 3 初始ρ(Cr6+)对虾壳生物质炭吸附Cr6+的影响 Fig. 3 The effect of Cr6+concentration on the adsorption of Cr6+ by shrimp shell-derived biochar |
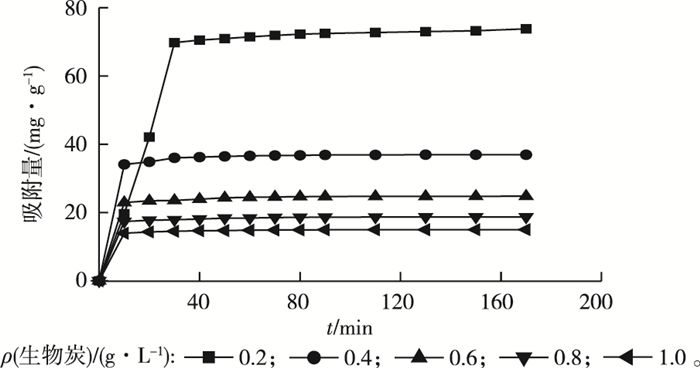
改变虾壳生物质炭用量,溶液中Cr6+吸附量随时间的变化情况如图 4所示。当溶液初始pH=3,溶液初始ρ(Cr6+)为15 mg·L-1时,虾壳生物质炭用量由0.2 g·L-1增大至1.0 g·L-1时达到吸附平衡所需时间缩短,但虾壳生物质炭对Cr6+的吸附量却逐渐减小,吸附量从73.83减小到14.99 mg·g-1。
|
图 4 虾壳生物质炭用量对虾壳生物质炭吸附Cr6+的影响 Fig. 4 The effect of dosage on the adsorption of Cr6+ by shrimp shell-derived biochar |
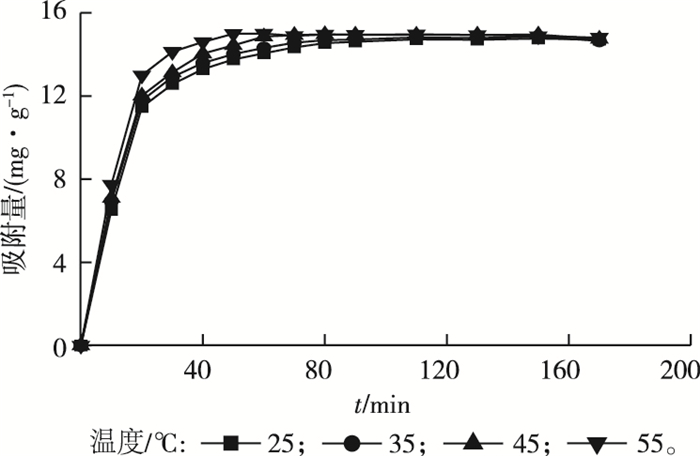
图 5是不同温度下虾壳生物质炭吸附溶液中Cr6+的吸附量随时间的变化情况。如图 5所示,当溶液初始pH=3,虾壳生物质炭用量为1 g·L-1,溶液初始ρ(Cr6+)为15 mg·L-1时,温度对平衡吸附量的影响并不明显。
|
图 5 温度对虾壳生物质炭吸附Cr6+的影响 Fig. 5 The effect of temperature on the adsorption of Cr6+ by shrimp shell-derived biochar |
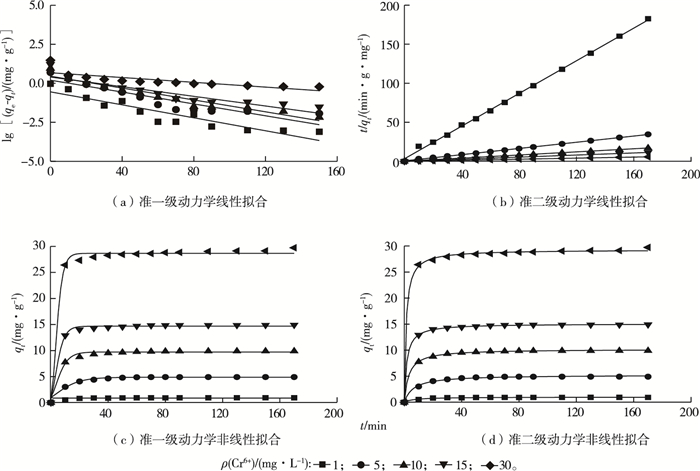
进一步采用准一级吸附动力学和准二级吸附动力学模型对虾壳生物质炭吸附Cr6+进行动力学拟合。根据不同Cr6+初始浓度下的实验数据拟合所得曲线如图 6所示,模型参数见表 1。由表 1可知,准一级动力学的线性拟合和非线性拟合相关系数均低于准二级动力学方程拟合得到的相关系数,且准一级动力学模型只适合描述吸附的初始阶段,准二级吸附动力学模型能够很好地描述吸附全过程,故认为准二级动力学方程能更好的描述Cr6+在虾壳生物质炭上的吸附动力学,表明虾壳生物质炭吸附Cr6+的过程主要以化学吸附为主[26]。进一步比较准二级动力学的线性拟合和非线性拟合数据可知,线性拟合的相关系数略大于非线性拟合,2种拟合的平衡吸附量都很接近于实验平衡吸附量,但两者拟合得到的吸附速率常数k2存在一定差别。
|
图 6 虾壳生物质炭对Cr6+准一级、准二级动力学线性拟合与准一级、准二级动力学非线性拟合 Fig. 6 Linear form of pseudo-first order, pseudo-second order kinetic models and non-linear form of pseudo-first order, pseudo-second order kinetic models for Cr6+ adsorption on the shrimp shell-derived biochar |
|
|
表 1 Cr6+的吸附动力学线性拟合参数 Table 1 Parameters of linear forms for pseudo-first and pseudo-second adsorption kinetic models |
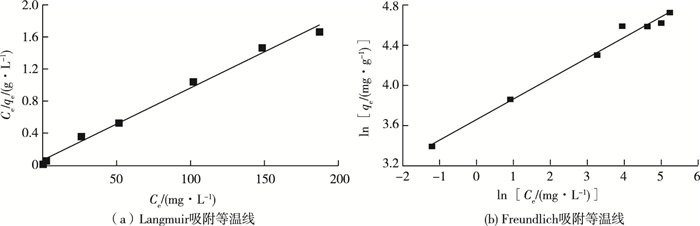
采用Langmuir和Freundlich方程拟合了25 ℃时虾壳生物质炭吸附Cr6+的平衡数据(图 7)。Cr6+在虾壳生物质炭上的吸附行为与Langmuir和Freundlich吸附等温模型均较为相符,拟合R2值分别为0.990和0.983。Langmuir和Freundlich常数分别为0.145和38.8 L·mg-1。通过Langmuir模型计算所得的理论最大吸附量为111.0 mg·g-1。Freundlich模型中n为4.90,n值反映了吸附反应强度,n值越大,吸附性能越好。一般认为n值在2~10之间易于吸附,< 0.5难以吸附。由此可见Cr6+易于吸附在虾壳生物质炭表面。
|
图 7 Cr6+在虾壳生物质炭上的Langmuir和Freundlich吸附等温线 Fig. 7 Langmuir and Freundlich adsorption isotherm curves for C6+ adsorption on the shrimp shell-derived biochar |
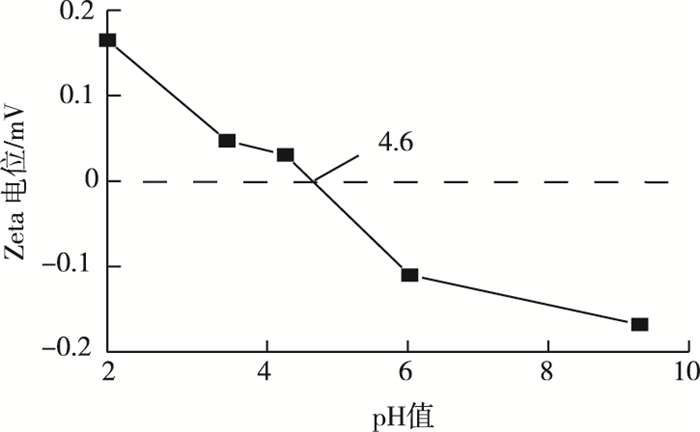
不同pH值下虾壳生物质炭的Zeta电位结果如图 8所示,虾壳生物质炭的等电点为4.6,说明在pH < 4.6的溶液中虾壳生物质炭表面带正电荷,而在pH>4.6的溶液中虾壳生物质炭表面带负电荷。对比图 8和图 2可知,Zeta电位的变化趋势与不同pH值条件下Cr6+在虾壳生物质炭表面的吸附行为一致,即在溶液pH值小于等电点时,虾壳生物质炭对Cr6+有较好的吸附能力,而当溶液pH值大于等电点时,虾壳生物质炭不能吸附Cr6+。李克斌等[20]研究也发现,当溶液pH值低于荞麦皮的等电点4.1时,荞麦皮能通过静电引力吸附铬酸根阴离子,当pH值过高时,荞麦皮表面带负电,静电斥力将不利于铬酸根阴离子的吸附。由以上实验结果可以推测Cr6+主要是通过静电引力吸附到虾壳生物质炭表面,在pH值为3和1时,生物质炭表面的正电荷有利于吸附Cr2O72-和HCrO4-阴离子,而在pH≥5时,生物质炭表面的负电荷与HCrO4-和CrO42-阴离子存在静电排斥力,不利于其对Cr6+的吸附。
|
图 8 虾壳生物质炭的Zeta电位图 Fig. 8 Zeta potential of the shrimp shell-derived biochar |
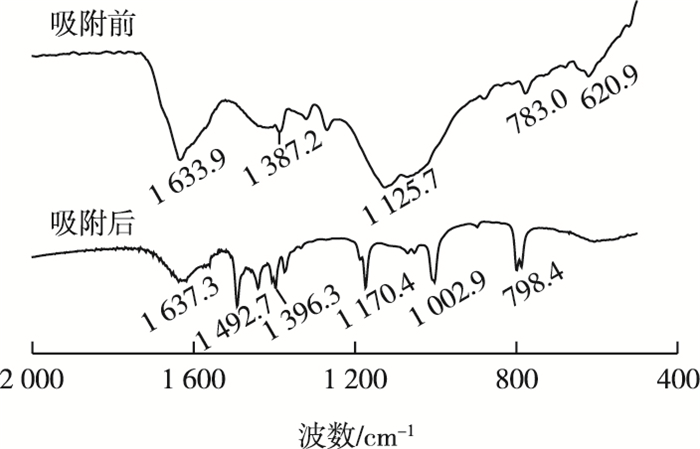
同一种物质在吸附剂上进行的可能是物理吸附,也可能是化学吸附,更多的是2种吸附同时发生。当存在化学吸附时,通常伴随着官能团的变化。例如GARG等[27]利用红外光谱对吸附Cr6+前后的生物质炭进行表征发现,吸附Cr6+后的生物质炭不仅会在609 cm-1处出现新的振动峰,且1 058 cm-1处的C—O官能团吸收峰移至1 047 cm-1,表明该官能团与Cr6+之间存在相互作用。HUANG等[28]通过原位红外光谱研究发现Cr6+吸附在Fe2O3不同晶面上的红外图谱会因为配位方式的不同而不同。为研究Cr6+与虾壳生物质炭表面官能团的作用机制,对比了吸附前后虾壳生物质炭的FT-IR谱图(图 9)。吸附前在1 125.7cm-1处的C—O—C伸缩振动吸收峰经过吸附Cr6+后偏移到1 170.4 cm-1,而原本在620 cm-1处的NH2面外振动吸收峰在吸附后消失,这可能是C—O—C和NH2与Cr2O72-发生了配位。同时在798.4 cm-1处出现Cr2O72-中不对称Cr—O—Cr的耦合振动吸收峰[28],证实Cr6+在虾壳生物质炭表面的吸附行为存在化学吸附模式。
|
图 9 虾壳生物质炭吸附Cr6+前后的红外谱图 Fig. 9 The infrared spectra of shrimp shell-derived biochar before and after adsorption |
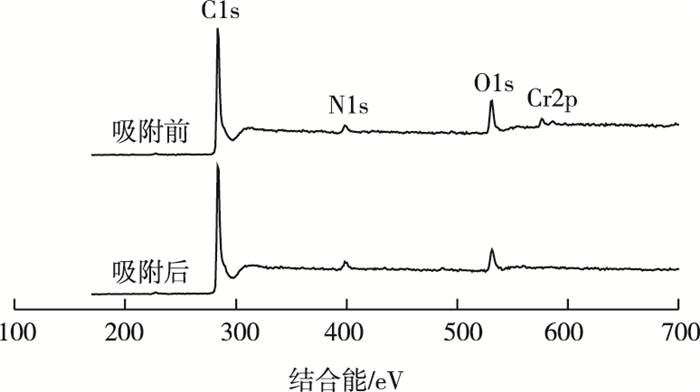
吸附Cr6+前后虾壳生物质炭的宽扫描XPS谱图如图 10所示。虾壳生物质炭在285.60 eV处出现强峰,而在399.17和533.15 eV处出现弱峰,分别表明其主要组成为C (88.43%)、N (4.11%)和O (7.46%)。经过吸附后,在结合能为578.43 eV处虾壳生物质炭出现了Cr2p轨道峰,这表明Cr6+吸附在虾壳生物质炭表面。
|
图 10 虾壳生物质炭吸附Cr6+前后的宽扫描XPS谱图 Fig. 10 XPS survey scanning spectra for shrimp shell-derived biochar before and after Cr6+ adsorption |
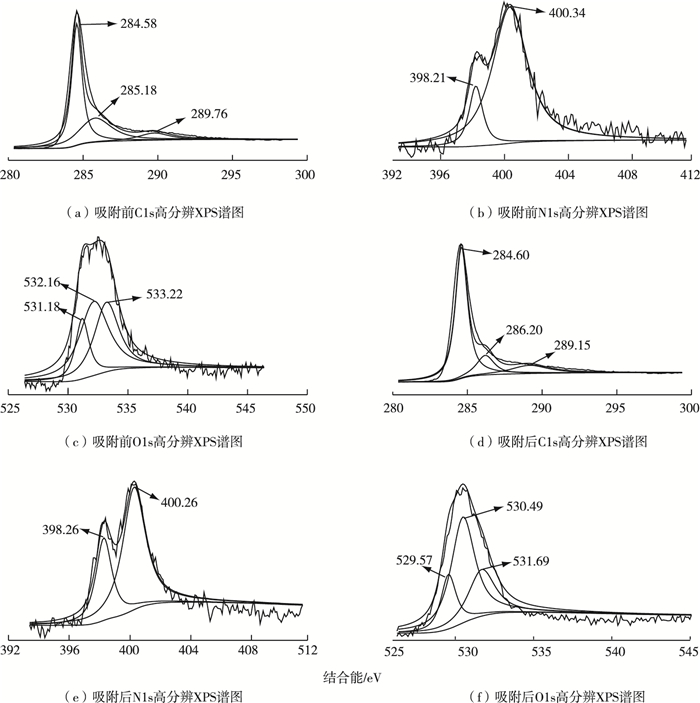
图 11是虾壳生物质炭吸附Cr6+前后C1s、N1s、O1s的高分辨XPS谱图。对比图 11(a)和(d)发现,吸附Cr6+后,结合能在285.18 eV处C—N、C—O—C、O═C—NH中C和289.76 eV处O—C═O中C的峰分别偏移至286.20和289.15 eV处,且285.18 eV处C的比例由35.13%降低至15.42%。C—N、C—O—C、O═C—NH中碳结合能位置的偏移以及比例的减少表明在Cr6+的吸附过程中,虾壳生物质炭表面含C—N、C—O—C、O═C—NH的官能团与Cr6+发生了配位作用。由N1s的XPS分峰谱图可知,吸附前结合能398.21 eV处NH2中N和400.34 eV处NH3+中N的峰位在吸附后没有发生明显偏移,但NH3+中的N1s由85.20%减少至67.63%,这可以归因于NH3+与Cr2O72-的静电引力作用,使得NH3+减少。从吸附前后虾壳生物质炭的O1s的XPS分峰谱图可以看出,532.16 eV(46.07%)处C═O中的氧的峰在吸附后偏移至531.69 eV(26.89%),且结合能529.57 eV(18.23%)和530.49 eV(54.88%)处为新出现的峰,分别为与金属离子结合的O—H(羟基、结合水)和C═O(酯、酸、酰胺)中的氧。由此可知吸附后的虾壳生物质炭表面组成发生了改变,新出现的与金属结合的O1s峰和C—O—C中O1s峰(533.22 eV)的消失都说明Cr以Cr—O或Cr—O—C═O形式结合在虾壳生物质炭表面[22]。
|
图 11 虾壳生物质炭吸附Cr6+前后C1s、N1s、O1s高分辨XPS谱图 Fig. 11 C1s, N1s, O1s high-resolution XPS spectra of shrimp shell-derived biochar before and after Cr6+ adsorption |
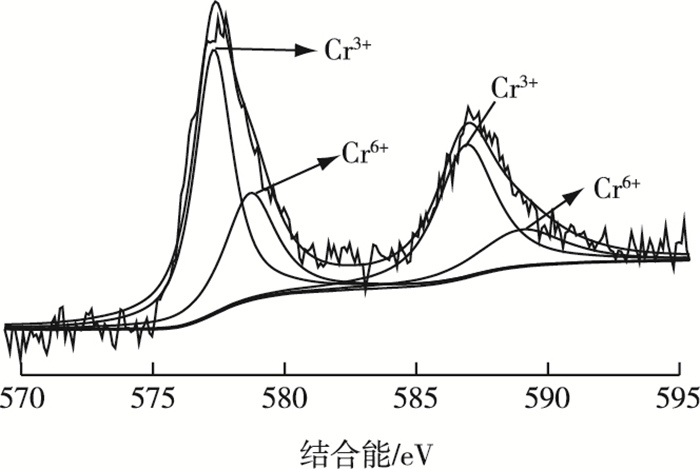
图 12为吸附Cr6+后虾壳生物质炭表面的Cr2p XPS谱图,其中在577.3和586.9 eV处出现了明显的轨道峰,分别对应Cr2p 3/2和Cr2p 1/2轨道的结合能。577.3 eV附近的Cr2p 3/2峰可归于Cr3+,578.7 eV附近的Cr2p 3/2峰可认为是Cr6+;而586.9 eV附近的Cr2p 1/2峰可归于Cr3+,589.0 eV附近的Cr2p 1/2峰可认为是Cr6+,可见Cr6+吸附于虾壳生物质炭后大部分被还原为Cr3+ [29-30]。酸性条件下,生物质炭表面的酚羟基等官能团可以作为电子供体,将吸附在其表面的金属离子还原至低价态[31]。由XPS元素分析结果可知,虾壳生物质炭吸附Cr的谱图中,Cr3+占吸附总Cr含量的70.46%,而Cr6+占总Cr含量的29.54%[32]。
|
图 12 虾壳生物质炭吸附Cr6+后Cr2p高分辨XPS谱图 Fig. 12 Cr2p high-resolution XPS spectra of shrimp shell- derived biochar after Cr6+adsorption |
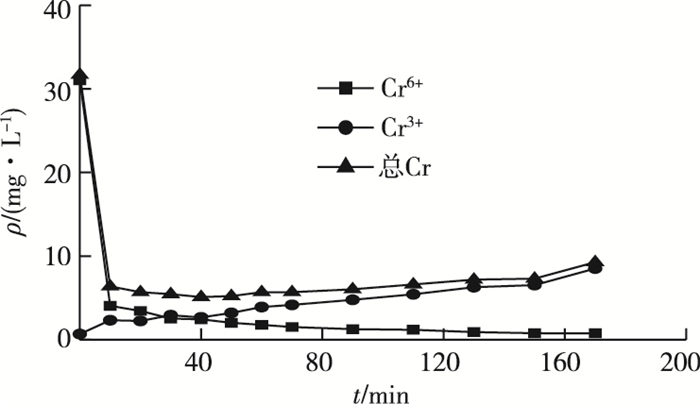
通过二苯基碳酰二肼分光光度法和原子吸收光谱法分别测定了溶液中Cr6+和总Cr的浓度随时间的变化情况,并分析了Cr3+的浓度变化趋势。如图 13所示,溶液中Cr6+的浓度逐渐减少,而总Cr浓度呈现出先减少后增大的趋势,从而得知溶液中Cr3+浓度逐渐增大,该结果进一步证实了虾壳生物质炭在吸附过程中会将Cr6+还原成Cr3+。有研究发现,在酸性条件下吸附剂对Cr3+的吸附明显弱于Cr6+ [33],因此Cr3+会从虾壳生物质炭表面脱附下来进入溶液。
|
图 13 溶液中ρ(Cr6+)、ρ(Cr3+)和ρ(总Cr)的变化 Fig. 13 The variation of Cr6+, Cr3+ and Cr concentration during the adsorption process |
(1) 实验结果表明溶液pH值、Cr6+初始浓度和生物质炭用量对Cr6+在虾壳生物质炭上的平衡吸附量有明显影响。当溶液pH值为3.0,生物质炭用量为0.2 g·L-1,初始ρ(Cr6+)为15 mg·L-1时,虾壳生物质炭对Cr6+的平衡吸附量可达73.83 mg·g-1。
(2) 虾壳生物质炭对Cr6+的吸附动力学符合准二级动力学模型,R2达0.99以上。Langmuir和Freundlich等温吸附模型对吸附平衡数据的拟合度均较高,通过Langmuir等温吸附模型计算得出25 ℃时Cr6+的最大吸附量为111.0 mg·g-1。
(3) XPS及AAS分析结果表明吸附于虾壳生物质炭表面的Cr6+部分被还原为Cr3+,而虾壳生物质炭对Cr3+的吸附明显低于Cr6+,致使Cr3+逐渐从虾壳生物质炭表面脱附,进入溶液中。
| [1] |
DAYAN D, PAINE J. Mechanisms of Chromium Toxicity, Carcinogenicity and Allergenicity:Review of the Literature From 1985 to 2000[J]. Human & Experimental Toxicology, 2001, 20(9): 439-451. (  0) 0) |
| [2] |
COSTA M. Toxicity and Carcinogenicity of Cr(Ⅵ) in Animal Models and Humans[J]. Critical Reviews in Toxicology, 1997, 27(5): 431-442. DOI:10.3109/10408449709078442 (  0) 0) |
| [3] |
KIRPNICK-SOBOL Z, RELIENE R, SCHIESTL R H. Carcinogenic Cr(Ⅵ) and the Nutritional Supplement Cr(Ⅲ) Induce DNA Deletions in Yeast and Mice[J]. Cancer Research, 2006, 66(7): 3480-3484. DOI:10.1158/0008-5472.CAN-05-3944 (  0) 0) |
| [4] |
GE S M, DONG X J, ZHOU J M, et al.Comparative Evaluations on Bio-Treatment of Hexavalent Chromate by Resting Cells of Pseudochrobactrum Sp.and Proteus Sp.in Wastewater[J].Journal of Environmental Management, 2013, 126: 7-12. https://www.sciencedirect.com/science/article/pii/S0301479713002557
(  0) 0) |
| [5] |
LUO S, KE J, YUAN M Q, et al. Cu in S2 Quantum Dots Embedded in Bi2WO6 Nanoflowers for Enhanced Visible Light Photocatalytic Removal of Contaminants[J]. Applied Catalysis B:Environmental, 2018, 221: 215-222. DOI:10.1016/j.apcatb.2017.09.028 (  0) 0) |
| [6] |
YANG D, SUN Y Y, TONG Z W, et al. Fabrication of Bimodal-Pore SrTiO3 Microspheres With Excellent Photocatalytic Performance for Cr(Ⅵ) Reduction Under Simulated Sunlight[J]. Journal of Hazardous Materials, 2016, 312: 45-54. DOI:10.1016/j.jhazmat.2016.03.032 (  0) 0) |
| [7] |
MALKOC E, NUHOGLU Y, DUNDAR M. Adsorption of Chromium(Ⅵ) on Pomace:An Olive Oil Industry Waste:Batch and Column Studies[J]. Journal of Hazardous Materials, 2006, 138(1): 142-151. DOI:10.1016/j.jhazmat.2006.05.051 (  0) 0) |
| [8] |
沈王庆, 雷阳, 邵培利. H3BO3改性柠檬渣对Cu2+ Pb2+ Cr6+的吸附性能[J]. 环境科学研究, 2017, 30(1): 152-158. [ SHEN Wang-qing, LEI Yang, SHAO Pei-li. Adsorption Properties of Lemon Residues Chemically Modifed by H3BO3 to Cu2+, Pb2+ and Cr6+[J]. Research of Environmental Sciences, 2017, 30(1): 152-158.] (  0) 0) |
| [9] |
WU Y H, CHA L G, FAN Y A, et al. Activated Biochar Prepared by Pomelo Peel Using H3PO4 for the Adsorption of Hexavalent Chromium:Performance and Mechanism[J]. Water, Air & Soil Pollution, 2017, 228(10): 405. (  0) 0) |
| [10] |
LI R N, WANG Z W, GUO J L, et al. Enhanced Adsorption of Ciprofloxacin by KOH Modified Biochar Derived From Potato Stems and Leaves[J]. Water Science and Technology, 2018, 77(4): 1127-1136. DOI:10.2166/wst.2017.636 (  0) 0) |
| [11] |
郑孟杰, 李继洲, 靳红梅, 等. 沉水植物生物炭对Cr6+和磷的吸附特性[J]. 生态与农村环境学报, 2017, 33(12): 1132-1139. [ ZHENG Meng-jie, LI Ji-zhou, JIN Hong-mei, et al. Characterization of Cr6+ and Phosphorus Adsorptions of Biochars Derived From Submerged Plants[J]. Journal of Ecology and Rural Environment, 2017, 33(12): 1132-1139. DOI:10.11934/j.issn.1673-4831.2017.12.010] (  0) 0) |
| [12] |
陈坦, 韩融, 王洪涛, 等. 污泥基生物炭对重金属的吸附作用[J]. 清华大学学报(自然科学版), 2014, 54(8): 1062-1067. [ CHEN Tan, HAN Rong, WANG Hong-tao, et al. Adsorption of Heavy Metals by Biochar Derived From Municipal Sewage Sludge[J]. Journal of Tsinghua University(Science and Technology), 2014, 54(8): 1062-1067.] (  0) 0) |
| [13] |
胡志彪, 陈杰斌, 张著森, 等. 竹炭对铬(Ⅵ)离子吸附性能的研究[J]. 功能材料, 2008, 39(3): 523-525. [ HU Zhi-biao, CHEN Jie-bin, ZHANG Zhu-sen, et al. Adsorption Properties of the Bamboo-Charcoal for Chromium(Ⅵ)[J]. Journal of Functional Materials, 2008, 39(3): 523-525. DOI:10.3321/j.issn:1001-9731.2008.03.052] (  0) 0) |
| [14] |
YANG G X, JIANG H. Amino Modification of Biochar for Enhanced Adsorption of Copper Ions From Synthetic Wastewater[J]. Water Research, 2014, 48: 396-405. DOI:10.1016/j.watres.2013.09.050 (  0) 0) |
| [15] |
HAN Y T, CAO X, OUYANG X, et al. Adsorption Kinetics of Magnetic Biochar Derived From Peanut Hull on Removal of Cr (Ⅵ) From Aqueous Solution:Effects of Production Conditions and Particle Size[J]. Chemosphere, 2016, 145: 336-341. DOI:10.1016/j.chemosphere.2015.11.050 (  0) 0) |
| [16] |
谢超然, 王兆炜, 朱俊民, 等. 核桃青皮生物炭对重金属铅、铜的吸附特性研究[J]. 环境科学学报, 2016, 36(4): 1190-1198. [ XIE Chao-ran, WANG Zhao-wei, ZHU Jun-min, et al. Adsorption of Lead and Copper From Aqueous Solutions on Biochar Produced From Walnut Green Husk[J]. Acta Scientiae Circumstantiae, 2016, 36(4): 1190-1198.] (  0) 0) |
| [17] |
谢华林. 二苯碳酰二肼吸光光度法测定水中铬(Ⅵ)[J]. 理化检验(化学分册), 2003, 39(6): 362-364. (  0) 0) |
| [18] |
王建, 贾斌, 郭丽萍, 等. 火焰原子吸收分光光度法测定饲料中的铬[J]. 光谱学与光谱分析, 2005, 25(7): 1142-1144. [ WANG Jian, JIA Bin, GUO Li-ping, et al. The Determination of Chromium in Feeds by Flame Atomic Absorption Spectrophotometry[J]. Spectroscopy and Spectral Analysis, 2005, 25(7): 1142-1144. DOI:10.3321/j.issn:1000-0593.2005.07.036] (  0) 0) |
| [19] |
ZHOU Y M, JIN Q, ZHU T W, et al. Adsorption of Chromium (Ⅵ) From Aqueous Solutions by Cellulose Modified With β-CD and Auaternary Ammonium Groups[J]. Journal of Hazardous Materials, 2011, 187(1/2/3): 303-310. (  0) 0) |
| [20] |
李克斌, 王勤勤, 党艳, 等. 荞麦皮生物吸附去除水中Cr(Ⅵ)的吸附特性和机理[J]. 化学学报, 2012, 70(7): 929-937. [ LI Ke-bin, WANG Qin-qin, DANG Yan, et al. Characteristic and Mechanism of Cr(Ⅵ) Biosorption by Buckwheat Hull From Aqueous Solutions[J]. Acta Chimica Sinica, 2012, 70(7): 929-937.] (  0) 0) |
| [21] |
RANGABHASHIYAM S, SELVARAJU N. Adsorptive Remediation of Hexavalent Chromium From Synthetic Wastewater by a Natural and ZnCl2 Activated Sterculia guttata Shell[J]. Journal of Molecular Liquids, 2015, 207: 39-49. DOI:10.1016/j.molliq.2015.03.018 (  0) 0) |
| [22] |
王学川, 张斐斐, 强涛涛. 超支化胶原纤维吸附剂对Cr(Ⅵ)的吸附特性和机理研究[J]. 化学学报, 2012, 70(24): 2536-2542. [ WANG Xue-chuan, ZHANG Fei-fei, QIANG Tao-tao. Characteristic and Adsorption Mechanism of Hyperbranched Collagen Fiber Toward Cr(Ⅵ)[J]. Acta Chimica Sinica, 2012, 70(24): 2536-2542.] (  0) 0) |
| [23] |
潘经健, 姜军, 徐仁扣, 等. Fe(Ⅲ)改性生物质炭对水相Cr(Ⅵ)的吸附试验[J]. 生态与农村环境学报, 2014, 30(4): 500-504. [ PAN Jing-jian, JIANG Jun, XU Ren-kou, et al. Adsorption of Aqueous Cr(Ⅵ) by Fe(Ⅲ)-Modified Biochar[J]. Journal of Ecology and Rural Environment, 2014, 30(4): 500-504. DOI:10.3969/j.issn.1673-4831.2014.04.015] (  0) 0) |
| [24] |
CHENG R M, OU S J, XIANG B, et al. Adsorption Behavior of Hexavalent Chromium on Synthesized Ethylenediamine Modified Starch[J]. Journal of Polymer Research, 2009, 16(6): 703-708. DOI:10.1007/s10965-009-9276-9 (  0) 0) |
| [25] |
MIAO Q C, BI E P, LI B H. Roles of Polar Groups and Aromatic Structures of Biochar in 1-Methyl-3-Octylimidazolium Chloride Ionic Liquid Adsorption:pH Effect and Thermodynamics Study[J]. Environmental Science and Pollution Research, 2017, 24(28): 22265-22274. DOI:10.1007/s11356-017-9886-4 (  0) 0) |
| [26] |
SHEHA R REI-SHAZLY E A. Kinetics and Equilibrium Modeling of Se(Ⅵ) Removal From Aqueous Solutions Using Metal Oxides[J]. Chemical Engineering Journal, 2010, 160: 63-71. DOI:10.1016/j.cej.2010.03.004 (  0) 0) |
| [27] |
GARG U K, KAUR M P, GARG V K, et al. Removal of Hexavalent Chromium From Aqueous Solution by Agricultural Waste Biomass[J]. Journal of Hazardous Materials, 2007, 140(1/2): 60-68. (  0) 0) |
| [28] |
HUANG X P, HOU X J, SONG F H, et al. Facet-Dependent Cr(Ⅵ) Adsorption of Hematite Nanocrystals[J]. Environmental Science & Technology, 2016, 50(4): 1964-1972. (  0) 0) |
| [29] |
BEESLEY L, MORENO-JIMÉNEZ E, GOMEZ-EYLES J L. Effects of Biochar and Greenwaste Compost Amendments on Mobility, Bioavailability and Toxicity of Inorganic and Organic Contaminants in a Multi-Element Polluted Soil[J]. Environmental Pollution, 2010, 158(6): 2282-2287. DOI:10.1016/j.envpol.2010.02.003 (  0) 0) |
| [30] |
伍清新, 刘杰, 游少鸿, 等. 李氏禾湿地系统净化Cr(Ⅵ)污染水体的机理研究[J]. 环境科学学报, 2014, 34(9): 2306-2312. [ WU Qing-xin, LIU Jie, YOU Shao-hong, et al. Decontamination Mechanism of Cr(Ⅵ)-Polluted Water in Constructed Wetland Planted With Leersia Hexandra Swartz[J]. Acta Scientiae Circumstantiae, 2014, 34(9): 2306-2312.] (  0) 0) |
| [31] |
HSU N H, WANG S L, LIN Y C, et al. Reduction of Cr(Ⅵ) by Crop-Residue-Derived Black Carbon[J]. Environmental Science & Technology, 2009, 43(23): 8801-8806. (  0) 0) |
| [32] |
CHEN X M, ZHANG W G, LUO X L, et al. Efficient Removal and Environmentally Benign Detoxification of Cr(Ⅵ) in Aqueous Solutions by Zr(Ⅳ) Cross-Linking Chitosan Magnetic Microspheres[J]. Chemosphere, 2017, 185: 991-1000. DOI:10.1016/j.chemosphere.2017.07.113 (  0) 0) |
| [33] |
TEL H, ALTAS Y, TANER M S. Adsorption Characteristics and Separation of Cr(Ⅲ) and Cr(Ⅵ) on Hydrous Titanium(Ⅳ) Oxide[J]. Journal of Hazardous Materials, 2004, 112(3): 225-231. DOI:10.1016/j.jhazmat.2004.05.025 (  0) 0) |




