2. 大气环境与装备技术协同创新中心, 江苏 南京 210044;
3. 南京信息工程大学环境科学与工程学院, 江苏 南京 210044
2. Collaborative Innovation Center of Atmospheric Environment and Equipment Technology, Nanjing 210044, China;
3. School of Environmental Science and Engineering, Nanjing University of Information Science & Technology, Nanjing 210044, China
氟元素是组成人体牙齿和骨骼的主要成分之一,是人体的必需元素[1]。饮用水中含氟的适宜质量浓度为0.5~1.0 mg·L-1,浓度过高时环境健康风险较大[2-6]。如长期饮用含氟量高于1.0 mg·L-1的水时易患氟斑牙;当水中含氟量高于4.0 mg·L-1时则会引起骨膜增生、形成骨刺、骨节硬化、骨质疏松、骨骼变形和发脆等氟骨病[7-9],因此研究一种经济有效、操作简单的除氟方法非常必要。目前,对超标含氟水的处理方法主要有沉淀法(包括化学沉淀法和混凝沉淀法)、电絮凝法、电渗析法、反渗透法、离子交换法和吸附法等[10-14]。其中吸附法由于操作简单和费用较低,常被用于低浓度含氟水的处理[15-16]。为此,吸附剂的选择对采用吸附法提高水中氟的去除具有重要意义。
骨炭具有表面积高、孔隙发达、易于改性和价格低廉等特点,已被广泛用于废水和土壤中氟化物和重金属的去除。羊骨、牛骨、鱼骨和鸡骨等制备的骨炭除氟效果比较好[17-19],且无需调整原水pH值。酸、碱、黏土、金属盐和稀土铈等材料已被用于骨炭改性[20-23],以进一步提高其对氟的吸附容量。另外,已有大量研究分析了骨炭对氟的吸附机理[24-26]。但目前有关骨炭去除水中氟的研究大多处于实验室阶段,在实际中的应用研究鲜见报道。为此,笔者选择3种兽骨(牛骨、猪骨和鸡骨)制备骨炭,研究3种骨炭对农村地下水的除氟效果,并与常用除氟剂(活性氧化铝)相比较,分析骨炭的除氟能力与机理,以期为农村地区氟超标饮用水的治理提供理论指导。
1 材料与方法 1.1 实验材料实验所用的牛骨、鸡骨和猪骨取自南京某饭店。在制备骨炭之前,先将骨头水洗,以清洗其表面的尘土,然后将一定质量的牛骨、猪骨和鸡骨等分别置于马弗炉中,加热至450 ℃烧制2 h分别制成牛骨炭、猪骨炭和鸡骨炭。将3种骨炭研磨后分别过0.2~2 mm孔径筛,然后水洗取密度大于水的骨炭,烘干后备用。活性氧化铝取自洁之源水处理材料有限公司,粒径为0.2~2 mm。
1.2 等温吸附实验配置ρ(F-)为10、20、40、80、160和320 mg·L-1的溶液,调节pH值为8。分别取0.5 g活性氧化铝、牛骨炭、猪骨炭和鸡骨炭,置于100 mL聚乙烯瓶中,然后分别加入40 mL不同浓度的氟溶液,室温(25 ℃)下振荡24 h。每个处理设3次重复,振荡结束后,取其溶液测定氟浓度,并通过下列公式计算骨炭对氟的吸附量。
| $ {Q_{\rm{e}}} = \frac{{({C_0} - {C_{\rm{e}}}) \times V}}{W}, $ | (1) |
| $ {Q_t} = \frac{{({C_0} - {C_t}) \times V}}{W}。$ | (2) |
式(1)~(2)中,Qe为平衡溶液氟的吸附量,mg·g-1;Qt为t时刻氟的吸附量,mg·g-1;C0、Ce和Ct分别为初始溶液、平衡溶液和t时刻溶液中氟的质量浓度,mg·L-1;V为加入氟溶液的体积,L;W为加入的除氟剂质量,g。
分别采用Langmuir[27]和Freundlich[28]2种模型拟合不同材料对氟的吸附过程,计算公式为
| $ {C_{\rm{e}}}/{Q_{\rm{e}}} = 1/({K_{\rm{L}}}{Q_{\rm{m}}}) + {C_{\rm{e}}}/{Q_m}, $ | (3) |
| $ {Q_{\rm{e}}} = {K_{\rm{f}}} \times {C_{\rm{e}}}^{\frac{1}{n}} 。$ | (4) |
式(3)~(4)中,Qm为氟的最大吸附量,mg·g-1;KL为与吸附热有关的吸附平衡常数,L·mg-1,可用来衡量除氟剂对溶液中氟的吸附亲和力大小;Kf为表示吸附能力大小的常数,用来衡量除氟剂的吸附能力,L·mg-1;n为Freundlich等温吸附常数,用来衡量除氟剂的吸附强度大小。
1.3 动态吸附实验分别将活性氧化铝、牛骨炭、猪骨炭和鸡骨炭(1 g)放置于250 mL聚乙烯瓶中,然后分别将100 mL ρ(F-)为16 mg·L-1的溶液(pH=8)放入聚乙烯瓶中,并在室温(25 ℃)中振荡,每个处理设3次重复。在振荡后的第1、2、3、4、5、8、12和24小时取样,测定溶液中氟浓度,并计算氟的吸附量。然后采用准一级动力学方程、准二级动力学方程和颗粒内扩散方程来模拟分析4种材料对氟的吸附过程,其方程式分别为
| $ {\rm{lg}}({Q_{\rm{e}}} - {Q_t}) = \lg{Q_{\rm{e}}} - {K_1}t, $ | (5) |
| $ t/{Q_t} = 1/{K_2}{Q_{\rm{e}}} + 1/{Q_{\rm{e}}}t, $ | (6) |
| $ {Q_t} = {K_{\rm{p}}} \times {t^{0.5}} + C。$ | (7) |
式(5)~(7)中,K1为准一级动力学反应速率常数,min-1;K2为准二级动力学反应速率常数,g·μg-1·min-1;Kp为颗粒内扩散速率常数,μg·g-1·min1/2;C为常数。
1.4 连续进水吸附柱实验取直径2 cm、高10 cm有机玻璃柱制成吸附柱,并分别将活性氧化铝、牛骨炭、猪骨炭和及骨炭(10 g)装入吸附柱中,两端采用无脂棉封口,吸附剂高度约7 cm。参照山西平遥梁家堡地区地下水氟浓度,配置ρ(F-)为2.4 mg·L-1的溶液(pH=8)。采用蠕动泵自下而上将溶液泵入吸附柱,流速为6.5 mL·min-1,每隔一定时间测定出水氟浓度,直至出水ρ(F-)>1 mg·L-1时停止进水。
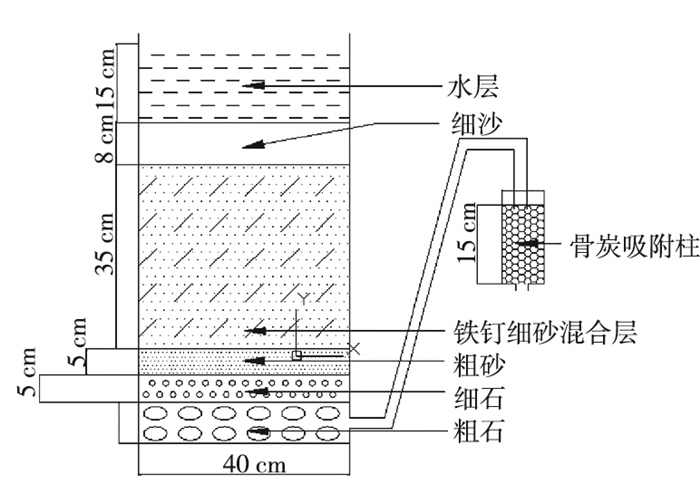
1.5 小试实验2017年7月取直径8 cm、高15 cm有机玻璃柱制成吸附柱,称取350 g牛骨炭放入吸附柱中,并在吸附柱两端采用无脂棉封口,吸附剂(牛骨炭)高度约12 cm。小试实验分别在实验室和山西平遥梁家堡进行。在实验室小试时,进水溶液ρ(F-)为2.3 mg·L-1,pH值为8.1,流速为5 mL·s-1。山西平遥梁家堡地区地下水出水ρ(F-)为1.2 mg·L-1(pH=8.1),将装有牛骨炭的吸附柱放在慢滤池的出口,进入吸附柱的流速为2 mL·s-1(图 1)。
|
图 1 慢滤池-吸附柱装置示意 Fig. 1 Schematic diagram of slow filter-adsorption column device |
水中的氟浓度采用离子选择电极法测定。样品的表面形貌特征采用日本日立公司的SU1510型扫描电子显微镜测定;样品孔隙结构采用美国康塔公司的Autosorb-iQ-AG-MP型全自动氮吸附比表面积测试仪测定,测定方法为先将样品置于50 ℃条件下干燥,然后称取一定质量的样品放置于球形管中,在液氮(77 K)的条件下完成吸附和脱附过程,最后利用BET和BTH法分别计算出各样品的比表面积、孔容和孔径分布。样品的FT-IR表征采用Nicolet iS5型傅里叶变换红外光谱(FT-IR),使用KBr压片,样品与KBr的质量比为1:100,分辨率为4 cm-1,扫描范围为400~4 000 cm-1。
1.7 数据处理采用Microsoft Excel 2013软件进行数据分析与绘图。
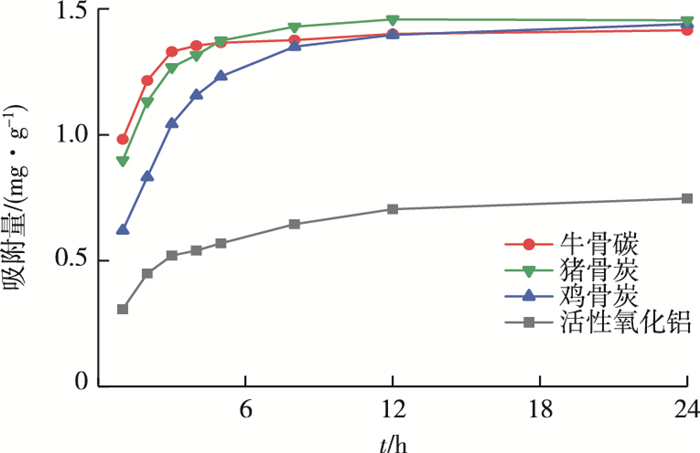
2 结果与讨论 2.1 骨炭对氟的吸附速率如图 2所示,4种材料对氟的吸附量均随着时间的增加而增加,前3 h吸附速度比较快,12 h后吸附速度基本不变,该结果与前人研究结果一致,即24 h吸附达到平衡[29-31]。考虑到实际应用中吸附效率,后续实验选取吸附时间为3 h,计算投药量,设计停留时间。
|
图 2 不同时间下吸附材料对氟的吸附量 Fig. 2 Amount of adsorption of fluorine for different adsorbent at different time |
如表 1所示,准一级和准二级动力学均能较好地拟合骨炭对氟的吸附过程,但准二级动力学模型的R2更大,均大于0.999,说明准二级动力方程可以更好地反映骨炭对氟离子的吸附过程,该结果与NIGRI等[32]的研究结果相一致。活性氧化铝和鸡骨炭的K2值较小,表明活性氧化铝和鸡骨炭对氟的吸附速率较慢。
|
|
表 1 4种材料对氟吸附的动力学参数 Table 1 Parameters of kinetic adsorption of fluorine for four adsorbents |
由于准二级动力学模型的基本假设是吸附速率受化学吸附机理的控制[33],因此可推断骨炭对水中氟的吸附以化学吸附为主[34]。颗粒内扩散方程对吸附氟的过程的拟合效果相对较差,说明颗粒内扩散不是吸附速率控制的唯一步骤,即吸附速率受吸附和扩散等多方面的影响[35]。
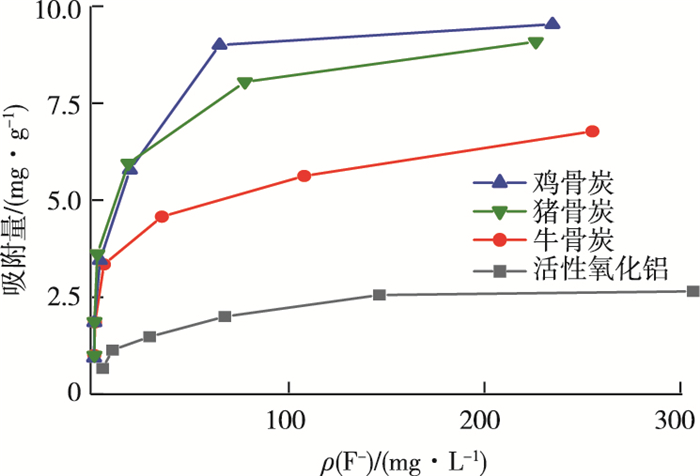
2.2 骨炭对氟的吸附能力活性氧化铝、牛骨炭、猪骨炭和鸡骨炭对氟的吸附如图 3所示。4种材料对氟的吸附量随着氟浓度增加而增加,其原因是氟浓度的增加能够增强固液间的吸附力,同时促进平衡吸附量[36]。通过比较发现,3种骨炭对氟的吸附量均大于活性氧化铝。
|
图 3 不同氟离子浓度对吸附量的影响 Fig. 3 Effect of different fluorine concentration on adsorption of fluorine |
Langmuir和Freundlich等温吸附模型均能较好地拟合材料对氟的吸附行为(表 2)。活性氧化铝、牛骨炭、猪骨炭和鸡骨炭对氟的最大吸附量(Qmax)分别为2.487、5.336、7.974和7.236 mg·g-1,其中活性氧化铝的最大吸附量与厂家提供的理论值(2.8 mg·g-1)相近。3种骨炭对氟的吸附量均显著大于活性氧化铝对氟的吸附量。从Kf可看出3种骨炭的吸附能力远大于活性氧化铝,4种材料对氟吸附能力从大到小依次为猪骨炭>鸡骨炭>牛骨炭>活性氧化铝;1/n < 1时说明吸附过程为优惠型吸附,吸附反应较易进行[31]。通过比较KL值,发现3种骨炭对氟离子的亲和力从大到小依次为牛骨炭>鸡骨炭>猪骨炭,骨炭对氟的亲和力远大于活性氧化铝,其中牛骨炭的亲和力最强。
|
|
表 2 4种材料对氟吸附的Langmuir和Freundlich等温吸附参数 Table 2 Parameters of Langmuir and Freundlich isotherms adsorption of fluorine for four adsorbents |
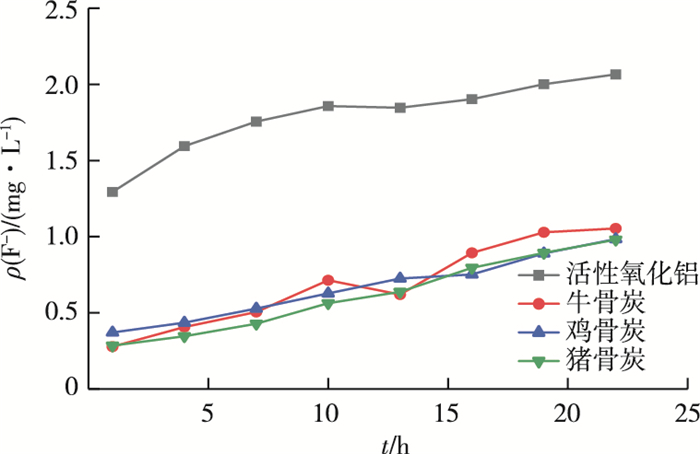
由图 4可知,当进水ρ(F-)为2.4 mg·L-1时,在不同时间段活性氧化铝吸附柱出水中ρ(F-)均大于1 mg·L-1,表明活性氧化铝去除低浓度氟的能力较差。因此,当活性氧化铝处理农村地区低氟地下水时,出水中ρ(F-)已超过饮用水氟的标准(1 mg·L-1),该结果说明活性氧化铝不适用于处理低浓度含氟〔ρ(F-) < 2.4 mg·L-1〕地下水。在运行19 h后,牛骨炭吸附柱出水中ρ(F-)>1 mg·L-1;在运行23 h后鸡骨炭和猪骨炭吸附柱出水ρ(F-)均>1 mg·L-1。该结果说明,骨炭吸附柱在运行19 h前出水中ρ(F-) < 1 mg·L-1,出水氟浓度满足饮用水的标准。这些结果表明与商用活性氧化铝相比,骨炭更适用于低浓度农村地区地下水除氟的处理。
|
图 4 吸附柱出水中氟离子浓度的变化 Fig. 4 Variation of fluorine concentration in the effluent from the adsorption column |
将牛骨和猪骨制成的滤芯分别置于实验室处理含氟污水和山西省平遥县梁家堡某村民家处理地下水,其对氟的去除效果如表 3所示。骨炭对氟的去除率达到69%以上,出水ρ(F-)均 < 1 mg·L-1,达到饮用水的标准。然而随着运行时间的增加,出水氟浓度逐渐增加。以山西平遥实地处理地下水为例,装有骨炭滤芯的装置经20 d的运行后,出水ρ(F-)>1 mg·L-1。在该实验中,运行20 d后出水氟浓度超过饮用水标准,可能与吸附剂(350 g)比较少有关,后续可以通过优化骨炭制备或骨炭与污水的最佳配比、吸附柱的最佳高度等方法来延长骨炭使用时间。
|
|
表 3 骨炭对氟的去除率 Table 3 Efficiency of removal of fluoride by bone biochar |
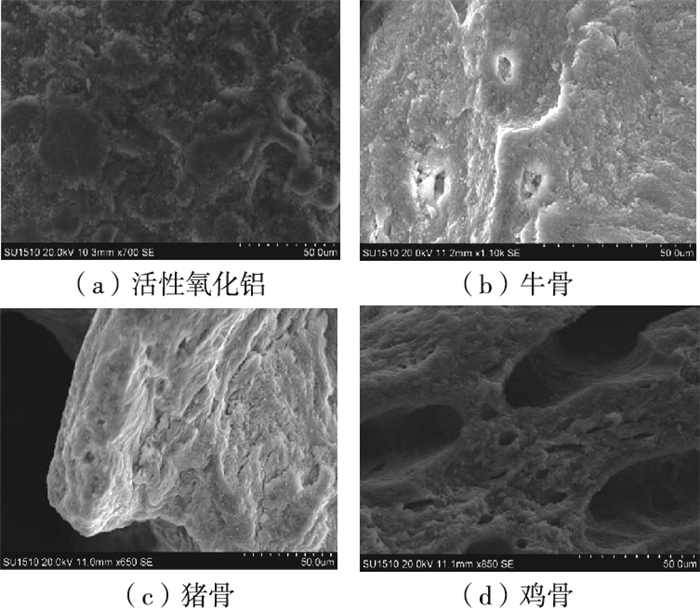
从图 5(a)可见,活性氧化铝的表面呈片状分布,堆块颗粒较大,表面没有特别明显的孔隙结构,有断裂,因此对氟的吸附性能较差。牛骨炭表面粗糙,有少量较小孔隙,呈块状〔图 5(b)〕。猪骨炭表面最为粗糙,孔隙较多,有较多凸起〔图 5(c)〕。鸡骨炭表面粗糙,孔隙较大且相通〔图 5(d)〕。因此猪骨炭和鸡骨炭的空间结构较为丰富,有利于促进对氟离子的吸附。
|
图 5 活性氧化铝、牛骨、猪骨和鸡骨扫描电镜图 Fig. 5 Scanning electron micrograph of activated alumina, cow bone, pig bone and chicken bone |
4种材料的孔隙结构参数见表 4。猪骨炭、鸡骨炭和牛骨炭的比表面积分别为128.7、111.7和103.6 m2·g-1。有研究表明,骨炭的比表面积越大,吸附氟离子量越大[37]。在该研究中,活性氧化铝的比表面积最大(256.4 m2·g-1),但对氟的吸附量最小,说明比表面积不是影响活性氧化铝和骨炭间对氟吸附的主要因素,有资料表明骨炭中含有碳酸根,可以与氟离子发生较强的离子交换作用[37]。
|
|
表 4 4种材料的孔隙结构参数 Table 4 Parameters of porosity structure of four materials |
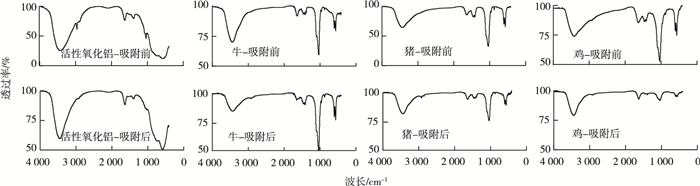
4种材料吸附氟前后的FTIR变化如图 6所示。对于活性氧化铝,吸附前活性氧化铝在3 440 cm-1处出现O—H伸缩振动峰,应为结晶水,2 975、1 640和1 384 cm-1处出现氧化铝特征峰,1 049和590 cm-1处出现SO42-特征峰。吸附后,在2 975 cm-1处的氧化铝基本骨架的特征峰消失,在1 049和590 cm-1处的SO42-特征峰也消失,说明活性氧化铝除氟过程有离子交换[38]。由此推测,该实验所用的活性氧化铝对于氟离子存在化学吸附。相关研究表明,pH值约为7.1条件下活性氧化铝对水中常见阴离子的吸附亲和力从大到小为OH->F->SO42->Cl->HCO3-,同时活性氧化铝的除氟过程为(Al2O3)n·H2SO4+2F-=(Al2O3)n·2HF+SO42-[39]。
|
图 6 4种材料的吸氟前后红外吸收光谱 Fig. 6 Infrared absorption spectra of four adsorbents before and after adsorption of fluoridation |
3种骨炭在吸附前在560~630 cm-1及1 000~1 200 cm-1处是PO43-的特征峰,在3 440和1 637是羟基引起的吸收峰,1 466和1 420 cm-1出现CO32-的吸收双峰,说明3种骨炭主要成分均为羟基磷酸钙和碳酸钙。同时可以明显看出鸡骨炭和猪骨炭的PO43-和CO32-特征峰较高,说明羟基磷酸钙和碳酸钙含量较牛骨炭高。吸附后牛骨炭、猪骨炭和鸡骨炭的特征峰都出现了减弱,其中牛骨炭、猪骨炭的特征峰位置保持着稳定,基本骨架没有变化;而鸡骨炭在吸附氟离子之后增加了2 921.16 cm-1处的特征峰。并且吸附后牛骨炭1 038.95 cm-1处的特征峰变尖锐且超过吸附前水平,可推测在一定程度上生成沉淀附着牛骨炭表面。同时在吸附氟后猪骨炭和鸡骨炭CO32-的吸收双峰变小,说明在吸附氟离子的过程中存在离子交换。通过该实验发现骨炭的吸附机理既包括国外学者认为的[Ca3(PO4)2]n·CaCO3+2F-→[Ca3(PO4)2]n·CaF2+CO32-,也有国内学者认为的Ca10(PO4)6(OH)2+2F-→Ca10(PO4)F2+2OH-,Ca10(PO4)6(OH)2+Ca2++2F-→Ca10(PO4)6(OH)2CaF2[40]。
骨炭在组成成分上含有碳酸根、羟基磷酸钙等,它们在吸附氟的同时又发生了离子交换,所以3种骨炭除氟效果强于活性氧化铝。
3 结论(1) 活性氧化铝、牛骨炭、猪骨炭和鸡骨炭对氟的吸附均符合准二级动力学,属于化学吸附,最大吸附量分别为2.487、5.336、7.974和7.236 mg·g-1;骨炭对氟的吸附能力和亲和力均显著大于活性氧化铝,其中牛骨炭亲和力最强。
(2) 处理低氟浓度地下水时骨炭对氟的去除率达到69%以上,其出水ρ(F-) < 1 mg·L-1,达到饮用水的标准,而活性氧化铝对氟的去除率较差,出水ρ(F-)>1 mg·L-1,活性氧化铝不适合处理低氟浓度的地下水。
| [1] |
陈涛, 杨晓瑛, 朱宝余. 利用自制骨炭除氟剂处理农村高氟地下水研究[J]. 中国农村水利水电, 2011(8): 100-103. [ CHEN Tao, YANG Xiao-ying, ZHU Bao-yu. Research on the Disposal of Rural High-Fluorine Groundwater by Self-Made Defluorinating Agents Prepared With Bone Chars[J]. China Rural Water and Hydropower, 2011(8): 100-103.] (  0) 0) |
| [2] |
赵良元, 胡波, 朱迟, 等. 沸石的载铁改性及饮用水除氟试验研究[J]. 环境科学研究, 2008, 21(1): 168-173. [ ZHAO Liang-yuan, HU Bo, ZHU Chi, et al. Modification of Activated Clinoptilolite With Fe3+ and the Efficiency in Fluoride Removal of Drinking Water[J]. Research of Environmental Sciences, 2008, 21(1): 168-173.] (  0) 0) |
| [3] |
WANG X C, KAWAHARA K, GUO X J. Fluoride Contamination of Groundwater and Its Impacts on Human Health in Inner Mongolia Area[J]. Journal of Water Supply:Research and Technology - Aqua, 1999, 48(4): 146-153. DOI:10.2166/aqua.1999.0015 (  0) 0) |
| [4] |
MISRA A K, MISHRA A. Study of Quaternary Aquifers in Ganga Plain, India:Focus on Groundwater Salinity, Fluoride and Fluorosis[J]. Journal of Hazardous Materials, 2007, 144(1/2): 438-448. (  0) 0) |
| [5] |
WANG Y X, REARDON E J. Activation and Regeneration of a Soil Sorbent for Defluoridation of Drinking Water[J]. Applied Geochemistry, 2002, 16(5): 531-539. (  0) 0) |
| [6] |
BROWNE D, WHELTON H, O'MULLANE D. Fluoride Metabolism and Fluorosis[J]. Journal of Dentistry, 2005, 33(3): 177-186. DOI:10.1016/j.jdent.2004.10.003 (  0) 0) |
| [7] |
仇付国, 王晓昌, 王云波. 活性氧化铝和骨炭除氟研究[J]. 西安建筑科技大学学报(自然科学版), 2001, 33(1): 56-60. [ QIU Fu-guo, WANG Xiao-chang, WANG Yun-bo. A Study on Fluoride Removal by Activated Alumina and Bone Charl[J]. Journal of Xi'an University of Architecture & Technology (Natural Science Edition), 2001, 33(1): 56-60. DOI:10.3969/j.issn.1006-7930.2001.01.013] (  0) 0) |
| [8] |
AYOOB S, GUPTA A K. Fluoride in Drinking Water:A Review on the Status and Stress Effects[J]. Critical Reviews in Environmental Science and Technology, 2006, 36(6): 433-487. DOI:10.1080/10643380600678112 (  0) 0) |
| [9] |
SUJANA M G, PRADHAN H K, ANAND S. Studies on Sorption of Some Geomaterials for Fluoride Removal From Aqueous Solutions[J]. Journal of Hazardous Materials, 2009, 161(1): 120-125. DOI:10.1016/j.jhazmat.2008.03.062 (  0) 0) |
| [10] |
SANDOVAL M A, FUENTES R, NAVA J L, et al. Fluoride Removal From Drinking Water by Electro-Coagulation in a Continuous Filter Press Reactor Coupled to a Flocculator and Clarifier[J]. Separation and Purification Technology, 2014, 134: 163-170. DOI:10.1016/j.seppur.2014.07.034 (  0) 0) |
| [11] |
LOGANATHAN P, VIGNESWARAN S, KANDASAMY J, et al. Defluoridation of Drinking Water Using Adsorption Processes[J]. Journal of Hazardous Materials, 2013, 248/249: 1-19. DOI:10.1016/j.jhazmat.2012.12.043 (  0) 0) |
| [12] |
SRIMURALI M, PRAGATHI A, KARTHIKEYAN J. A Study on Removal of Fluorides From Drinking Water by Adsorption Onto Low-Cost Materials[J]. Environmental Pollution, 1998, 99(2): 285-289. DOI:10.1016/S0269-7491(97)00129-2 (  0) 0) |
| [13] |
BHATNAGAR A, KUMAR E, SILLANPÄÄ M. Fluoride Removal From Water by Adsorption:A Review[J]. Chemical Engineering Journal, 2011, 171(3): 811-840. DOI:10.1016/j.cej.2011.05.028 (  0) 0) |
| [14] |
DU J Y, SABATINI D A, BUTLER E C. Synthesis, Characterization and Evaluation of Simple Aluminum-Based Adsorbents for Fluoride Removal From Drinking Water[J]. Chemosphere, 2014, 101: 21-27. DOI:10.1016/j.chemosphere.2013.12.027 (  0) 0) |
| [15] |
MEDELLIN-CASTILLO N A, LEYVA-RAMOS R, PADILLA-ORTEGA E, et al. Adsorption Capacity of Bone Char for Removing Fluoride From Water Solution.Role of Hydroxyapatite Content, Adsorption Mechanism and Competing Anions[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(6): 4014-4021. DOI:10.1016/j.jiec.2013.12.105 (  0) 0) |
| [16] |
RAJKUMAR S, MURUGESH S, SIVASANKAR V, et al. Low-Cost Fluoride Adsorbents Prepared From a Renewable Biowaste:Syntheses, Characterization and Modeling Studies[J]. Arabian Journal of Chemistry, 2015. DOI:10.1016/j.arabjc.2015.06.028 (  0) 0) |
| [17] |
沈小娃.骨炭去除低浓度含氟废水的实验研究[D].赣州: 江西理工大学, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10407-1011169285.htm
(  0) 0) |
| [18] |
BRUNSON L R, SABATINI D A. An Evaluation of Fish Bone Char as an Appropriate Arsenic and Fluoride Removal Technology for Emerging Regions[J]. Environmental Engineering Science, 2009, 26(12): 1777-1784. DOI:10.1089/ees.2009.0222 (  0) 0) |
| [19] |
MIYAZAKI H, NAGASAWA S, MOTOYAMA A, et al. Chemical Reactions of Fluoride Removal by Chicken Bone Char[J]. Journal of Japan Society of Civil Engineers, 2014, 70(7): 527-534. (  0) 0) |
| [20] |
HIKARU M, SHIORI N, AYURI M, et al. Enhancement of Fluoride Removal by Acid and Alkaline Treatment on Chicken Bone Char[J]. Journal of Ecotechnology Research, 2014, 17: 137-142. (  0) 0) |
| [21] |
金浩.炭陶除氟吸附材料的研究[D].福州: 福建农林大学, 2009. [JIN Hao.Research on Carbon/Pottry Adsorption Composite for Removing Fluoride[D].Fuzhou: Fujian Agriculture and Forestry University, 2009.] http://cdmd.cnki.com.cn/Article/CDMD-10389-2009170547.htm
(  0) 0) |
| [22] |
BRUNSON L R, SABATINI D A. Practical Considerations, Column Studies and Natural Organic Material Competition for Fluoride Removal With Bone Char and Aluminum Amended Materials in the Main Ethiopian Rift Valley[J]. Science of the Total Environment, 2014, 488/489: 580-587. DOI:10.1016/j.scitotenv.2013.12.048 (  0) 0) |
| [23] |
ZÚÑIGA-MURO N M, BONILLA-PETRICIOLET A, MENDOZA-CASTILLO D I, et al. Fluoride Adsorption Properties of Cerium-Containing Bone Char[J]. Journal of Fluorine Chemistry, 2017, 197: 63-73. DOI:10.1016/j.jfluchem.2017.03.004 (  0) 0) |
| [24] |
LUKIKO K, MACHUNDA R L, IJUMBA J N. Regeneration of Fluoride-Saturated Bone Char by Means of Wood Ash and Heat[J]. Fluoride, 2016, 49(4): 549-559. (  0) 0) |
| [25] |
ROJAS-MAYORGA C K, BONILLA-PETRICIOLET A, AGUAYO-VILLARREAL I A, et al. Optimization of Pyrolysis Conditions and Adsorption Properties of Bone Char for Fluoride Removal From Water[J]. Journal of Analytical and Applied Pyrolysis, 2013, 104: 10-18. DOI:10.1016/j.jaap.2013.09.018 (  0) 0) |
| [26] |
MEDELLIN-CASTILLO N A, PADILLA-ORTEGA E, TOVAR-GARCÍA L D, et al. Removal of Fluoride From Aqueous Solution Using Acid and Thermally Treated Bone Char[J]. Adsorption, 2016, 22(7): 951-961. DOI:10.1007/s10450-016-9802-0 (  0) 0) |
| [27] |
CHEN Y N, CHAI L Y, SHU Y D. Study of Arsenic(Ⅴ) Adsorption on Bone Char From Aqueous Solution[J]. Journal of Hazardous Materials, 2008, 160(1): 168-172. DOI:10.1016/j.jhazmat.2008.02.120 (  0) 0) |
| [28] |
WEI S C, LI D T, HUANG Z, et al. High-Capacity Adsorption of Cr(Ⅵ) From Aqueous Solution Using a Hierarchical Porous Carbon Obtained From Pig Bone[J]. Bioresource Technology, 2013, 134: 407-411. DOI:10.1016/j.biortech.2013.02.040 (  0) 0) |
| [29] |
NIGRI E M, CECHINEL M A P, MAYER D A, et al. Cow Bones Char as a Green Sorbent for Fluorides Removal From Aqueous Solutions:Batch and Fixed-Bed Studies[J]. Environmental Science and Pollution Research, 2017, 24(3): 2364-2380. DOI:10.1007/s11356-016-7816-5 (  0) 0) |
| [30] |
李佳, 詹艳慧, 林建伟. 镧改性沸石改良太湖底泥的磷吸附特征[J]. 生态与农村环境学报, 2013, 29(4): 500-506. [ LI Jia, ZHAN Yan-hui, LIN Jian-wei. Effect of La-Modified Zeolite on Phosphate Sorption of Taihu Lake Sediments[J]. Journal of Ecology and Rural Environment, 2013, 29(4): 500-506. DOI:10.3969/j.issn.1673-4831.2013.04.017] (  0) 0) |
| [31] |
李三姗, 王楚楚, 何晓云, 等. 改性水生植物生物炭对低浓度硝态氮的吸附特性[J]. 生态与农村环境学报, 2018, 34(4): 356-362. [ LI San-wei, WANG Chu-chu, He Xiao-yun, et al. Adsorption Characteristics of Modified Aquatic Biochar for Low Concentration Nitrate-Nitrogen Onto Modified Macrophytes Biochar[J]. Journal of Ecology and Rural Environment, 2018, 34(4): 356-362.] (  0) 0) |
| [32] |
NIGRI E M, BHATNAGAR A, ROCHA S D F. Thermal Regeneration Process of Bone Char Used in the Fluoride Removal From Aqueous Solution[J]. Journal of Cleaner Production, 2017, 142: 3558-3570. DOI:10.1016/j.jclepro.2016.10.112 (  0) 0) |
| [33] |
林春香, 詹怀宇, 刘明华, 等. 球形纤维素吸附剂对Cu2+的吸附动力学与热力学研究[J]. 离子交换与吸附, 2010, 26(3): 226-238. [ LIN Chun-xiang, ZHAN Huai-yu, LIU Ming-hua, et al. Thermodynamics and Kinetics of Adsorption of Cu(Ⅱ) From Aqueous Solutions a Spherical Cellulose Adsorbent[J]. Ion Exchange and Adsorption, 2010, 26(3): 226-238.] (  0) 0) |
| [34] |
DURAN C, OZDES D, GUNDOGDU A, et al. Kinetics and Isotherm Analysis of Basic Dyes Adsorption Onto Almond Shell (Prunus dulcis) as a Low Cost Adsorbent[J]. Journal of Chemical & Engineering Data, 2011, 56(5): 2136-2147. (  0) 0) |
| [35] |
AYOOB S, GUPTA A K, BHAKAT P B, et al. Investigations on the Kinetics and Mechanisms of Sorptive Removal of Fluoride From Water Using Alumina Cement Granules[J]. Chemical Engineering Journal, 2008, 140(1/2/3): 6-14. (  0) 0) |
| [36] |
YADAV A K, ABBASSI R, GUPTA A, et al. Removal of Fluoride From Aqueous Solution and Groundwater by Wheat Straw, Sawdust and Activated Bagasse Carbon of Sugarcane[J]. Ecological Engineering, 2013, 52: 211-218. DOI:10.1016/j.ecoleng.2012.12.069 (  0) 0) |
| [37] |
赵延杰, 张蒋维, 迟万凯, 等. 纳米羟基磷灰石对氟离子的吸附[J]. 济南大学学报(自然科学版), 2011, 25(2): 138-141. [ ZHAO Yan-jie, ZHANG Jiang-wei, CHI Wan-kai, et al. Adsorption of Fluoride Form Aqueous Solution by Nano-Hydroxyapatite[J]. Journal of University of Jinan(Science and Technology), 2011, 25(2): 138-141. DOI:10.3969/j.issn.1671-3559.2011.02.007] (  0) 0) |
| [38] |
郝晓伟, 黄益宗, 崔岩山, 等. 赤泥和骨炭对污染土壤As化学形态及其生物可给性的影响[J]. 环境化学, 2010, 29(3): 383-387. [ HAO Xiao-wei, HUANG Yi-zong, CUI Yan-shan, et al. Effects of Red Mud and Bone Char Addition on Fractionation and Bio-Accessibility of Arsenic in Contaminated Soil[J]. Environmental Chemistry, 2010, 29(3): 383-387.] (  0) 0) |
| [39] |
EL HADDAD M, MAMOUNI R, SAFFAJ N, et al. Removal of a Cationic Dye-Basic Red 12-From Aqueous Solution by Adsorption Onto Animal Bone Meal[J]. Journal of the Association of Arab Universities for Basic and Applied Sciences, 2012, 12(1): 48-54. DOI:10.1016/j.jaubas.2012.04.003 (  0) 0) |
| [40] |
王涌. 饮用水骨炭除氟机理的研究[J]. 广州大学学报(自然科学版), 2003, 2(5): 423-426. [ WANG Yong. Research on Removing Fluoride Mechanism From Drinking Water by Using Bone Char[J]. Journal of Guangzhou University(Natural Science Edition), 2003, 2(5): 423-426. DOI:10.3969/j.issn.1671-4229.2003.05.006] (  0) 0) |




