2. 洛阳市共生微生物与绿色发展重点实验室/洛阳市植物营养与环境生态重点实验室, 河南 洛阳 471023
2. Luoyang Key Laboratory of Symbiotic Microorganism and Green Development/Luoyang Key Laboratory of Plant Nutrition and Environmental Ecology, Luoyang 471003, China
磷在不同污水中浓度变化广泛, 当含磷废水排入地表水体后会带来严重的环境污染[1-3]。因此, GB 18918—2002《城镇污水处理厂污染物排放标准》规定一级和二级排放的ρ(磷)限值为0.5~3 mg·L-1。磷是大多数生态系统中生物生长的限制因素, 所以容易造成受纳水体的富营养化, 使得水质恶化并威胁水生生物安全[4-5]。目前已有相关的深度控制技术可处理此类低浓度磷酸盐(PO43-)污水, 如生物处理技术和化学沉淀法等[6-11], 且吸附技术被普遍认为是一种实用并经济可行的方法, 其中吸附材料的粒径选择基本以粉末状、甚至是纳米级别[12-17], 但从应用成本和使用方便等方面考虑, 如果选用粒径较大的吸附材料则更有利于实际应用[18-19]。活性炭作为吸附剂已被应用在有机污染物[20-21]、金属离子[22-23]和染料[24-26]等污染物的去除研究中, 其主要优点是成本低、量大, 且高度发达的孔隙结构和巨大的比表面积对污染物具有较强的吸附能力。目前颗粒活性炭对污水中低浓度PO43-的去除效果尚鲜有报道。因此, 笔者利用颗粒无烟煤活性炭为吸收剂, 研究其对低浓度PO43-的吸附效果, 并借助等温吸附、傅里叶变换红外光谱(FTIR)、X射线能谱(XRD)、颗粒Zeta电位等方法, 探索无烟煤活性炭对低浓度PO43-的吸附过程与机制, 为颗粒活性炭应用于城市尾水PO43-的深度净化提供依据。
1 材料与方法 1.1 颗粒无烟煤活性炭颗粒无烟煤活性炭购自河南巩义滤料有限公司, 使用前用蒸馏水清洗并110 ℃烘干。前期研究表明, 0.5~1与0.01~0.1 mm粒径的活性炭比表面积差别不大, 因此选用粒径为0.5~1 mm的颗粒活性炭为吸附材料, 用氮气吸附法(ASAP2000)测定其比表面积和孔径。活性炭的C、N、O、S、P的含量w分别为7.49%、3.35%、6.01%、1.26%、1.72%;w(灰分)为15.15%, w(SiO2)为2.15%, Fe、Al、Mg、Ca的含量w为5.13%, 比表面积为551.49 m2·g-1, 孔体积为0.279 cm3·g-1, 平均孔径为202.4 nm。
1.2 研究方法用KH2PO4配置ρ(PO43-)为2 mg·L-1的模拟废水, 将0、0.4、1.0、2.0、4.0、10.0、20.0和40.0 g·L-1无烟煤活性炭和50 mL模拟PO43-废水分别放置于250 mL锥形瓶中, 溶液的pH值用0.05 mol·L-1 NaOH或HCl调节至6.0。在25 ℃、250 r·min-1条件下振荡24 h, 吸附平衡后采用钼酸盐比色法测定溶液中磷浓度, 并计算活性炭对PO43-的吸附量。根据无烟煤剂量试验结果分别设置特定条件下不同吸附时间(0、0.08、0.17、0.33、0.50、1、2、4、6、8、12和16 h)、不同温度(5、15、25、35和45 ℃)和不同pH值(3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0和11.0)对活性炭吸附磷的影响研究。在吸附平衡后, 溶液过0.45 μm孔径膜, 分析PO43-的平衡吸附浓度和吸附量。
吸附等温线:将2 g颗粒活性炭加入250 mL锥形瓶中, 并加入50 mL PO43-溶液, 使得溶液中ρ(PO43-)分别为0、5、10、20、30、50、100、200、300和500 mg·L-1。将溶液的pH值调节至6.0, 25 ℃条件下以250 r·min-1振荡6 h, 最后将悬浮液过0.45 μm孔径滤膜, 用于PO43-含量的分析。
Zeta电位:取2 g无烟煤活性炭样品2组份, 用去离子水洗涤干净, 在105 ℃烘箱中干燥24 h, 然后放置在50 mL离心管中, 2组样品分别与50 mL PO43-溶液和50 mL蒸馏水混合, 25 ℃条件下250 r·min-1振荡24 h, 将上述溶液的pH值分别调至3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0、12.0和13.0, 振荡24 h后用Malvern Zetasizer 2000 Zeta电位仪测定蒸馏水和PO43-溶液的Zeta电位。
105 ℃烘箱中干燥24 h后采用FTIR、XRD和SEM分析25 ℃、pH=6.0、吸附时间为6 h、初始ρ(PO43-)为2 mg·L-1的活性炭样品。红外光谱用TENSOR 27(Germany)测定, 把样品和KBr一起压片后在500~4 000 cm-1光谱范围下扫描。并用X射线衍射仪(Philips X′pert Pro)在25 ℃(电压为40 kV, 电流为30 mA)下进行衍射光束测定。
1.3 数据分析用SPSS 16.0软件进行数据分析, 数据以平均值和标准差表示。PO43-平衡吸附量(q)用下列方程式计算:
| $ q = \frac{{V({C_0} - {C_{\rm{e}}})}}{{{m_{\rm{s}}}}} 。$ | (1) |
式(1)中, C0和Ce分别为初始和平衡时的PO43-质量浓度, mg·L-1; V为溶液体积, L; ms为活性炭的质量, g。
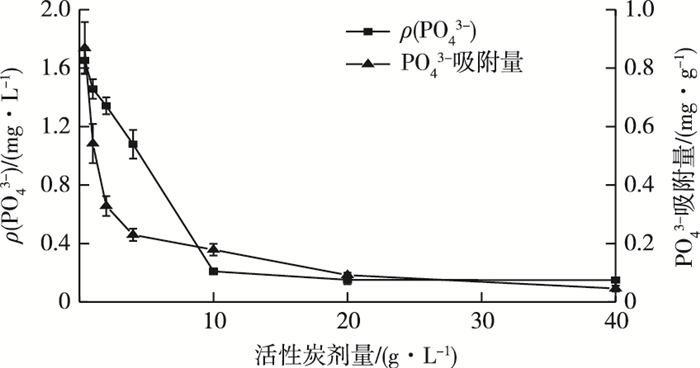
2 结果与分析 2.1 活性炭剂量对PO43-吸附的影响不同用量活性炭(0~40 g·L-1)吸附污水中PO43-的变化见图 1。当无烟煤活性炭剂量为0~10 g·L-1时, PO43-在废水中的平衡浓度会随着活性炭用量的增加而快速降低, 同时活性炭对磷酸盐的单位吸附量呈降低趋势。当活性炭剂量超过10 g·L-1后活性炭对PO43-吸附量的增加趋缓, 溶液中PO43-的平衡浓度趋于稳定, 继续增大活性炭用量后吸附量不再增加, 说明处理ρ(PO43-)为2.0 mg·L-1的溶液时,颗粒活性炭用量为10 g·L-1比较合适。
|
图 1 不同剂量活性炭对污水中PO43-的吸附影响 Fig. 1 The effect of activated carbon dose on PO43- adsorption |
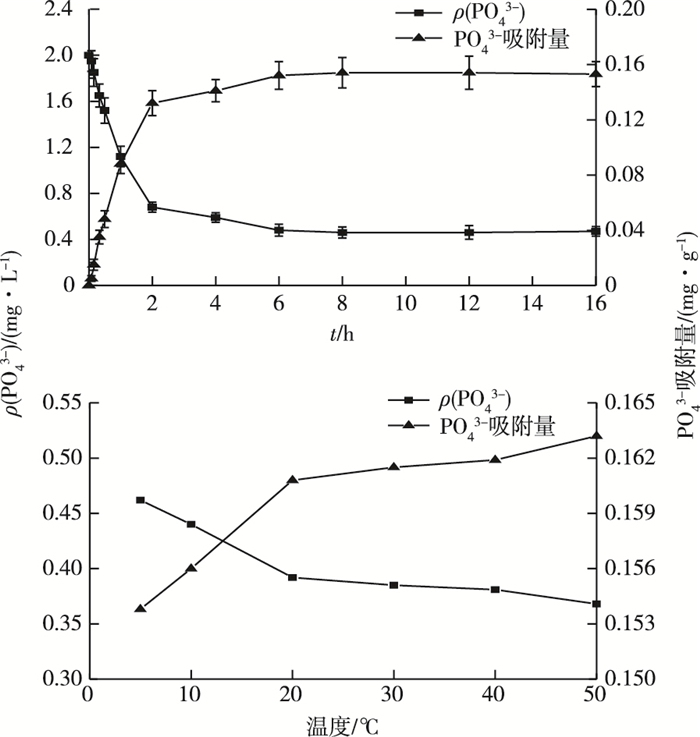
吸附时间和温度变化会对活性炭的吸磷效果产生影响。从图 2可知, PO43-的平衡浓度会随着吸附时间的增加而降低, 最初2 h内PO43-的平衡浓度降低很快, 2~6 h降低减慢, 6~16 h趋于稳定。该结果表明在前2 h内PO43-会快速吸附到活性炭表面上, 6 h时活性炭对PO43-的吸附量达到0.152 mg·g-1。
|
图 2 吸附时间和温度对活性炭吸附PO43-的影响 Fig. 2 The effect of contact time and temperature on PO43- adsorption |
溶液中PO43-的平衡浓度会随着溶液温度的升高而降低, 当温度从5 ℃增加到20 ℃时PO43-的平衡浓度降低幅度较快, 此后随着温度的上升活性炭对PO43-吸附量的增加趋势不明显。高温有利于活性炭对PO43-的吸附, 因为高温会导致无烟煤颗粒活性炭中Al3+、Fe3+和Ca2+溶解度的增加, 从而形成FePO4、AlPO4、Ca3(PO4)2沉淀[27]。因此, 考虑到实际的应用, 活性炭对低浓度磷酸盐的吸附间和温度的选择以6 h和25 ℃为宜。
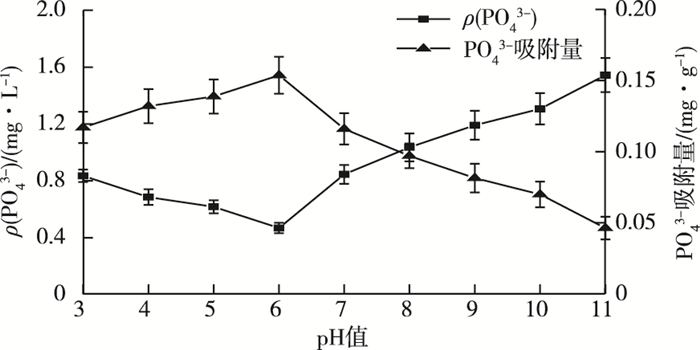
2.3 pH值对PO43-吸附的影响pH值会对PO43-吸附效果产生较大影响。由图 3可知, 当吸附溶液的pH=11.0时PO43-的吸附量最低, 溶液中浓度最高。随着pH值的降低吸附量增加, 当pH值降到6.0时PO43-的平衡浓度最低, 此时活性炭对PO43-的吸附达最大值。此后, 随着pH值的继续降低, PO43-的吸附量又呈下降趋势。因此, pH=6.0时溶液中PO43-的吸附量最高, 磷酸盐去除率达80.35%, 原因在于当pH < 6.0时酸性磷酸根离子主要以H2PO4-, HPO42-的形式存在, 不利于PO43-在活性炭表面发生沉淀吸附。而当pH值较高(6.0~11.0)时, 活性炭表面会发生铝、铁和钙元素与氢氧根的沉淀反应, 从而抑制其与PO43-的沉淀反应[28-29]。
|
图 3 pH值对活性炭吸附PO43-的影响 Fig. 3 The effect of pH on PO43- adsorption |
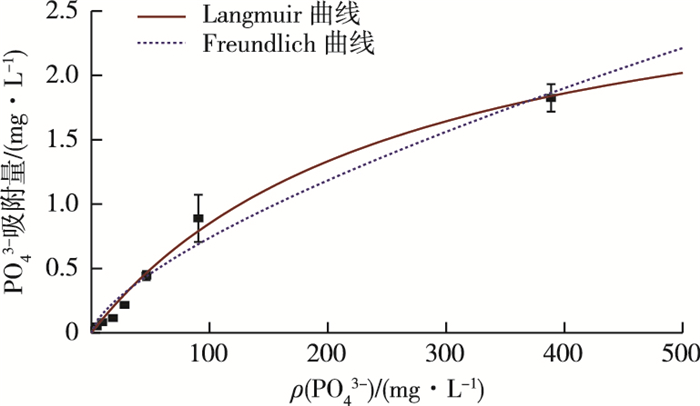
PO43-的等温吸附结果见图 4。随着PO43-浓度的提高, 活性炭对PO43-的吸附能力显著增加, 最大达300 mg·L-1。从Langmuir吸附方程可知, 无烟煤活性炭对PO43-最大的吸附能力为3.07 mg·g-1。不同吸附剂的磷吸附模型和吸附能力差别较大[30], 因为不同吸附剂的化学组分及表面积不同。目前在水处理中对于吸附作用的描述主要有2种类型:一种是由物理吸附作用引起的Freundlich型吸附等温线, 另一种是由化学吸附作用, 即单分子层吸附作用引起的Langmuir型吸附等温线。该研究中无烟煤活性炭对PO43-的吸附等温线更符合Langmuir方程。与一般天然颗粒吸附剂相比, 该研究中的颗粒活性炭填料可以作为磷的吸附剂使用。贺凯等[31]开展了5种填料(天然沸石、陶粒、北京土壤、蛭石和砾石)对PO43-的等温吸附研究, 其中蛭石的最大吸附量只有1.38 mg·g-1。赵雪松等[32]对不同粒径方解石的磷等温吸附表明, 在pH=6条件下方解石的最大吸附量为0.544 mg·g-1, 其他粒径和pH值条件下吸附量也均低于该研究中活性炭的最大吸附量。
|
图 4 活性炭对PO43-的Langmuir和Freundlich等温吸附曲线 Fig. 4 Langmuir and Freundlich isotherms of activated carbon adsorption of PO43- |
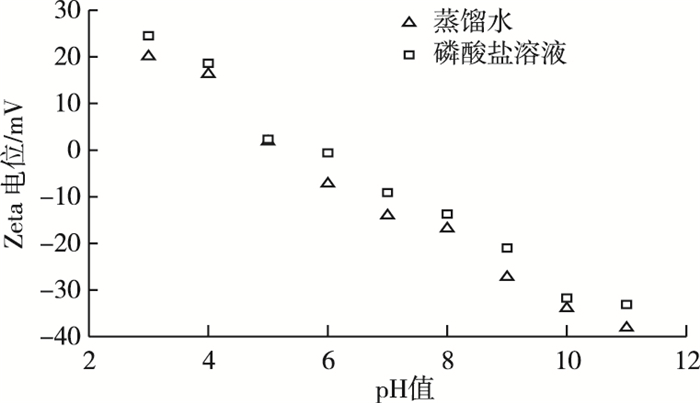
将10 g·L-1无烟煤颗粒活性炭置于蒸馏水和ρ(PO43-)为2.0 mg·L-1的溶液中, 分别测定不同pH值条件下的Zeta电位。由图 5可知, 在pH值为3.0~11.0的范围内, 活性炭在蒸馏水中的Zeta电位低于磷酸溶液, 主要是因为活性炭表面的官能团与PO43-发生静电吸附作用, 使得PO43-吸附在活性炭表面, 导致溶液中H+增加, 增加了溶液中的Zeta电位。研究表明:活性炭除了比表面积和孔径外, 其本身的表面化学性质对吸附过程有重要影响。在活性炭表面石墨层边缘存在不同类型的含氧基团, 这些基团决定了活性炭的表面反应、亲/疏水性、表面酸碱性、催化性能和Zeta电位等。相对来说, 活性炭在溶液中的吸附过程较气相吸附更为复杂, 表面化学性质的影响也更为重要, 因为涉及到溶剂与吸附质的竞争吸附及溶液的性质如pH值及极性等的影响[33]。Zeta电位的分析表明该活性炭上官能团与磷酸盐的结合是其去除磷酸盐的机制之一。
|
图 5 活性炭Zeta电位与pH值之间的关系 Fig. 5 Relationship between Zeta potentials and pH |
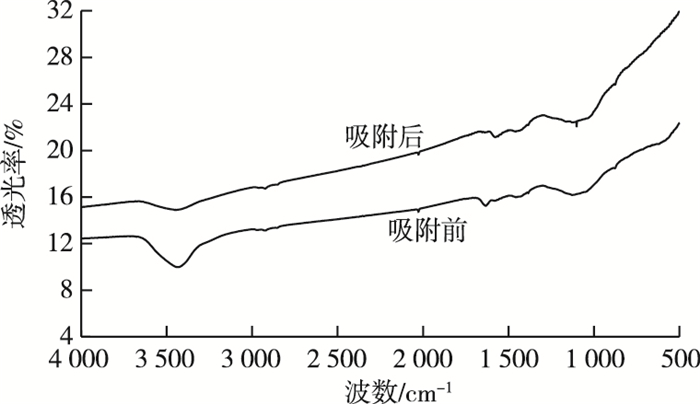
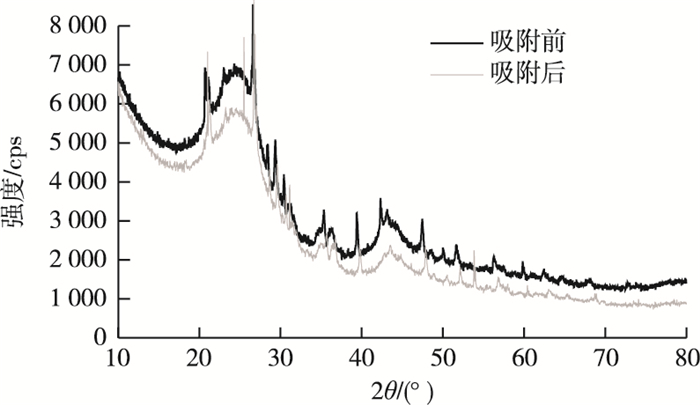
磷酸吸附前后的红外光谱如图 6所示。在3 200和3 700 cm-1之间的谱带表示吸附剂表面上存在自由和氢键—OH基团, 这种拉伸是由于在表面上的硅烷醇基团(Si—OH)和吸附的水(在3 400 cm-1的峰值上)。在3 420 cm-1处无烟煤活性炭中出现的谱带表明氢键存在; 而在2 921和2 847 cm-1处为对称的CO2拉伸。在磷酸盐吸附光谱中有一些新突出光谱, 1 620 cm-1左右的峰为C═C拉伸。比较无烟煤活性炭磷酸盐吸附前后的光谱, 发现磷酸盐吸附到无烟煤活性炭后不同官能团如COO—、—OH和Si—OH的对应峰值发生位移, 这表明这些官能团在PO43-的吸附过程中是有效的。另外, PO43-吸附后在1 100 cm-1处有P—O特征键加强震动, 证明有PO43-吸附到无烟煤活性炭表面上。把上述吸附前后的活性炭颗粒进行X射线衍射扫描(图 7)。从图中可以看出, 该活性炭颗粒在不同2θ处有特殊的化学组成, 并且在磷吸附前后从2θ处为20°到80°有较明显的峰位移, 同时磷的吸附后对应有Ca3(PO4)2、FePO4、AlPO4特征峰2θ在31.1°、25.50°、21°时有增强表现, 说明在该研究中金属离子(Ca2+、Al3+、Fe3+)和活性炭颗粒存在沉淀吸附作用, 因此活性炭吸附前后的图谱会有所改变。
|
图 6 活性炭红外光谱图 Fig. 6 FTIR of activated carbon |
|
图 7 活性炭X衍射光谱图 Fig. 7 X-ray diffraction spectroscopy of activated carbon |
吸附饱和的活性炭颗粒利用电子扫描电镜(SEM)观察吸附前后颗粒表面特征见图 8。活性碳在磷吸附前后表面形态发生变化, 吸附前表面无絮状沉淀物质存在, 吸附后颗粒活性炭表面存在磷酸盐絮状沉淀物, 这说明溶液中的磷酸盐与活性炭表面所含重金属发生了化学反应。

|
图 8 吸附前后活性炭SEM图谱 Fig. 8 SEM spectrum of activated carbon before and after adsorption |
该研究选用的颗粒无烟煤活性炭可以应用于污水中低浓度PO43-的去除中, 吸附优化条件为6 h、pH=6.0、吸附剂量10 g·L-1, 较高温度条件下有利于PO43-的去除。颗粒无烟煤活性炭对水体中PO43-同时存在物理和化学吸附过程, 去除PO43-的机制在于表面官能团的吸附与金属离子共沉淀作用。从Langmuir吸附模型拟合计算得到无烟煤活性炭最大的PO43-吸附能力为3.07 mg·g-1。
| [1] |
常会庆, 徐晓峰. 活性氧化铝去除不同浓度污水中磷的研究[J]. 水土保持学报, 2013, 27(4): 181-185. [ CHANG Hui-qing, XU Xiao-feng. Phosphate Removal From Different Wastewater Concentration by Activate Aluminum Oxide[J]. Journal of Soil and Water Conservation, 2013, 27(4): 181-185.] (  0) 0) |
| [2] |
KRISHNAN K A, HARIDAS A. Removal of Phosphate From Aqueous Solutions and Sewage Using Natural and Surface Modified Coir Pith[J]. Journal of Hazardous Materials, 2008, 152(2): 527-535. DOI:10.1016/j.jhazmat.2007.07.015 (  0) 0) |
| [3] |
常会庆, 徐晓峰, 王世华. 球形陶粒滤池对城市尾水净化效果研究[J]. 生态环境学报, 2012, 21(8): 1452-1456. [ CHANG Hui-qing, XU Xiao-feng, WANG Shi-hua. Advanced Treatment of City Tail Water by Bio-Ceramic Filter[J]. Ecology and Environmental Sciences, 2012, 21(8): 1452-1456.] (  0) 0) |
| [4] |
ISMAIL Z Z. Kinetic Study for Phosphate Removal From Water by Recycled Date-Palm Wastes as Agricultural By-Products[J]. International Journal of Environment Studies, 2012, 69(1): 135-149. DOI:10.1080/00207233.2012.656975 (  0) 0) |
| [5] |
JYOTHI M D, KIRAN K R, RAVINDHRANATH K. Pollution Control in Wastewaters Using New Biosorbents[J]. International Journal of Water Resources and Environmental Engineering, 2012, 4: 73-85. (  0) 0) |
| [6] |
SELVARATNAM T, PEGALLAPATI A K, MONTELYA F, et al. Evaluation of a Thermo-Tolerant Acidophilic Alga, Galdieria Sulphuraria, for Nutrient Removal From Urban Wastewaters[J]. Bioresource Technology, 2014, 156: 395-399. DOI:10.1016/j.biortech.2014.01.075 (  0) 0) |
| [7] |
SEO B S, PARK C M, SONG U, et al. Nitrate and Phosphate Removal Potentials of Three Willow Species and a Bald Cypress From Eutrophic Aquatic Environment[J]. Landscape and Ecological Engineering, 2010, 6(2): 211-217. DOI:10.1007/s11355-009-0102-7 (  0) 0) |
| [8] |
SHI J, PODOLA B, MELKONIAN M. Removal of Nitrogen and Phosphorus From Wastewater Using Microalgae Immobilized on Twin Layers:An Experimental Study[J]. Journal of Applied Phycology, 2007, 19(5): 417-423. DOI:10.1007/s10811-006-9148-1 (  0) 0) |
| [9] |
YAN Y B, SUN X Y, MA F B, et al. Removal of Phosphate From Wastewater Using Alkaline Residue[J]. Journal of Environmental Sciences, 2014, 26(5): 970-980. DOI:10.1016/S1001-0742(13)60537-9 (  0) 0) |
| [10] |
AZAM H M, FINNERAN K T. Fe (Ⅲ) Reduction-Mediated Phosphate Removal as Vivianite[Fe3(PO4)28H2O] in Septic System Wastewater[J]. Chemosphere, 2014, 97: 1-9. DOI:10.1016/j.chemosphere.2013.09.032 (  0) 0) |
| [11] |
吴晓娜, 王助贫, 谢恩, 等. 一株反硝化聚磷菌筛选及其接种量对脱氮除磷效应的影响[J]. 环境工程学报, 2018, 12(2): 544-551. [ WU Xiao-na, WANG Zhu-pin, XIE En, et al. Screening of One Strain of Denitrifying Phosphorus Accumulation Bacteria (DPAB) and Inhibitions Effects of Nitrogen-Phosphorus Removal[J]. Chinese Journal of Environmental Engineering, 2018, 12(2): 544-551.] (  0) 0) |
| [12] |
OLADOJA N A, ADELAGUN R O A, OLOLADE I A, et al. Synthesis of Nano-Sized Hydrocalumite From a Gastropod Shell for Aqua System Phosphate Removal[J]. Separation and Purification Technology, 2014, 124(6): 186-194. (  0) 0) |
| [13] |
DOGˇAN M, ABAK H, ALKAN M. Adsorption of Methylene Blue Onto Hazelnut Shell:Kinetics, Mechanism and Activation Parameters[J]. Journal of Hazardous Materials, 2009, 164(1): 172-181. DOI:10.1016/j.jhazmat.2008.07.155 (  0) 0) |
| [14] |
NGUYEN T A H, NGO H H, GUO W S, et al. Modification of Agricultural Waste/By-Products for Enhanced Phosphate Removal and Recovery:Potential and Obstacles[J]. Bioresource Technology, 2014, 169: 750-762. DOI:10.1016/j.biortech.2014.07.047 (  0) 0) |
| [15] |
WAJIMA T, RAKOVAN J F. Removal Behavior of Phosphate From Aqueous Solution by Calcined Paper Sludge[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2013, 435: 132-138. (  0) 0) |
| [16] |
XU K, DENG T, LIU J T, et al. Study on the Phosphate Removal From Aqueous Solution Using Modified Fly Ash[J]. Fuel, 2010, 89(12): 3668-3674. DOI:10.1016/j.fuel.2010.07.034 (  0) 0) |
| [17] |
申战辉, 史嘉璐, 樊静. 负载型纳米Fe/Ni材料同步去除水中硝酸盐/磷酸盐[J]. 工业水处理, 2017, 37(5): 53-57. [ SHEN Zhan-hui, SHI Jia-lu, FAN Jing. Fe/Ni Bimetal Supported Nano-Particle Composite Materials for the Simultaneous Removal of Nitrate/Phosphate From Water[J]. Industrial Water Treatment, 2017, 37(5): 53-57.] (  0) 0) |
| [18] |
CHEN B. Film-Pore Diffusion Modeling and Contact Time Optimization for the Adsorption of Dyestuffs on Pith[J]. Chemical Engineering Journal, 2001, 84(2): 77-94. DOI:10.1016/S1385-8947(01)00193-0 (  0) 0) |
| [19] |
HO Y S, MCKAY G. Sorption of Dye from Aqueous Solution by Peat[J]. Chemical Engineering Journal, 1998, 70(2): 115-124. DOI:10.1016/S0923-0467(98)00076-1 (  0) 0) |
| [20] |
LIN X Q, JIN Y Q, WU H L, et al. Removal of PCDD/Fs and PCBs From Flue Gas Using a Pilot Gas Cleaning System[J]. Journal of Environmental Sciences, 2013, 25(9): 1833-1840. DOI:10.1016/S1001-0742(12)60292-7 (  0) 0) |
| [21] |
RAZVIGOROVA M, BUDINOVA T, PETROV N, et al. Purification of Water by ACs From Apricot Stones, Lignites and Anthracite[J]. Water Research, 1998, 32(7): 2135-2139. DOI:10.1016/S0043-1354(97)00446-6 (  0) 0) |
| [22] |
AWWAD N S, EL-ZAHHAR A A, FOUDA A M, et al. Removal of Heavy Metal Ions From Ground and Surface Water Samples Using Carbons Derived From Date Pits[J]. Journal of Environmental Chemical Engineering, 2013, 1(3): 416-423. DOI:10.1016/j.jece.2013.06.006 (  0) 0) |
| [23] |
赵研, 郎朗, 姜彬慧, 等. 玉米芯基活性炭吸附去除水中重金属的实验及机理研究[J]. 东北大学学报(自然科学版), 2018, 39(3): 441-445. [ ZHAO Yan, LANG Lang, JIANG Bin-hui, et al. Experiment and Mechanistic Study on Adsorption and Removal of Heavy Metals in Water by Corncob-Based Activated Carbon[J]. Journal of Northeastern University(Natural Science), 2018, 39(3): 441-445.] (  0) 0) |
| [24] |
EMAMI Z, AZIZIAN S. Preparation of Activated Carbon From Date Sphate Using Microwave Irradiation and Investigation of Its Capability for Removal of Dye Pollutant from Aqueous Media[J]. Journal of Analytical and Applied Pyrolysis, 2014, 108: 176-184. DOI:10.1016/j.jaap.2014.05.002 (  0) 0) |
| [25] |
ARSLAN G, PEHLIVAN E. Batch Removal of Chromium (Ⅵ) From Aqueous Solution by Turkish Brown Coals[J]. Bioresource Technology, 2007, 98(15): 2836-2845. DOI:10.1016/j.biortech.2006.09.041 (  0) 0) |
| [26] |
常会庆, 王浩, 徐晓峰. 无烟煤活性炭对酸碱性不同染料废水的吸附研究[J]. 水土保持学报, 2014, 28(2): 276-280. [ CHANG Hui-qing, WANG Hao, XU Xiao-feng. Adsorption Studies of Acid and Base Dyes Wastewater on Anthracite Activated Carbon[J]. Journal of Soil and Water Conservation, 2014, 28(2): 276-280.] (  0) 0) |
| [27] |
LU S G, BAI S Q, SHAN H D. Mechanisms of Phosphate Removal From Aqueous Solution by Blast Furnace Slag and Steel Furnace Slag[J]. Journal of Zhejiang Unvierstiy(Science A), 2008, 9(1): 125-132. DOI:10.1631/jzus.A071272 (  0) 0) |
| [28] |
OGUZ E. Removal of Phosphate From Aqueous Solution With Blast Furnace Slag[J]. Journal of Hazardous Materials, 2004, 114(1/2/3): 131-137. (  0) 0) |
| [29] |
JENKINS D, FERGUSON J F, MENAR A B. Chemical Processes for Phosphate Removal[J]. Water Research, 1971, 5(7): 369-389. DOI:10.1016/0043-1354(71)90001-7 (  0) 0) |
| [30] |
杨欣妍, 魏儒平, 杨柳燕. 污染底泥制备陶粒及除磷潜力研究[J]. 生态与农村环境学报, 2019, 35(3): 368-376. [ YANG Xin-yan, WEI Ru-ping, YANG Liu-yan. Research on Preparing Ceramsite From Polluted River Sediment and the Potential of the Ceramsite on Phosphorus Removal[J]. Journal of Ecology and Rural Environment, 2019, 35(3): 368-376.] (  0) 0) |
| [31] |
贺凯, 卢少勇, 金相灿, 等. 五种填料对磷酸盐的等温吸附-解吸特性[J]. 农业工程学报, 2008, 24(8): 232-235. [ HE Kai, LU Shao-yong, JIN Xiang-can, et al. Adsorption-Desorption Characteristics of Phosphate by Five Kinds of Substrates[J]. Transactions of the Chinese Society of Agricultural Engineering, 2008, 24(8): 232-235. DOI:10.3321/j.issn:1002-6819.2008.08.051] (  0) 0) |
| [32] |
赵雪松, 胡小贞, 卢少勇, 等. 不同粒径方解石在不同pH值时对磷的等温吸附特征与吸附效果[J]. 环境科学学报, 2008, 28(9): 1872-1877. [ ZHAO Xue-song, HU Xiao-zhen, LU Shao-yong, et al. Phosphorus Sorption by Natural Calcite and the Effects of pH and Grain Size[J]. Acta Scientiae Circumstantiae, 2008, 28(9): 1872-1877. DOI:10.3321/j.issn:0253-2468.2008.09.024] (  0) 0) |
| [33] |
SAYAG C, SUPPAN S, TRAWCZYN'SKI J, et al. Effect of Support Activation on the Kinetics of Indole Hydrodenitrogenation Over Mesoporous Carbon Black Composites-Supported Molybdenum Carbide[J]. Fuel Processing Technology, 2002, 77/78: 261-267. DOI:10.1016/S0378-3820(02)00038-3 (  0) 0) |



