锌是一种常见的重金属,含锌化合物通过采矿、冶炼、机械制造、造纸等工业活动进入水体环境[1-2]。水中锌含量过高时,会对水生生物造成严重毒害。而人体接触到的ρ(锌)超过0.8 mg·L-1时,就会出现免疫功能下降、休克等现象[3]。同时锌在一定程度上还会抑制水体的自净过程。因此,研究水体中锌污染的治理问题具有重要意义。含锌废水的处理方法多样,例如化学沉淀法、离子交换法及吸附法等。吸附法因其工艺流程简单、处理效果好、可操作性强等优点而被广泛利用[4-5]。
生物炭是由废弃生物质在限氧条件下热解的富含炭的吸附材料,由于其比表面积大,孔状结构发达,热稳定性好,在处理水体重金属方面具有广泛的应用前景[6]。但是,不同热解温度生物炭的理化性质及对重金属吸附特性存在较大差异[7]。郭素华等[8]以花生壳和玉米秸秆为原料,研究了3种热解温度(300、500和700 ℃)条件下生物炭对水中锌的吸附特性,发现高温制备的生物炭的灰分、pH及芳香化程度均较高,并且对Zn2+的吸附能力也较强。CIBATI等[9]研究了热解温度对芒草竹生物炭吸附锌的影响,发现600 ℃条件下热解的生物炭对Zn2+的吸附效果比350 ℃条件下更好。然而不同热解温度条件下生物炭对Zn2+的吸附机制却鲜有研究。
大部分研究以植物类农业废弃物为生物炭原料,以甲壳类食品废弃物为原料的研究很少。笔者选用龙虾壳废弃物为生物炭原料,研究不同热解温度条件下制备的生物炭理化性质差异。通过批量吸附实验研究龙虾壳生物炭对Zn2+的吸附特性,并结合表征定性分析其吸附机制,以期为龙虾壳废弃物资源的再利用及发挥龙虾壳生物炭在重金属污染治理中的作用提供理论支持。
1 材料与方法 1.1 生物炭的制备龙虾壳收集于安徽省合肥市罍街,将收集的新鲜龙虾壳头部肉质部分去除,洗净后于80 ℃烘箱烘干,磨碎置于自封袋中备用。
采用限氧升温炭化法制备生物炭:取已研磨的龙虾壳用铝箔纸密封包裹,置于马弗炉(SX2箱式马弗炉,上海锦屏)中裂解,马弗炉升温程序:先以7 ℃·mim-1升温到110 ℃保温20 min后,再以15 ℃· min-1逐渐升温至所需温度(300、400、500和600 ℃)后维持4 h,自然冷却至室温后取出。将生物炭研磨过筛,取粒径为0.25~0.85 mm的生物炭颗粒用去离子水反复清洗,于80 ℃条件下烘干备用;制得的生物炭分别标记为LS300、LS400、LS500和LS600。
1.2 生物炭的表征通过生物炭前后的质量损失计算龙虾壳生物炭的产率;按m(生物炭):V(去离子水)=1:20的比例混合振荡24 h后测定生物炭pH值[10];灰分含量测定参照GB/T 17664—1999《木炭和木炭实验方法》[11];挥发分含量测定参照GB/T 2001—2013《焦炭工业分析测定方法》[11];生物炭中C、H和N含量测定采用元素分析仪(vario ELcube,德国);生物炭的浸出毒性测定采用HJ/T 299—2007《固体废物浸出毒性浸出方法硫酸硝酸法》[12];生物炭颗粒的外貌结构及元素含量测定采用扫描电子显微镜与能谱分析仪(S-4800,日立)。
1.3 吸附实验称取0.1 g生物炭于250 mL锥形瓶中,加入50 mL的150 mg·L-1 Zn2+溶液,以去离子水为背景溶液,用0.1 mol·L-1 HNO3或NaOH调节pH为5.0±0.05,于25 ℃、180 r·min-1条件下恒温振荡24 h。同时设置空白和平行。
1.3.1 吸附动力学实验分别于0、30、60、120、240、420、600、720、1 440、2 160和2 880 min时取样,按V(Zn2+溶液):V(去离子水)=1:200比例稀释后过0.45 μm微孔滤膜,用原子吸收分光光度计(atomic absorption spectrophotometer,AAS)测定Zn2+浓度。
采用准一级动力学[13]〔式(1)〕、准二级动力学[14] 〔式(2)〕、Elovich[15]〔式(3)〕和颗粒内扩散[16]方程〔式(4)〕对生物炭吸附Zn2+的动力学行为进行拟合。
| $ {Q_t} = {Q_{\rm{e}}}\left( {1 - {{\rm{e}}^{ - {k_1}t}}} \right), $ | (1) |
| $ t/{Q_t} = 1/\left( {{k_2}Q_{\rm{e}}^2} \right) + t/{Q_{\rm{e}}}, $ | (2) |
| $ {Q_t} = (\ln ab)/b + (\ln t)/b, $ | (3) |
| $ {Q_t} = {k_{{\rm{id}}}}{t^{1/2}} + {C_i}。$ | (4) |
式(1)~(4)中,Qe为平衡吸附量,mg·g-1;Qt为t时刻吸附量,mg·g-1;t为时间,min;k1为准一级反应速率常数,min-1;k2为准二级反应速率常数,g·mg-1·min-1;a为吸附速率常数,g·mg-1·min-1;b为解吸速率常数,g·mg-1;kid为颗粒内扩散速率常数,mg·g-1·min-0.5;Ci为常数,表示生物炭边界层。
根据准二级动力学方程拟合参数可以计算初始吸附速率(h):
| $ h=k_{2} Q_{\mathrm{e}}^{2} $ |
配制初始ρ(Zn2+)为50~850 mg·L-1的溶液,生物炭投加量为2 g·L-1,待吸附平衡后取样过膜稀释测定Zn2+浓度。
利用Langmuir〔式(5)〕和Freundlich〔式(6)〕[9]等温吸附模型拟合等温吸附过程,方程如下:
| $ {Q_{\rm{e}}} = {Q_{\rm{m}}}{C_{\rm{e}}}{K_{\rm{L}}}/\left( {1 + {K_{\rm{L}}}{C_{\rm{e}}}} \right), $ | (5) |
| $ {Q_{\rm{e}}} = {K_{\rm{F}}}C_{\rm{e}}^{1/n}。$ | (6) |
式(5)~(6)中,Ce为吸附平衡浓度,mg·L-1;Qe为平衡吸附量,mg·g-1;Qm为最大吸附量,mg·g-1;KL为吸附剂对重金属离子的亲和力,L·mg-1;KF为吸附容量,mg·g-1;n为吸附强度。
1.3.3 pH影响实验在pH 2~6范围内用0.1 mol· L-1 HNO3和NaOH溶液精确调定Zn2+溶液pH,待吸附平衡后测定Zn2+溶液浓度和吸附后溶液pH值。
1.3.4 吸附机制实验利用AAS测定吸附前后生物炭中K+、Ca2+、Na+和Mg2+释放量,采用傅里叶红外光谱仪(Vertex 80- Hyperion 2000,上海)分析吸附前后生物炭表面官能团,采用X射线衍射仪(XRD,D/MAX 2500 V,日本理学制造公司)分析生物炭矿物质组成。
2 结果与讨论 2.1 生物炭的特征由表 1可知,当热解温度由300上升到600 ℃时,生物炭产率由84.81%下降到76.60%,生物炭产率较高且稳定,这可能是因为在制备过程中20 min保温措施可使龙虾壳表面缓慢炭化,内部水分缓慢蒸发,导致龙虾壳内部残留水分因快速升温而产生的生物油含量减少,从而提高产率。由于大部分挥发性物质在低温已经损失[17],所以产率较为稳定。LS600灰分含量比LS300仅增加4.14百分点,增幅较小。这可能是由于低温裂解时无机成分浓缩程度已经很高[18]。由于低温时龙虾壳热解不完全,挥发分没有完全析出,随着温度升高,部分有机质和矿物质开始析出,使生物炭挥发分减少。生物炭pH值均大于7,呈碱性,且碱性逐渐增强,这是因为高温使碱盐从热解物中释放出来[19]。在热解过程中,挥发性物质的损失带走了很多表面官能团[12],导致C、H和N含量均呈下降趋势,原子比C/H表示生物炭的芳香性,比值越大,表明芳香性越高,因此龙虾壳生物炭的芳香性随着裂解温度的升高而升高。
|
|
表 1 不同热解温度条件下龙虾壳生物炭性质比较 Table 1 Comparisions of properties between crayfish shell biochars at different temperatures |
为评估使用龙虾壳生物炭材料是否存在危险,对其重金属含量进行测定。由表 2可知,生物炭中重金属含量较低,对比GB 5085.3—2007《危险废物鉴别标准浸出毒性鉴别》,不同裂解温度生物炭中Cu、Zn、Cd、Cr、As和Ni含量均低于标准限值,其中Ni含量为痕量,这说明龙虾壳生物炭的浸出毒性属安全级别。
|
|
表 2 不同热解温度龙虾壳生物炭的浸出毒性 Table 2 Leaching toxicity of crayfish shell biochars at different temperatures |
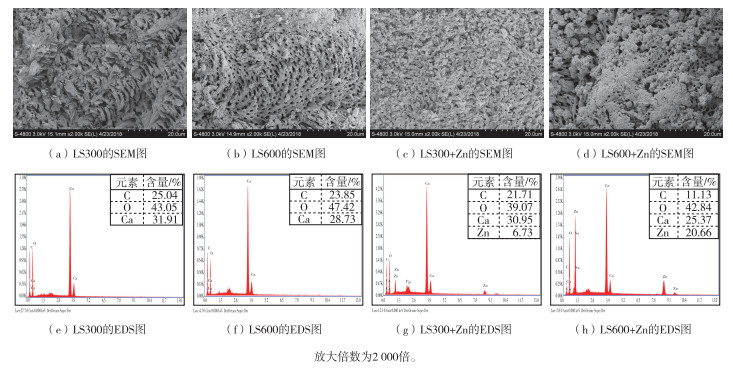
根据对生物炭性质的分析,选取特征差异较大的LS300和LS600进行SEM-EDS分析,LS300和LS600吸附Zn2+前后的SEM-EDS图见图 1,可以看出300 ℃条件下裂解的生物炭孔状结构呈长条形,孔径较小,孔隙不发达,而600 ℃条件下裂解的生物炭表面则出现明显蜂窝状孔隙结构,孔隙更密集,孔结构发育更完全。因此,LS600生物炭比表面积更大,提供的吸附位点更多。对比吸附前后的电镜能谱图可知,吸附后生物炭表面有一层明显的附着物,且表面附着的物质为含锌化合物。与吸附锌之前相比,吸附锌之后C、O和Ca含量均有减少现象。
|
图 1 LS300和LS600吸附前后的电镜能谱图 Fig. 1 SEM-EDS images of LS300 and LS600 before and after adsorption |
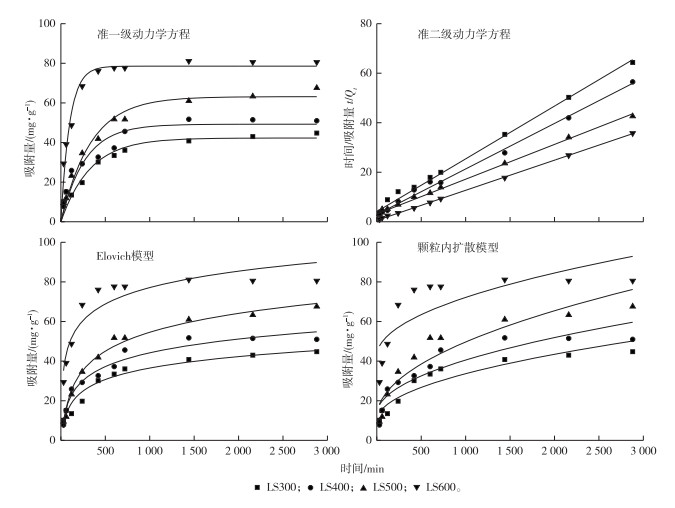
由图 2可知,LS300、LS400和LS500在吸附7 h时已经达到吸附饱和的60%以上,随着时间的增加,吸附量持续增加,但增幅下降,24 h时吸附趋于平衡。LS600在吸附2 h时就达到饱和吸附量的60%,7 h时达到吸附平衡状态。这是由于吸附初始阶段吸附剂表面有大量吸附位点,表面吸附占主导作用;待表面吸附位点达到饱和,吸附速率则取决于Zn2+从吸附剂外部进入内部位点的速度[20]。
|
图 2 龙虾壳生物炭对Zn2+的吸附动力学曲线 Fig. 2 The adsorption kinetics of Zn2+ by crayfish shell biochar |
如表 3所示,准一级动力学方程可较好地拟合Zn2+的吸附过程,其R2 > 0.9,LS600的k1值最大,说明在反应初始阶段LS600的吸附速率更快。准二级动力学方程可以更好地拟合4种生物炭对Zn2+的吸附过程,其R2值在4种拟合方程中最大,表明4种生物炭的吸附速率受化学吸附机制的控制,吸附过程包括外部液膜扩散、表面吸附和颗粒内扩散[21]。根据准二级动力学方程拟合参数可得LS300、LS400、LS500和LS600的初始吸附速率(h)分别为0.245、0.341、0.321和1.875 mg·g-1·min-1,说明LS600的吸附速率更快,这与准一级动力学方程中k1值分析结果一致。Elovich模型对4种生物炭拟合的R2 >0.9,拟合度较好,说明4种生物炭在整个吸附过程中具有均匀分布的表面吸附能[21],并且LS600的a和b值均大于LS300、LS400和LS500,说明LS600的吸附速率和解吸速率都相对较快。颗粒内扩散模型的拟合度较差,说明该模型不适用于拟合龙虾壳吸附Zn2+的过程。
|
|
表 3 龙虾壳生物炭对Zn2+的吸附动力学 Table 3 Kinetic parameters of Zn2+ adsorption by crayfish shell biochar |
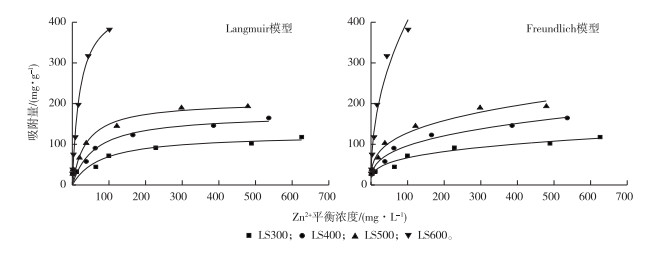
由图 3可知,LS300、LS400、LS500和LS600的吸附量均随Zn2+平衡浓度的增大而增加,最终趋于平衡。这是因为在低浓度时,生物炭表面可以为Zn2+提供足够的吸附位点,随着Zn2+浓度的增加,吸附位点饱和,吸附量不再增加。
|
图 3 龙虾壳生物炭对Zn2+的吸附等温线 Fig. 3 The adsorption isotherms of Zn2+ by crayfish shell biochar |
根据表 4,比较2种模型拟合的决定系数R2可知:Langmuir和Freundlich模型对4种生物炭吸附Zn2+的过程的拟合度均较好,而LS300、LS400和LS500的Freundlich模型拟合的R2值更大,说明这3种生物炭对Zn2+的吸附主要为多层吸附;LS600的Langmuir模型拟合的R2更大,表明LS600对Zn2+的等温吸附主要为单层吸附,吸附主要通过静电引力和氢键作用,吸附剂表面均匀同质且吸附位点之间不存在相互作用[22]。在Freundlich模型中,4种生物炭的参数1/n<1,表明这4种生物炭的吸附过程为非线性等温吸附,生物炭对Zn2+的吸附是由多种机制共同作用的。比较KF值可知,各生物炭的吸附能力由大到小依次为LS600、LS500、LS400和LS300。在Langmuir模型中,比较拟合参数Qm可知,各生物炭最大吸附量由大到小依次为LS600、LS500、LS400和LS300。参数KL表示吸附剂与吸附质的亲和力,其值越大,亲和力越强[23],因此各生物炭亲和力由大到小依次为LS600、LS500、LS400和LS300。
|
|
表 4 龙虾壳生物炭对Zn2+的吸附等温线拟合数据 Table 4 Isotherm equation parameters of Zn2+ adsorption by crayfish shell biochar |
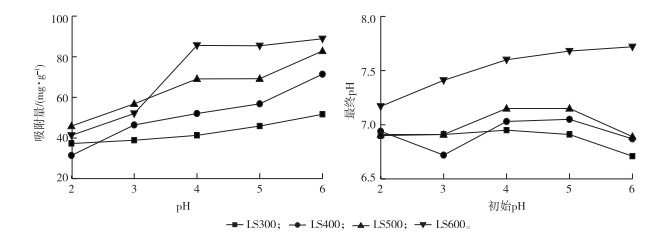
溶液初始pH是影响吸附过程的重要因素,它会影响生物炭表面电荷和重金属的赋存形态。当pH<7时,溶液中Zn以Zn2+形态存在[24],所以选取pH的范围为2~6。由图 4可知,LS300、LS400、LS500和LS600对Zn2+的吸附量与pH值呈正相关,当pH=2时,溶液中H+浓度较高,H+与Zn2+会竞争龙虾壳生物炭表面的吸附位点,从而阻碍Zn2+吸附;当pH值为4和5时,4种生物炭对Zn2+的吸附量基本保持不变,这与JIANG等[24]研究中溶液初始pH对软木与硬木生物炭吸附铜与锌的影响所得结果一致;当pH为6时,吸附量又呈明显上升趋势,这是因为当pH > 5时,溶液中OH-逐渐增多,Zn2+与OH-以氢氧化物形式存在,促进了Zn2+的沉淀,所以吸附量又呈上升趋势。
|
图 4 pH对生物炭吸附Zn2+的影响 Fig. 4 Effects of pH on Zn2+ adsorption by crayfish shell biochar |
由于不同裂解温度生物炭具有不同的碱度,所以吸附后生物炭溶液的平衡pH值有着不同程度的增加。由图 4可知,LS600的平衡pH值明显高于其他3种生物炭,说明LS600碱度更大,这与生物炭的pH值测定结果一致。
2.3.4 不同原料生物炭特征的比较根据表 5[6, 11, 25-26],在相似热解条件下,龙虾壳生物炭与牛粪源蚓粪生物炭的特征较为相似,不同原料生物炭间pH值及H、N含量差异不大,生物炭均呈碱性,且H、N含量均较低。与水稻秸秆等植物类生物炭相比,龙虾壳生物炭C含量较低,但灰分含量较高,灰分主要由无机成分和矿物质组成,在生物炭作为吸附剂方面起着主要作用。因此,龙虾壳生物炭在固定碳的能力方面较弱,但含有更多的矿物质,所以更适合作吸附剂材料。此外,与其他原料生物炭相比,龙虾壳生物炭H/C比值更小,说明龙虾壳生物炭的芳香结构更加完备。根据表 6[3, 8-9],比较龙虾壳生物炭与其他生物炭对锌的最大吸附量可知,龙虾壳生物炭对锌的吸附量高于许多其他吸附材料,这可能与龙虾壳生物炭含有大量矿物质有关。因此,龙虾壳生物炭对锌的吸附能力更强。
|
|
表 5 不同原料生物炭特征的比较 Table 5 Comparison of biochar properties of different raw materials |
|
|
表 6 不同吸附剂对Zn2+最大吸附量(Qm)的比较 Table 6 Comparison of the maximum Zn2+ adsorption capacity of various adsorbents |
综上,龙虾壳生物炭C含量较低,但矿物质成分含量较高,芳香结构较完备。与其他生物炭材料相比,龙虾壳生物炭固定碳的能力较弱,但吸附重金属能力较强。因此,龙虾壳生物炭更适合作为吸附材料使用。
2.4 龙虾壳生物炭对Zn2+的吸附机制生物炭吸附重金属主要涉及4种机制:(1)与阳离子(K+、Ca2+、Na+和Mg2+)的交换;(2)与矿物质成分的沉淀;(3)与官能团的络合;(4)与π电子的配位[27]。为进一步探索热解温度对Zn2+吸附机制的影响,根据动力学及等温吸附实验结论选取吸附效果差异最大的LS300和LS600进行吸附机制分析。
2.4.1 阳离子交换生物炭中阳离子(K+、Ca2+、Na+和Mg2+)主要通过静电引力及与生物炭中含氧官能团络合作用存在,这些阳离子可与溶液中Zn2+发生静电阳离子交换或金属置换反应。为进一步探讨阳离子交换机制,测定了LS300和LS600吸附Zn2+前后溶液中阳离子释放量。
如表 7所示,低温热解生物炭LS300释放的K+、Ca2+、Na+和Mg2+比高温热解LS600释放的多,这可能是在高温条件下形成矿物结晶所致[28]。比较吸附前后阳离子的变化,发现吸附Zn2+后生物炭释放的K+、Ca2+、Na+和Mg2+含量比吸附前有明显增加,这说明龙虾壳生物炭在吸附过程中Zn2+与阳离子发生了交换作用。LS300和LS600的实际吸附量分别为40.81和81.11 mg·g-1,通过阳离子交换的增量与实际吸附量的比值可得到LS300和LS600在吸附Zn2+过程中阳离子交换量对总吸附的贡献比分别为58.93%和76.23%。由此可见,阳离子交换作用是龙虾壳生物炭吸附机制的主导作用,并且随着热解温度的升高,阳离子交换作用对吸附的贡献也在不断增加。
|
|
表 7 生物炭释放到Zn2+溶液中的K+、Ca2+、Na+和Mg2+量 Table 7 The amount of K+, Ca2+, Na+, Mg2+ released from biochars into Zn2+ sorption solutions |
LS300、LS600吸附Zn2+前后红外光谱图和XRD图见图 5。
|
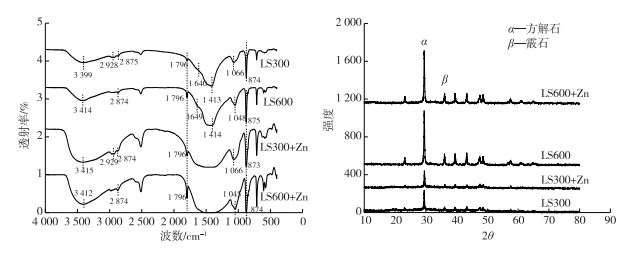
图 5 LS300、LS600吸附Zn2+前后红外光谱图和XRD图 Fig. 5 FTIR spectra and XRD of LS300, LS600 before and after adsorption of Zn2+ |
由图 5可知,LS300和LS600在1 465~1 340 cm-1处的宽峰为碳酸盐中的C=O和C—O伸缩振动[6],吸附后,LS300+Zn和LS600+Zn的碳酸盐中C=O和C—O伸缩振动峰均有明显变宽现象。这可能是因为Zn2+与碳酸盐形成了沉淀。同时,从XRD图可看出龙虾壳生物炭的主要成分是存在于方解石和霰石中的CaCO3,并且对比吸附前后的XRD图,发现仅在峰值强度上产生了轻微变化。这说明沉淀作用对龙虾壳生物炭吸附Zn2+的贡献较小。XIAO等[29]在小龙虾壳生物炭对Pb2+的吸附研究中也得出相似结论。此外,高温热解生物炭的难溶碳酸盐含量较高,不利于对Zn2+的吸附,致使沉淀作用对高温热解生物炭吸附的贡献也更小[20]。
2.4.3 官能团络合及与π电子的配位由图 5可知,LS300和LS600分别在3 399和3 414 cm-1处表现出明显的醇类与酚类分子间氢键O—H伸缩振动峰。LS300在2 875、2 928 cm-1处的2个峰值分别为—CH3对称伸缩振动峰和—CH2—不对称伸缩振动峰,LS600只有在2 874 cm-1处的—CH3对称伸缩振动峰,而没有—CH2—吸收峰,这可能是由于炭化过程将—CH2—转变为挥发分或固定碳[6];在1 796 cm-1处的吸收峰是由于环酸酐的C=O对称伸缩振动引起的。在1 680~1 610 cm-1处为烯烃的C=C振动伸缩峰。LS300在1 066 cm-1处的吸收峰为酸酐的C—O伸缩振动峰,LS600在1 048 cm-1处的吸收峰为醇类的C—O伸缩振动峰;LS300和LS600分别在874、875 cm-1处的吸收峰为芳环C—H弯曲振动峰[25]。
吸附后,LS300+Zn的O—H伸缩振动峰移至3 415 cm-1处,—CH3的对称伸缩振动峰偏移至2 874 cm-1处,且—CH2—的不对称伸缩振动峰移至2 929 cm-1处,C—H振动峰移至873 cm-1处。LS600+ Zn的O—H伸缩振动峰移至3 412 cm-1处,C—O伸缩振动峰移至1 045 cm-1处,C—H振动峰移至874 cm-1处。这说明在LS300吸附Zn2+过程中醇类和酚类的—OH、饱和烃和芳环的C—H参与了反应;LS600吸附Zn2+过程中醇类和酚类的—OH、芳环的C—H及醇类的C—O参与了反应。由此可见,热解温度不同,参与吸附过程的官能团种类也不同。LS300+Zn和LS600+Zn在1 680~1 610 cm-1处C=C伸缩振动峰有明显变宽现象,这可能是因为Zn2+与C=C双键中的π键发生了配位作用。因此,龙虾壳生物炭吸附Zn2+的过程中存在Zn2+与官能团的络合作用及与C=C双键中π键的配位作用。另外,热解温度越高,生物炭的芳香性越强,π电子的配位作用也越大,说明π电子配位作用对高温热解生物炭吸附的贡献更大[30]。
3 结论(1)随着热解温度的升高,生物炭产率下降,灰分含量和pH值升高,C、H和N含量降低,芳香性增强。
(2)4种生物炭对Zn2+的吸附动力学曲线更符合准二级动力学方程,吸附速率受化学吸附机制的控制,LS600对Zn2+吸附最快到达平衡。
(3)LS300、LS400和LS500的等温吸附曲线更符合Freundlich模型,LS600更符合Langmuir模型。热解温度越高,生物炭对Zn2+的吸附能力、吸附量和亲和力就越大。
(4)生物炭对Zn2+的吸附机制为多机制共同作用,主要包括阳离子交换、官能团络合、与π电子的配位及沉淀作用。
(5)阳离子交换作用是龙虾壳生物炭对Zn2+吸附机制的主导作用,并且随着热解温度的升高,阳离子交换和π电子的配位作用对吸附的贡献增加。
| [1] |
LI H B, DONG X L, DA SILVA E B, et al. Mechanisms of Metal Sorption by Biochars:Biochar Characteristics and Modifications[J]. Chemosphere, 2017, 178: 466-478. DOI:10.1016/j.chemosphere.2017.03.072 (  0) 0) |
| [2] |
ZHANG H Y, YUE X P, LI F, et al. Preparation of Rice Straw-Derived Biochar for Efficient Cadmium Removal by Modification of Oxygen-Containing Functional Groups[J]. Science of the Total Environment, 2018, 631: 795-802. (  0) 0) |
| [3] |
KHAN T A, MUKHLIF A A, KHAN E A. Uptake of Cu2+ and Zn2+ From Simulated Wastewater Using Muskmelon Peel Biochar:Isotherm and Kinetic Studies[J]. Egyptian Journal of Basic and Applied Sciences, 2017, 4(3): 236-248. DOI:10.1016/j.ejbas.2017.06.006 (  0) 0) |
| [4] |
周菁菁.茶叶对废水中铅锌镉离子的吸附性能研究[D].长沙: 湖南大学, 2013. [ZHOU Jing-jing.Adsorption of Lead, Zinc, and Cadmium Ions From Aqueous Solution by Teawaste Adsorbents[D].Changsha: Hunan University, 2013.] http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2357156
(  0) 0) |
| [5] |
CIESIELCZYK F, BARTCZAK P, JESIONOWSKI T. Removal of Cadmium(Ⅱ)and Lead(Ⅱ)Ions From Model Aqueous Solutions Using Sol-Gel-Derived Inorganic Oxide Adsorbent[J]. Adsorption, 2016, 22(4/5/6): 445-458. (  0) 0) |
| [6] |
杜文慧, 朱维琴, 潘晓慧, 等. 牛粪源蚓粪及其生物炭对Pb2+, Cd2+的吸附特性[J]. 环境科学, 2017, 38(5): 2172-2181. [ DU Wen-hui, ZHU Wei-qin, PAN Xiao-hui, et al. Adsorption of Pb2+, Cd2+ From Aqueous Solution Using Vermicompost Derived From Cow Manure and Its Biochar[J]. Environmental Science, 2017, 38(5): 2172-2181.] (  0) 0) |
| [7] |
郑凯琪, 王俊超, 刘姝彤, 等. 不同热解温度污泥生物炭对Pb2+、Cd2+的吸附特性[J]. 环境工程学报, 2016, 10(12): 7277-7282. [ ZHENG Kai-qi, WANG Jun-chao, LIU Shu-tong, et al. Adsorption Characteristic of Pb2+ and Cd2+ With Sludge Biochars Derived at Different Pyrolysis Temperatures[J]. Chinese Journal of Environmental Engineering, 2016, 10(12): 7277-7282. DOI:10.12030/j.cjee.201507083] (  0) 0) |
| [8] |
郭素华, 许中坚, 李方文, 等. 生物炭对水中Pb(Ⅱ)和Zn(Ⅱ)的吸附特征[J]. 环境工程学报, 2015, 9(7): 3215-3222. [ GUO Su-hua, XU Zhong-jian, LI Fang-wen, et al. Adsorption of Pb(Ⅱ), and Zn(Ⅱ)From Aqueous Solution by Biochars[J]. Chinese Journal of Environmental Engineering, 2015, 9(7): 3215-3222.] (  0) 0) |
| [9] |
CIBATI A, FOEREID B, BISSESSUR A, et al. Assessment of Miscanthus giganteus Derived Biochar as Copper and Zinc Adsorbent:Study of the Effect of Pyrolysis Temperature, pH and Hydrogen Peroxide Modification[J]. Journal of Cleaner Production, 2017, 162: 1285-1296. DOI:10.1016/j.jclepro.2017.06.114 (  0) 0) |
| [10] |
QI F J, YAN Y B, LAMB D, et al. Thermal Stability of Biochar and Its Effects on Cadmium Sorption Capacity[J]. Bioresource Technology, 2017, 246: 48-56. DOI:10.1016/j.biortech.2017.07.033 (  0) 0) |
| [11] |
简敏菲, 高凯芳, 余厚平. 不同裂解温度对水稻秸秆制备生物炭及其特性的影响[J]. 环境科学学报, 2016, 36(5): 1757-1765. [ JIAN Min-fei, GAO Kai-fang, YU Hou-ping. Effects of Different Pyrolysis Temperatures on the Preparation and Characteristics of Biochar From Rice Straw[J]. Acta Scientiae Circumstantiae, 2016, 36(5): 1757-1765.] (  0) 0) |
| [12] |
CHEN T, ZHANG Y X, WANG H T, et al. Influence of Pyrolysis Temperature on Characteristics and Heavy Metal Adsorptive Per-formance of Biochar Derived From Municipal Sewage Sludge[J]. Bioresource Technology, 2014, 164: 47-54. DOI:10.1016/j.biortech.2014.04.048 (  0) 0) |
| [13] |
CHEN Y Y, WANG B Y, XIN J, et al. Adsorption Behavior and Mechanism of Cr(Ⅵ)by Modified Biochar Derived From Enteromorpha prolifera[J]. Ecotoxicology and Environmental Safety, 2018, 164: 440-447. DOI:10.1016/j.ecoenv.2018.08.024 (  0) 0) |
| [14] |
HO Y S, MCKAY G. Pseudo-Second Order Model for Sorption Processes[J]. Process Biochemistry, 1999, 34(5): 451-465. DOI:10.1016/S0032-9592(98)00112-5 (  0) 0) |
| [15] |
MCLINTOCK I S. The Elovich Equation in Chemisorption Kinetics[J]. Nature, 1967, 216: 1204-1205. DOI:10.1038/2161204a0 (  0) 0) |
| [16] |
MORRIS J C, WEBER W J Jr.Removal of Biologically-Resistant Pollutant From Waste Water by Adsorption[M]//Advances in Water Pollution Research.s.l.: [s.n., 1964: 231-266.DOI: 10.1016/B978-1-4832-8391-3.50032-4.
(  0) 0) |
| [17] |
陈友媛, 惠红霞, 卢爽, 等. 浒苔生物炭的特征及其对Cr(Ⅵ)的吸附特点和吸附机制[J]. 环境科学, 2017, 38(9): 3953-3961. [ CHEN You-yuan, HUI Hong-xia, LU Shuang, et al. Characteristics of Enteromorpha Prolifera Biochars and Their Adsorption Performance and Mechanisms for Cr(Ⅵ)[J]. Environmental Science, 2017, 38(9): 3953-3961.] (  0) 0) |
| [18] |
ZHANG W H, MAO S Y, CHEN H, et al. Pb(Ⅱ)and Cr(Ⅵ) Sorption by Biochars Pyrolyzed From the Municipal Wastewater Sludge Under Different Heating Conditions[J]. Bioresource Technology, 2013, 147(9): 545-552. (  0) 0) |
| [19] |
CHEN X C, CHEN G C, CHEN L G, et al. Adsorption of Copper and Zinc by Biochars Produced From Pyrolysis of Hardwood and Corn Straw in Aqueous Solution[J]. Bioresource Technology, 2011, 102(19): 8877-8884. DOI:10.1016/j.biortech.2011.06.078 (  0) 0) |
| [20] |
申磊, 荆延德, 孙小银, 等. 动植物来源生物炭对水体中Cd2+的吸附特性[J]. 生态与农村环境学报, 2018, 34(4): 363-370. [ SHEN Lei, JING Yan-de, SUN Xiao-yin, et al. Cd2+ Adsorption Characteristics of Animal-Waste-and-Plant-Derived Biochars in Water[J]. Journal of Ecology and Rural Environment, 2018, 34(4): 363-370.] (  0) 0) |
| [21] |
常春, 王胜利, 郭景阳, 等. 不同热解条件下合成生物炭对铜离子的吸附动力学研究[J]. 环境科学学报, 2016, 36(7): 2491-2502. [ CHANG Chun, WANG Sheng-li, GUO Jing-yang, et al. Adsorption Kinetics and Mechanism of Copper Ion on Biochar With Different Pyrolysis Condition[J]. Acta Scientiae Circumstantiae, 2016, 36(7): 2491-2502.] (  0) 0) |
| [22] |
王章鸿, 郭海艳, 沈飞, 等. 蚯蚓粪便制备生物炭及其对罗丹明B吸附的研究[J]. 环境科学学报, 2015, 35(10): 3170-3177. [ WANG Zhang-hong, GUO Hai-yan, SHEN Fei, et al. Production of Biochar by Vermicompost Carbonization and Its Adsorption to Rhodamine-B[J]. Acta Scientiae Circumstantiae, 2015, 35(10): 3170-3177.] (  0) 0) |
| [23] |
YAO W, ZHU W Q, ZHAN Y N, et al. Adsorption of Cu(Ⅱ)and Zn(Ⅱ)Ions by Solidified Landfilled Sludge and Its Pyrolyzed Produce[J]. Advanced Materials Research, 2014, 955/956/957/958/959: 2629-2634. (  0) 0) |
| [24] |
JIANG S S, HUANG L B, NGUYEN T A H, et al. Copper and Zinc Adsorption by Softwood and Hardwood Biochars Under Elevated Sulphate-Induced Salinity and Acidic pH Conditions[J]. Chemosphere, 2016, 142: 64-71. DOI:10.1016/j.chemosphere.2015.06.079 (  0) 0) |
| [25] |
邓金环, 郜礼阳, 周皖婉, 等. 不同温度制备香根草生物炭对Cd2+的吸附特性与机制[J]. 农业环境科学学报, 2018, 37(2): 340-349. [ DENG Jin-huan, GAO Li-yang, ZHOU Wan-wan, et al. Adsorption Characteristics and Mechanisms of Cd2+ in Biochar Derived From Vetiver Grass Under Different Pyrolysis Temperatures[J]. Journal of Agro-Environment Science, 2018, 37(2): 340-349.] (  0) 0) |
| [26] |
郜礼阳, 邓金环, 唐国强, 等. 不同温度桉树叶生物炭对Cd2+的吸附特性及机制[J]. 中国环境科学, 2018, 38(3): 1001-1009. [ GAO Li-yang, DENG Jin-huan, TANG Guo-qiang, et al. Adsorption Characteristics and Mechanism of Cd2+ on Biochar With Different Pyrolysis Temperatures Produced From Eucalyptus Leaves[J]. China Environmental Science, 2018, 38(3): 1001-1009. DOI:10.3969/j.issn.1000-6923.2018.03.025] (  0) 0) |
| [27] |
WANG R Z, HUANG D L, LIU Y G, et al. Investigating the Adsorption Behavior and the Relative Distribution of Cd2+ Sorption Mechanisms on Biochars by Different Feedstock[J]. Bioresource Technology, 2018, 261: 265-271. DOI:10.1016/j.biortech.2018.04.032 (  0) 0) |
| [28] |
WANG Z Y, LIU G C, ZHENG H, et al. Investigating the Mechanisms of Biochar's Removal of Lead From Solution[J]. Bioresource Technology, 2015, 177: 308-317. DOI:10.1016/j.biortech.2014.11.077 (  0) 0) |
| [29] |
XIAO Y L, XUE Y W, GAO F, et al. Sorption of Heavy Metal Ions Onto Crayfish Shell Biochar:Effect of Pyrolysis Temperature, pH and Ionic Strength[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 80: 114-121. DOI:10.1016/j.jtice.2017.08.035 (  0) 0) |
| [30] |
UCHIMIYA M, LIMA I M, THOMAS-KLASSON K, et al. Immobilization of Heavy Metal Ions(CuⅡ, CdⅡ, NiⅡ, and PbⅡ)by Broiler Litter-Derived Biochars in Water and Soil[J]. Journal of Agricultural and Food Chemistry, 2010, 58(9): 5538-5544. DOI:10.1021/jf9044217 (  0) 0) |




