2. 鄞州区农业技术服务站, 浙江 宁波 315100;
3. 慈溪市农业监测中心, 浙江 宁波 315300;
4. 浙江省农业科学院环境资源与土壤肥料研究所, 浙江 杭州 310021
2. Agricultural Techniques Extension Server Station of Yinzhou District, Ningbo 315100, China;
3. Agricultural Monitoring Center of Cixi City, Ningbo 315300, China;
4. Institute of Environment, Resources, Soil and Fertilizers, Zhejiang Academy of Agricultural Sciences, Hangzhou 310021, China
土壤微生物群落是土壤生态系统最为重要和活跃的功能组分,在驱动土壤有机质分解、养分循环等方面有着重要作用[1]。由于对土壤环境条件变化敏感,土壤微生物群落功能多样性也常被用作评价土壤质量和健康状况的重要生物学指标[2-4]。随着土壤微生物研究方法的发展,许多新技术被引入土壤微生物群落功能多样性研究中,其中MicroRespTM技术是一种基于土壤微生物代谢功能研究土壤微生物生态的方法,因其测定具有简单、灵敏和快捷等优点而被越来越多地应用于土壤微生物群落功能多样性研究[5-6]。
施肥是农业中最为重要和普遍的增产手段,不同施肥方式不仅影响土壤养分循环和土壤肥力,对土壤微生物活性、群落结构及功能多样性也会产生影响。有研究表明不同施肥条件下土壤酶活性和微生物群落功能多样性的差异较大,土壤脲酶和脱氢酶活性可作为土壤肥力的指标[7]。罗希茜等[8]研究结果表明,不同施肥对土壤微生物功能多样性产生不同影响,从而影响土壤有机质中碳、氮含量。虽然土壤生态功能变化和微生物群落响应正逐渐成为施肥方式研究的热点,但以往研究主要集中在土壤生物碳、土壤酶和土壤理化性质等方面[9-11],对于长期定位观测不同施肥方式对土壤微生物群落功能特性的影响关注较少。笔者基于5 a定位试验,采用MicroRespTM技术研究长期施用有机肥、沼液肥和化肥配施有机肥或沼液肥等不同施肥方式下土壤微生物代谢功能差异,旨在探索不同施肥方式对土壤微生物群落功能的影响,为当地选择适宜的施肥模式来提高耕地土壤质量和实现耕地永续利用提供理论依据。
1 材料与方法 1.1 试验区概况试验区设在东吴镇生态农业园(29°49′48.8″ N,121°43′53.5″ E),位于鄞州区东部水网平原,属亚热带季风性湿润气候区,因濒临东海而且有海洋性气候特征。该地区年均日照2 070 h,年均太阳辐射461.4 kJ·cm-2,年均温度16.2 ℃。该地区年均降水量1 538.8 mm,年均雨日174 d,年均相对湿度82.4%[12]。试验点地势平坦,常年种植单季水稻。供试田块土壤类型为脱潜水稻土,黄黏田亚类,青紫泥田土种,质地为壤土。试验前耕层土壤pH值为5.33,w(有机质)为11.2 g·kg-1,w(碱解氮)、w(有效磷)和w(速效钾)分别为13.8、2.27和48.6 mg·kg-1。
1.2 试验设计于2011年在园区设置不同施肥方式的5 a连续定位试验点,共设6个处理:不施肥对照(CK)、纯化肥(NPK)、纯有机肥(HOM)、中量有机肥+化肥(MOM)、纯沼液肥(HBS)和中量沼液肥+化肥(MBS)。各处理施肥方式见表 1,其中纯化肥区施肥量(N、P2O5和K2O用量分别为249、63和13 kg·hm-2·a-1)按测土配方施肥法确定,纯有机肥区和纯沼液肥区施肥量按当地习惯施肥确定,中量肥区施肥用量减半。各处理面积为666.7 m2,不设重复。
|
|
表 1 各处理施肥方式 Table 1 Design of fertilization system |
供试化肥为当地农资市场优品肥料,有机肥为当地生产的猪粪源商品有机肥,沼液肥由附近猪粪源沼气工程物流配送。所投入有机肥和沼液肥氮磷钾养分和重金属含量及其年带入量见表 2~3,商品有机肥料符合NY 525—2012《有机肥料》的重金属限量,沼液肥在国内尚无相应重金属限量标准。参照GB 5084—2005《农田灌溉水质标准》,部分年份沼液肥镉、铜和锌含量超标。
|
|
表 2 有机肥和沼液肥的pH值和氮磷钾养分含量 Table 2 pH value and nitrogen, phosphorus and potassium content of organic manure and biogas slurry manure |
|
|
表 3 有机肥和沼液肥重金属残留量及年带入量 Table 3 The residual concentration of heavy metals in organic manure and biogas slurry manure and the annual input of heavy metals into soil |
于2015年12月单季稻收获后按“S”形分别使用约5 cm孔径取土器采集各处理0~20 cm耕层土样,采集时每10点混合组成一个代表土样,每个处理采集3个代表土样,6个处理共采集18个代表土样装入塑封袋并置于冰块上带回实验室。新鲜土样剔除动植物残体后,过2 mm孔径筛,4 ℃条件下冷藏保存,1周内完成MicroRespTM分析。具体取样方法执行NY/T 1121.1—2006《土壤检测第1部分:土壤样品的采集、处理和贮存》[13]。
1.4 分析方法采用MicroRespTM方法进行土壤微生物群落功能分析。MicroRespTM是一种基于土壤微生物代谢功能反映土壤微生物群落的测定方法,利用土壤在不同碳源诱导下的CO2产生情况来表征原位土壤微生物群落水平的生理特征[14]。操作步骤如下:
(1) 预培养活化微生物:根据土壤含水率,将4 ℃条件下冷藏保存的土壤样品湿度调至20%~30%,均匀称取50 g至烧杯中,25 ℃条件下密封预培养4 d。
(2) 检测微孔板制备:将甲酚红(12.5 mg·L-1)、氯化钾(150 mmol·L-1)和碳酸氢钠(2.5 mmol·L-1)混合形成的指示剂,溶解在0.03 g·mL-1纯化琼脂(sigma)中,混合均匀后取150 μL指示琼脂填加到检测板微孔中,配制好的检测板存放在含有湿巾和碱石灰的避光干燥器皿中待用,以防变干或与空气中的CO2反应。
(3) 检测:将待测土样均匀填加到96孔深孔板中,并在每个深孔板中按照一定顺序添加16种碳源底物:水、L-丙氨酸、L-阿拉伯糖、精氨酸、半胱氨酸盐酸盐、柠檬酸、D-果糖、D-半乳糖、D-葡萄糖、γ-氨基丁酸、L-赖氨酸、L-苹果酸、N-乙酰葡糖胺、草酸、原儿茶酸和海藻糖分别为0、30、30、30、30、30、30、30、30、30、30、30、7.5、30、7.5和30 mg·g-1。将检测板倒扣在深孔板上,用专用夹子固定,在25 ℃条件下培养6 h。在酶标仪570 nm波长下测定检测板在土样培养前及培养6 h后的吸光值,利用吸光值变化计算CO2产生率(%)。
CO2产生率和吸光值通用标准化计算公式[15]为
| $ {A_i} = ({A_t}_6/{A_t}_0) \times {{\bar A}_{t\;0}}, $ | (1) |
| $ {\rho _{{\rm{C}}{{\rm{O}}_{\rm{2}}}}} = a + b/(1 + d \times {A_i}), $ | (2) |
| $ \begin{array}{l} {W_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}} = {\rm{ }}({\rho _{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}/100) \times L \times \left( {44/22.4} \right) \times \\ \;\;\;\;\;\;\;\;\;\;\left( {12/44} \right) \times [273/(273 + T)]/(W \times U)/t。\end{array} $ | (3) |
式(1)~(3)中,Ai为吸光值;At6为检测板在培养6 h后的吸光值;At0为培养初始(0 h)吸光值;At0为96孔检测板所有孔At0的平均值;ρCO2为CO2释放浓度,%;a=-0.226 5,b=-1.606,d=-6.771;WCO2为CO2产生率, μg·g-1·h-1;L为检测板孔体积,为945 μL;T为培养温度,为25 ℃;W为土壤鲜重,g;U为土壤含水率,%;t为培养时间,为6 h。
1.5 数据处理Shannon-Wiener多样性指数、Shannon-Wiener均匀度指数和Simpson多样性指数是表征土壤微生物群落多样性常用指数,不同的多样性指数可以表征土壤微生物多样性的不同方面。Shannon-Wiener多样性指数能反映土壤微生物群落利用碳源类型的多与少,即功能多样性,指数值越高,表明该系统土壤微生物群落功能多样性越高。Shannon-Wiener均匀度指数可度量群落物种均一性,均匀度指数越大,种类之间个体分配越均匀,生物多样性就越高[16]。Simpson多样性指数也可用于判断群落多样性,群落中物种越多, 各个体分配越均匀,Simpson指数就越高,群落多样性也越高[17]。Shannon-Wiener物种丰富度指数、Shannon-Wiener均匀度指数和Simpson多样性指数计算方法参照文献[18]。
试验数据采用Excel 2004和SPSS 15.0软件处理,差异显著性分析采用单因素方差分析(One-way ANOVA)和最小显著差法(LSD),作图采用SigmaPlot 10.0软件,聚类分析采用SPSS 15.0软件。
2 结果与讨论 2.1 不同施肥方式下土壤理化性质和重金属累积5 a不同施肥方式下土壤理化性质和重金属残留情况见表 4。从土壤理化性质上看,有机肥处理(HOM和MOM)和沼液处理(HBS和MBS)土壤pH值、有机质含量和氮磷养分含量有明显提高,但沼液提高效果不如有机肥,此与以往研究报道[17]基本一致。从重金属残留上看,与CK土壤相比,沼液处理(HBS和MBS)土壤重金属含量无明显变化,表明该施肥方式没有明显造成土壤重金属累积;而有机肥处理(HOM和MOM)除土壤Hg、As、Pb、Cd、Cr和Ni含量较CK无明显变化外,Cu和Zn含量有显著增加(P < 0.05),且HOM处理少量土样Zn含量少量超标(标准限值为200 mg·kg-1)[19]。这与各施肥方式的重金属年带入量有关,有机肥处理重金属年带入量明显较沼液处理高,但各处理土壤重金属累积量基本在限值内。
|
|
表 4 不同施肥方式下土壤理化性质和重金属残留量 Table 4 Soil properties and heavy metal residues under different fertilization regimes |
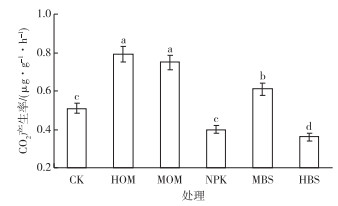
土壤微生物基础呼吸CO2产生率表征土壤微生物群落对碳源底物的利用能力,是反映土壤微生物代谢活性的有效指标。MicroRespTM测定结果显示,CK、HOM、MOM、NPK、MBS和HBS处理CO2产生率分别为0.51、0.79、0.75、0.4、0.61和0.36 μg·g-1·h-1(图 1)。除HBS处理外,其他处理土壤呼吸强度均高于或显著高于CK和NPK。可见,不同施肥方式对土壤微生物代谢活性产生明显差异。其中,施用有机肥或有机肥、沼液肥配施化肥可促进土壤呼吸作用。这与文献[9-11]的研究结果相近。分析认为,适量施用有机肥或沼液肥能增加土壤有机碳含量,进而通过提高土壤微生物生物量及活性增强土壤呼吸强度。也有研究[20]指出,重金属对土壤基础呼吸作用存在浓度效应,重金属胁迫可刺激土壤CO2释放,尤其是Cu和Zn。该研究中有机肥施用后土壤Cu和Zn含量明显增加也支持了这一论点。此外,长期高量施用沼液肥导致土壤呼吸降低,表明该施肥方式对土壤微生物代谢活动具有抑制作用,这可能是由于长期施用大量单一沼液使土壤微域环境发生改变,从而对土壤微生物适宜性造成影响,致使土壤微生物代谢活性下降。
|
图 1 不同施肥处理对土壤平均CO2产生率的影响 Figure 1 Effects of different fertilization treatments on the average production rate of soil CO2 CK为对照处理,NPK为纯化肥处理,HOM为纯有机肥处理,MOM为中量有机肥+化肥处理,HBS为纯沼液肥处理,MBS为中量沼液肥+化肥处理。直方柱上方英文小写字母不同表示不同处理间CO2产生率差异显著(P < 0.05)。 |
不同施肥方式下Shannon-Wiener多样性指数、Shannon-Wiener均匀度指数和Simpson多样性指数见表 5。各处理Shannon-Wiener多样性指数和均匀度指数变化趋势表现一致,由大到小依次均为MOM、NPK、CK、HOM、MBS和HBS处理。经差异显著性分析,HOM、MOM和NPK处理与CK无显著差异(P>0.05),而HBS处理显著低于CK(P < 0.05)。此外,从Simpson多样性指数上看,HBS处理也显著低于CK及其他处理(P < 0.05)。可见,不同施肥方式对土壤微生物群落功能多样性影响也有所不同。首先,MOM和NPK处理3种指数均较大,表明有机肥配施化肥和氮磷钾配合施肥的土壤微生物种类较多,分布较均匀,且对碳源利用程度也较高。这与张逸飞等[7]和孙瑞等[21]的研究结果类似。分析认为这是由于有机肥和矿物质肥料本身为土壤微生物提供了较多营养物质,有利于土壤微生物均衡生长,提高物种丰富度和优势度[22]。其次,该研究中HBS处理各指数均最低,这与李轶等[23]研究发现单施沼液会降低土壤微生物群落多样性的结果吻合,这可能是由于长期单一施用沼液会促进某些微生物种群生长代谢,但对其他微生物种群生长代谢产生抑制作用,致使土壤微生物群落多样性下降。
|
|
表 5 不同施肥方式下土壤微生物群落功能多样性指数 Table 5 Functional diversity indices of the soil microbial communities under different fertilization regimes |
为探讨不同施肥方式土壤微生物群落代谢结构变化,对不同碳源底物呼吸速率数据进行聚类分析。如图 2所示,6个处理可分为2个聚类簇,HOM和MOM处理土壤微生物群落代谢结构相似度较高,聚为一簇(聚类簇1),其余处理聚为另一簇(聚类簇2)。进一步分析聚类簇2中各处理发现,MBS处理与其他处理的距离较大,表现出较不同的土壤微生物群落代谢结构特征;而HBS和NPK处理土壤微生物群落代谢结构相似度较高,可以推测沼液肥和化肥对土壤微生物群落代谢存在交互影响。综上可知,相较于化肥和沼液肥,有机肥对土壤微生物群落代谢结构的影响更大,这可能与施用有机肥后土壤养分发生变化有关。BAUSENWEIN等[24]认为微生物群落结构主要受有机质调控。WAKELIN等[25]研究也发现微生物群落结构改变与碳、氮、钾和钠有关。该研究中施用有机肥后土壤有机质和氮钾养分含量明显提高也支持了这一论点。

|
图 2 不同施肥方式下土壤微生物群落代谢结构的分层聚类分析 Figure 2 Hierarchical cluster analysis of the metabolic structure of soil microbial community under different fertilization regimes CK1~3为对照处理3个样本,NPK1~3为纯化肥处理3个样本,HOM1~3为纯有机肥处理3个样本,MOM1~3为中量有机肥+化肥处理3个样本,HBS1~3为纯沼液肥处理3个样本,MBS1~3为中量沼液肥+化肥处理3个样本。 |
通过将土壤理化性质及重金属因子与土壤微生物代谢活性及群落多样性进行相关分析(表 6)发现,土壤理化性质(除全氮、全钾外)和重金属总残留量分别与土壤微生物呼吸速率呈极显著或显著正相关,其中以土壤pH值及全盐量、全磷、Cu和Zn含量与土壤微生物呼吸作用的关系最密切,相关性较高(R2>0.7)。此外,各土壤理化因素和重金属因子中,仅有土壤Cr含量与Shannon-Wiener多样性指数呈显著正相关,但相关性不高(R2=0.569),表明在较低浓度范围内提高土壤Cr含量水平可能增加土壤微生物群落类型。
|
|
表 6 土壤微生物生物量与土壤理化性质及重金属因子的相关系数 Table 6 Correlative coefficients between soil microbial biomass and soil properties or heavy metal factors |
综上,HOM和MOM处理使土壤微生物呼吸强度增加可归结于土壤pH值提高及全磷、Cu和Zn含量增加,其中土壤Cu含量是主要影响因子,表明土壤中Cu含量变化会改变土壤微生物群落代谢利用行为。这与郭星亮[26]研究结果一致,Cu可提高微生物群落对高聚物类碳源的转化利用,但也证实高剂量Cu则会产生一定抑制作用。另外,由于土壤微生物群落代谢多样性仅与土壤Cr含量呈显著相关(P < 0.05),可知MOM与HBS处理土壤代谢群落多样性存在较大差异可能是由于两者Cr含量不同所致,但相关性不高,这可能是因为土壤微生物群落代谢多样性受土壤微生物生物量碳等其他重要因素影响,尚有待进一步研究。
采用基于距离的线性模型(distance-based linear modelling,DistLM)研究土壤微生物群落代谢结构与土壤理化性质及重金属分布相关性(表 7)。
|
|
表 7 土壤微生物群落代谢结构与土壤理化性质及重金属的DistLM分析 Table 7 Distance-based linear modelling (DistLM) analysis of soil microbial community metabolism structure with soil properties and heavy metals |
各土壤重金属因子中,仅有Cu和Zn含量对土壤微生物群落代谢结构变化产生极显著影响(P<0.01),其中土壤Cu含量是造成微生物群落代谢结构差异最根本影响因子〔离均差平方和(sum of squared deviations from mean,SS)为2 583.0〕。各土壤理化指标中,pH值、全盐量、有机质、有效磷和全磷含量等可极显著解释土壤微生物群落代谢结构变化(P<0.01),其中土壤pH值(SS为2 193.2)、全盐量(SS为2 100.8)、有效磷含量(SS为1 995.7)、全磷含量(SS为1 993.8)和有机质含量(SS为1 190.8)对微生物群落代谢结构产生差异的贡献较大。
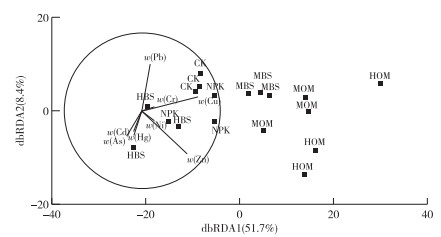
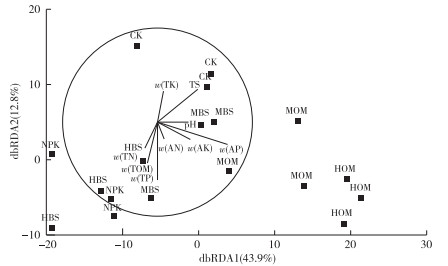
通过基于距离的冗余分析(distance-based redundancy analysis,dbRDA)方法进一步分析土壤理化性质及重金属因子对微生物群落代谢功能多样性影响发现,不同施肥方式下土壤微生物群落功能多样性呈现不同空间分布特征,各影响因子中最主要的为土壤Cu含量,其次是土壤pH值、全盐量和全磷含量(图 3~4),这与DistLM分析结果基本一致。
|
图 3 不同施肥方式下土壤微生物代谢功能与重金属含量的dbRDA分析排序 Figure 3 dbRDA analysis of microbial metabolic function and heavy metals with different fertilization regimes CK为对照处理,NPK为纯化肥处理,HOM为纯有机肥处理,MOM为中量有机肥+化肥处理,HBS为纯沼液肥处理,MBS为中量沼液肥+化肥处理。圆圈内处理相似性较高。 |
|
图 4 不同施肥方式下土壤微生物代谢功能与土壤理化因素dbRDA分析排序 Figure 4 dbRDA analysis of the microbial metabolic function and soil properties with different fertilization regimes CK为对照处理,NPK为纯化肥处理,HOM为纯有机肥处理,MOM为中量有机肥+化肥处理,HBS为纯沼液肥处理,MBS为中量沼液肥+化肥处理。TK、TN、TP、TOM、AN、AP和AK分别为全钾、全氮、全磷、有机质、碱解氮、有效磷和速效钾,TS为全盐量。圆圈内处理相似性较高。 |
连续5 a施用高量(22 500 kg·hm-2·a-1)商品有机肥、中量(11 250 kg·hm-2·a-1)商品有机肥或中量(450 000 kg·hm-2·a-1)沼液肥显著提高土壤微生物代谢活性,且仅有施用高量(22 500 kg·hm-2·a-1)商品有机肥、中量(11 250 kg·hm-2·a-1)商品有机肥对土壤微生物群落代谢结构具有明显影响,而施用高量(450 000 kg·hm-2·a-1)沼液肥显著降低土壤微生物代谢活性和群落多样性。据相关性分析表明,土壤微生物群落代谢功能与土壤理化性质及重金属累积有关,土壤pH值、全磷和Cu含量与土壤微生物代谢活性及其结构关系最密切,其中土壤Cu含量为主要影响因子。综上,适量施用有机肥、沼液肥对土壤微生物群落代谢功能有积极作用,且有机肥较沼液肥效果更明显;而长期高量施用沼液肥不利于土壤微生物代谢活性和群落多样性的维持。可见,在当前发展生态循环农业,大力推广有机肥、沼液肥时,必须在监测重金属等污染残留的基础上,关注安全投入用量,形成沼液肥和有机肥的安全使用技术。
| [1] |
DEGENS B P, SCHIPPER L A, SPARLING G P, et al. Decreases in Organic C Reserves in Soils Can Reduce the Catabolic Diversity of Soil Microbial Communities[J]. Soil Biology and Biochemistry, 2000, 32(2): 189-196. DOI:10.1016/S0038-0717(99)00141-8 (  0) 0) |
| [2] |
李娟, 赵秉强, 李秀英, 等. 长期不同施肥制度下几种土壤微生物学特征变化[J]. 植物生态学报, 2008, 32(4): 891-899. LI Juan, ZHAO Bing-qiang, LI Xiu-ying, et al. Changes of Soil Microbial Properties Affected by Different Long-Term Fertilization Regimes[J]. Journal of Plant Ecology(Chinese Version), 2008, 32(4): 891-899. (  0) 0) |
| [3] |
ENWALL K, NYBERG K, BERTILSSON S, et al. Long-Term Impact of Fertilization on Activity and Composition of Bacterial Communities and Metabolic Guilds in Agricultural Soil[J]. Soil Biology and Biochemistry, 2007, 39(1): 106-115. DOI:10.1016/j.soilbio.2006.06.015 (  0) 0) |
| [4] |
GU Y F, ZHANG X P, TU S H, et al. Soil Microbial Biomass, Crop Yields, and Bacterial Community Structure as Affected by Long-Term Fertilizer Treatments Under Wheat-Rice Cropping[J]. European Journal of Soil Biology, 2009, 45(3): 239-246. DOI:10.1016/j.ejsobi.2009.02.005 (  0) 0) |
| [5] |
陈晓娟, 吴小红, 刘守龙, 等. 不同耕地利用方式下土壤微生物活性及群落结构特性分析:基于PLFA和MicroRespTM方法[J]. 环境科学, 2013, 34(6): 2375-2382. CHEN Xiao-juan, WU Xiao-hong, LIU Shou-long, et al. Microbial Activity and Community Structure Analysis Under the Different Land Use Patterns in Farmland Soils:Based on the Methods PLFA and MicroRespTM[J]. Environmental Science, 2013, 34(6): 2375-2382. (  0) 0) |
| [6] |
钱美宇. MicroRespTM方法研究土壤微生物群落水平生理特征(CLPP)进展[EB/OL]. (2011-03-01)[2017-11-20]. http://www.paper.edu.cn/releasepaper/content/201103-2. QIAN Mei-yu. A Review of Assessing Soil Community Level Physiological Profiles Using MicrorespTM[EB/OL]. (2011-03-01)[2017-11-20]. http://www.paper.edu.cn/releasepaper/content/201103-2. (  0) 0) |
| [7] |
张逸飞, 钟文辉, 李忠佩, 等. 长期不同施肥处理对红壤水稻土酶活性及微生物群落功能多样性的影响[J]. 生态与农村环境学报, 2006, 22(4): 39-44. ZHAGN Yi-fei, ZHONG Wen-hui, LI Zhong-pei, et al. Effects of Long-Term Different Fertilization on Soil Enzyme Activity and Microbial Community Functional Diversity in Paddy Soil Derived From Quaternary Red Clay[J]. Journal of Ecology and Rural Environment, 2006, 22(4): 39-44. (  0) 0) |
| [8] |
罗希茜, 郝晓晖, 陈涛, 等. 长期不同施肥对稻田土壤微生物群落功能多样性的影响[J]. 生态学报, 2009, 29(2): 740-748. LUO Xi-qian, HAO Xiao-hui, CHEN Tao, et al. Effects of Long-Term Different Fertilization on Microbial Community Functional Diversity in Paddy Soil[J]. Acta Ecologica Sinica, 2009, 29(2): 740-748. (  0) 0) |
| [9] |
郝晓晖, 胡荣桂, 吴金水, 等. 长期施肥对稻田土壤有机氮、微生物生物量及功能多样性的影响[J]. 应用生态学报, 2010, 21(6): 1477-1484. HAO Xiao-hui, HU Rong-gui, WU Jin-shui, et al. Effects of Long-Term Fertilization on Paddy Soils Organic Nitrogen, Microbial Biomass, and Microbial Functional Diversity[J]. Chinese Journal of Applied Ecology, 2010, 21(6): 1477-1484. (  0) 0) |
| [10] |
侯晓杰, 汪景宽, 李世朋. 不同施肥处理与地膜覆盖对土壤微生物群落功能多样性的影响[J]. 生态学报, 2007, 27(2): 655-661. HOU Xiao-jie, WANG Jing-kuan, LI Shi-peng. Effect of Different Fertilization and Plastic-Mulching on Functional Diversity of Soil Microbial Community[J]. Acta Ecologica Sinica, 2007, 27(2): 655-661. (  0) 0) |
| [11] |
高明霞, 孙瑞, 崔全红, 等. 长期施用化肥对塿土微生物多样性的影响[J]. 植物营养与肥料学报, 2015, 21(6): 1572-1580. GAO Ming-xia, SUN Rui, CUI Quan-hong, et al. Effect of Long-Term Chemical Fertilizer Application on Soil Microbial Diversity in Anthropogenic Loess Soil[J]. Journal of Plant Nutrition and Fertilizer, 2015, 21(6): 1572-1580. DOI:10.11674/zwyf.2015.0624 (  0) 0) |
| [12] |
王斌, 孙健. 鄞州区耕地质量评价与管理[M]. 北京: 中国农业科学技术出版社, 2014: 2. WANG Bin, SUN Jian. Evaluation and Management on Quality of Cultivated Land in Yinzhou[M]. Beijing: China Agricultural Science and Technology Press, 2014: 2. (  0) 0) |
| [13] |
NY/T 1121. 1-2006, 土壤检测. 第1部分: 土壤样品的采集、处理和贮存[S]. NY/T 1121. 1-2006, Soil Testing Part 1: Soil Sampling, Processing and Reposition[S]. (  0) 0) |
| [14] |
CAMPBELL C D, CHAPMAN S J, CAMERON C M, et al. A Rapid Microtiterplate Method to Measure Carbon Dioxide Evolved From Carbon Substrate Amendments so as to Determine the Physiological Profiles of Soil Microbial Communities by Using Whole Soil[J]. Applied Environmental Microbiology, 2003, 69(6): 3593-3599. DOI:10.1128/AEM.69.6.3593-3599.2003 (  0) 0) |
| [15] |
HARCHA B D, CORRELLA R L, MEECHB W, et al. Using the Gini Coefficient With BIOLOG Substrate Utilization Data to Provide an Alternative Quantitative Measure for Comparing Bacteria Soil Communities[J]. Journal of Microbiological Methods, 1997, 30(1): 91-101. DOI:10.1016/S0167-7012(97)00048-1 (  0) 0) |
| [16] |
MERWE T V D, WOLFAARDT F, RIEDEL K H. Analysis of the Functional Diversity of the Microbial Communities in a Paper-Mill Water System[J]. Water SA, 2003, 9(1): 31-34. (  0) 0) |
| [17] |
林辉, 孙万春, 王飞, 等. 有机肥中重金属对菜田土壤微生物群落代谢的影响[J]. 农业环境科学学报, 2016, 35(11): 2123-2130. LIN Hui, SUN Wan-chun, WANG Fei, et al. Effects of Heavy Metal Within Organic Fertilizers on the Microbial Community Metabolic Profile of a Vegetable Soil After Land Application[J]. Journal of Agro-Environment Science, 2016, 35(11): 2123-2130. DOI:10.11654/jaes.2016-0674 (  0) 0) |
| [18] |
时鹏, 高强, 王淑平, 等. 玉米连作及其施肥对土壤微生物群落功能多样性的影响[J]. 生态学报, 2010, 30(22): 6173-6182. SHI Peng, GAO Qiang, WANG Shu-ping, et al. Effects of Continuous Cropping of Corn and Fertilization in Soil Microbial Community Functional Diversity[J]. Acta Ecologica Sinica, 2010, 30(22): 6173-6182. (  0) 0) |
| [19] |
GB 15618-1995, 土壤环境质量标准[S]. GB 15618-1995, Environmental Quality Standard for Soils[S]. (  0) 0) |
| [20] |
蒋艳梅. 重金属Cu、Zn、Cd、Pb复合污染对稻田土壤微生物群落结构与功能的影响[D]. 杭州: 浙江大学, 2007. JIANG Yan-mei. Effect of the Combined Pollution of Heavy Metals Microbial Community Structure and Function in Paddy Soil[D]. Hangzhou: Zhejiang University, 2007. (  0) 0) |
| [21] |
孙瑞, 孙本华, 高明霞, 等. 长期不同土地利用方式下土壤微生物特性的变化[J]. 植物营养与肥料学报, 2015, 21(3): 655-663. SUN Rui, SUN Ben-hua, GAO Ming-xia, et al. Changes of Soil Microbial Characteristics Under Long-Term Different Land Use Patterns on an Anthropogenic Loess Soil[J]. Journal of Plant Nutrition and Fertilizer, 2015, 21(3): 655-663. DOI:10.11674/zwyf.2015.0312 (  0) 0) |
| [22] |
BUYER J S, TEASDALE J R, ROBERTS D P, et al. Factors Affecting Soil Microbial Community Structure in Tamato Cropping Systems[J]. Soil Biology and Biochemistry, 2010, 42(5): 831-841. DOI:10.1016/j.soilbio.2010.01.020 (  0) 0) |
| [23] |
李轶, 张玉龙, 谷士艳, 等. 施用沼肥对保护地土壤微生物群落影响的研究[J]. 可再生能源, 2007, 25(2): 44-46. LI Yi, ZHANG Yu-long, GU Shi-yan, et al. Study on Effects of Applying Biogas Fertilizer on Diversity Index of Microbial Communities in Soil of Protected Field[J]. Renewable Energy Resources, 2007, 25(2): 44-46. (  0) 0) |
| [24] |
BAUSENWEIN U, GATTINGER A, LANGER U, et al. Exploring Soil Microbial Communities and Soil Organic Matter:Variability and Interactions in Arable Soils Under Minimum Tillage Practice[J]. Applied Soil Ecology, 2008, 40(1): 67-77. DOI:10.1016/j.apsoil.2008.03.006 (  0) 0) |
| [25] |
WAKELIN S A, COLLOFF M J, HARVEY P R, et al. The Effects of Stubble Retention and Nitrogen Application on Soil Microbial Community Structure and Functional Gene Abundance Under Irrigated Maize[J]. FEMS Microbiology Ecology, 2006, 59(3): 661-670. (  0) 0) |
| [26] |
郭星亮. 重金属Cu、Zn对堆肥过程中微生物群落代谢和水解酶活性的影响[D]. 杨凌: 西北农林科技大学, 2011. GUO Xing-liang. Effect of Heavy Metal Cu and Zn on Microbial Community Metabolic Profiles and Hydrolytic Enzyme Activities in Composting[D]. Yangling: Northwest Agriculture & Forestry University, 2011. (  0) 0) |




