2. 浙江省环境监测中心, 浙江 杭州 310012
2. Zhejiang Environmental Monitoring Centre, Hangzhou 310012, China
大量氮素进入水体是引起水体富营养化的重要原因之一。硝态氮是河道水体中氮素的主要组成部分, 由于其具有较高的稳定性和溶解性, 因此去除水中低浓度硝态氮较为困难。吸附法因具有设计简单、操作方便和运行成本低等优点, 常被用来去除水中硝态氮。生物炭一般是指生物有机材料(生物质, 如植物根茎、木材或动物组织等)在缺氧或限氧条件下高温裂解形成的固体产物[1]。生物炭表面官能团丰富, 具有多孔结构, 是一种高效的吸附剂[2]。近年来, 生物炭作为一种新型功能材料, 对氨氮、有机污染物和金属阳离子等有良好的吸附效果, 在土壤改良、固碳减排以及污染环境修复等方面得到广泛应用[3]。由于未改性生物炭表面的含氧活性基团使其通常带负电荷, 阳离子交换容量高于阴离子交换容量, 因此未改性生物炭主要通过静电作用吸附硝态氮, 吸附能力很弱[2]。为提高生物炭对硝态氮的吸附能力, 通常对生物炭进行改性, 如酸改性、负载金属离子改性等。负载金属离子改性主要通过金属离子在生物炭表面生成金属氧化物或氢氧化物实现对硝态氮的吸附。ρ(硝态氮)为27 mg·L-1时, 经ZnCl2改性的甜菜渣生物炭对硝态氮的最大吸附量为15.75 mg·g-1[4]; 铁改性花生壳炭和小麦秸秆炭对硝态氮最大吸附潜力分别为2 674和1 285 mg·kg-1[5]。
目前大多数研究都集中在生物炭去除工业废水中高浓度硝态氮, 将生物炭用于去除湿地和湖泊等水体中低浓度硝态氮的研究较少。利用大型水生植物处理污水具有成本低、效果好等优势, 目前大型水生植物修复技术已广泛应用于富营养化湖泊的治理中[6], 芦苇、香蒲等大型水生植物也在人工湿地中发挥着重要作用[7]。但当秋冬季节大型水生植物进入衰亡期后, 植物残体分解会释放大量氮磷等营养物, 易造成水体二次污染。因此, 笔者利用再力花(Thalia dealbata)、香蒲(Typha orientalis)和芦苇(Phragmites australis)3种水生态修复植物作为原料制备生物炭并进行改性, 增强其对水体中低浓度硝态氮的吸附能力, 为水体深度脱氮和解决大型水生植物修复富营养化水体过程中二次污染问题提供新思路。
1 材料与方法 1.1 水生植物生物炭的制备及改性选用常见的3种水生植物再力花、香蒲和芦苇作为制备生物炭的原料。3种水生植物采自南京大学仙林校区天籁河, 洗净剪碎, 放入烘箱中60 ℃条件下烘干后备用。取一定量烘干的水生植物用锡箔纸包住, 轻轻压实, 放入真空管式炉中。以400 mL·min-1的流速通入N2, 以10 ℃·min-1的升温速率升至500 ℃后保持恒温热解1 h制备生物炭。取出制备好的生物炭粉碎后过1 mm孔径筛, 再用去离子水润洗3次除去表面杂质。然后分别将3种生物炭放入1 mol·L-1盐酸溶液中浸泡2 h, 以去除生物炭中灰分等杂质。接着将浸泡有生物炭的盐酸溶液用真空泵抽滤, 并用去离子水反复洗涤过滤直至滤液为中性, 在60 ℃烘箱中烘干至恒重。再力花、香蒲和芦苇生物炭分别用ZC、XC和LC表示。
生物炭改性方法如下:分别将酸洗后的3种生物炭放入一定量1 mol·L-1FeCl3溶液中, 通过调节溶液体积, 使铁与生物炭质量比为0.6, 放入磁力搅拌器充分搅拌混合1 h后用真空泵抽滤, 然后采用去离子水反复洗涤至滤液透明澄清无Fe3+, 最后在60 ℃条件下烘干至恒重, 得到改性生物炭[8]。铁改性再力花、香蒲和芦苇生物炭分别用Fe-ZC、Fe-XC和Fe-LC表示。试验用试剂均为分析纯。
1.2 不同改性水生植物生物炭的结构表征与吸附能力的比选采用扫描电镜(SEM)观察改性前后生物炭表面形态结构变化, 采用能谱分析仪(EDS)分析改性前后水生植物生物炭中常量元素组成。将改性前后的生物炭样品与干燥的KBr以1:20质量比混合压片后, 在红外灯下烘干, 然后用傅里叶变换红外光谱仪扫描检测, 扫描范围为400~4 000 cm-1。
分别取3种水生植物改性前后的生物炭0.1 g放入50 mL含氮量为2 mg·L-1的KNO3溶液中, 在200 r·min-1、25 ℃条件下振荡24 h后取出, 过0.45 μm孔径滤膜, 滤液中硝态氮浓度测定参照HJ/T 346—2007 《水质硝酸盐氮的测定紫外分光光度法(试行)》。改性水生植物生物炭对硝态氮的平衡吸附量计算公式为
| $ {q_{\rm{e}}} = \left( {{C_0}-{C_{\rm{e}}}} \right) \cdot V/m 。$ | (1) |
式(1)中, qe为平衡吸附量, mg·g-1; C0为初始硝态氮质量浓度, mg·L-1; Ce为吸附平衡时硝态氮质量浓度, mg·L-1; V为硝态氮溶液体积, mL; m为生物炭质量, g。
1.3 改性水生植物生物炭对低浓度硝态氮的吸附动力学分别在50 mL含氮量为2 mg·L-1的KNO3溶液中加入0.1 g的3种改性后水生植物生物炭, 在200 r·min-1、25 ℃条件下振荡, 分别于0.5、1、2、4、6、8、10、12和24 h时取出, 过0.45 μm孔径滤膜, 测定滤液中硝态氮浓度, 测定方法同1.2节。各对应时间改性水生植物生物炭对硝态氮的吸附量计算公式为
| $ {q_t} = \left( {{C_0}-{C_{\rm{e}}}} \right) \cdot V/m 。$ | (2) |
式(2)中, qt为t时刻硝态氮吸附量, mg·g-1; C0为初始溶液中硝态氮质量浓度, mg·L-1; Ct为t时刻溶液中硝态氮质量浓度, mg·L-1; V为硝态氮溶液体积, mL; m为生物炭质量, g。
1.4 改性水生植物生物炭对硝态氮的吸附热力学分别取50 mL不同浓度梯度(0、0.5、1、2、4、6、8和10 mg·L-1)硝态氮溶液加入具塞聚丙烯瓶中, 每个浓度组设置3个重复。分别在上述溶液中添加0.1 g Fe-ZC、Fe-XC和Fe-LC, 200 r·min-1、25 ℃条件下振荡24 h后取出, 过滤后测定滤液中硝态氮浓度, 测定方法同1.2节, 并按式(1)计算改性水生植物生物炭对硝态氮的平衡吸附量。
1.5 溶液pH对改性水生植物生物炭吸附硝态氮的影响通过添加浓度为1 mol·L-1的NaOH或HCl溶液, 调节KNO3溶液(2 mg·L-1)pH值分别为3.0、5.0、7.0、9.0和11.0。分别在50 mL不同pH值的KNO3溶液中加入0.1 g Fe-ZC、Fe-XC和Fe-LC, 200 r·min-1、25 ℃条件下振荡24 h, 取出过滤后测定滤液中硝态氮浓度, 测定方法同1.2节, 并按式(1)计算改性水生植物生物炭对硝态氮的平衡吸附量。
1.6 数据分析采用Excel 2010软件进行数据统计, 采用OriginPro 2016软件制图, 采用SPSS 16.0软件进行方差、回归以及最小显著差异法分析, 显著性水平设置为α=0.05。
2 结果与讨论 2.1 不同改性水生植物生物炭的结构表征与吸附硝态氮能力比选不同水生植物生物炭改性前后扫描电镜图见图 1。

|
图 1 不同水生植物生物炭改性前后扫描电镜图 Figure 1 SEM images of biochar and modified biochar prepared with different macrophytes ZC、XC和LC分别为再力花、香蒲和芦苇生物炭; Fe-ZC、Fe-XC和Fe-LC分别为铁改性再力花、香蒲和芦苇生物炭。 |
由图 1可知, 生物质材料通过热解后一定程度上保留了原材料的结构特性, 大多为片状或者管状。未改性生物炭表面较光滑, 改性之后生物炭表面和空隙端口变得粗糙, 粗糙的表面会使其比表面积更大, 有利于增加改性生物炭的吸附位点。BHATNAGAR等[9]研究发现经ZnCl2改性后的椰子壳生物炭比表面积变小, 而笔者研究中采用氯化铁对水生植物生物炭改性后其比表面积变大。能谱分析发现, 未改性生物炭中铁含量低于检测限, 而改性后3种生物炭中铁含量w分别为1.75%(Fe-ZC)、1.54%(Fe-XC)和1.37%(Fe-LC)。
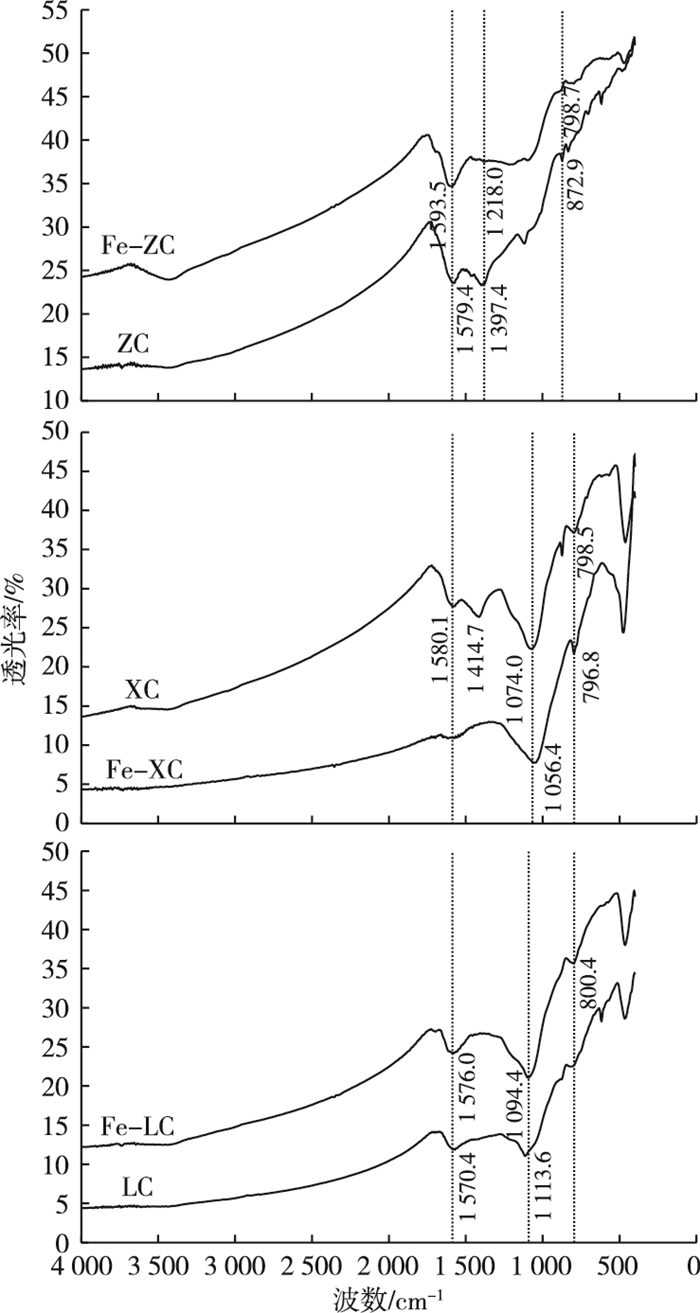
由图 2可知, 改性前后生物炭表面官能团较相似, 主要吸收峰在1 587 cm-1附近, 是由羰基C=O的伸缩振动引起, 也包含共轭的C=C伸缩振动, 这与SWIATKOWSKI等[10]的研究结果相一致。其他主要吸收峰在1 050~1 090和800 cm-1附近, 分别是由饱和的C—O伸缩振动和—C—H在苯环外的弯曲振动引起。在600 cm-1附近, 铁改性前后的水生植物生物炭波形图略有不同, 有研究表明该波段体现的是Fe—O基团的弯曲振动[11]。Fe—O基团的存在使得生物炭表面具有正电荷, 使提升其对硝态氮吸附能力成为可能。
|
图 2 不同水生植物生物炭改性前后红外光谱图 Figure 2 FTIR spectra of biochar and modified biochar prepared with different macrophytes ZC、XC和LC分别为再力花、香蒲和芦苇生物炭; Fe-ZC、Fe-XC和Fe-LC分别为铁改性再力花、香蒲和芦苇生物炭。 |
3种改性生物炭对硝态氮吸附量如表 1所示。未改性水生植物生物炭对硝态氮的吸附量为负值, 这是由于在生物炭孔道内部残留有微量硝态氮, 经过吸附试验过程中长时间的振荡, 这些硝态氮会释放到溶液中。而经过铁改性后, 3种水生植物生物炭对硝态氮的吸附量都明显提高。这是因为经过铁改性后的生物炭表面负载了Fe—O基团, 表面更为粗糙, 吸附位点增加, 从而增强了生物炭对低浓度硝态氮的吸附性能。其中铁改性香蒲生物炭对硝态氮吸附量最大, 为0.754 mg·g-1, 对硝态氮去除率达75.4%。吕欣田等[12]用1 g分别经MgCl2·6H2O和CaCl2改性的香蒲生物炭对20 mg·L-1硝态氮溶液进行吸附试验, 发现两者对硝态氮的去除率分别为9.55%和2.32%。笔者研究中, 经FeCl3改性的香蒲生物炭对硝态氮的去除率明显提高, 表明FeCl3改性能有效提升水生植物生物炭对低浓度硝态氮的吸附性能。已有研究表明经过铁改性的芦苇生物炭能够有效去除水中低浓度磷[13], 因此, 将FeCl3改性水生植物生物炭用于去除水体中低浓度硝态氮的同时, 还能有效去除磷。
|
|
表 1 不同水生植物生物炭改性前后对硝态氮吸附量的比较 Table 1 Nitrate adsorption capacity of biochar and modified biochar prepared with different macrophytes |
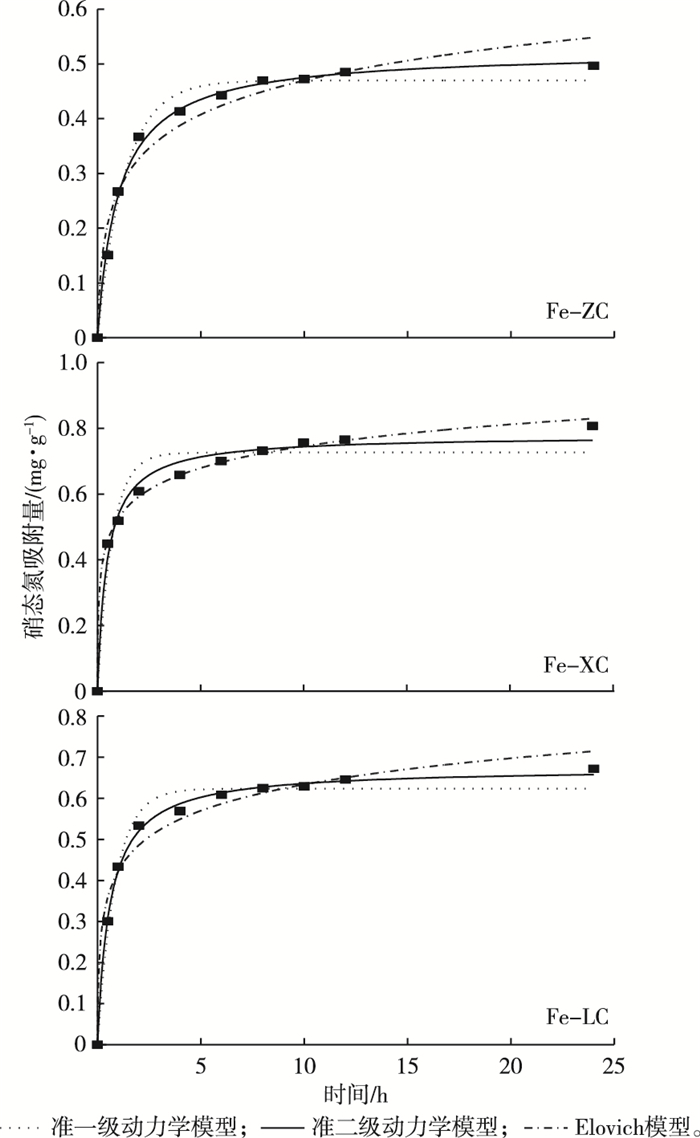
分别用准一级动力学、准二级动力学和Elovich这3种模型拟合分析改性水生植物生物炭对低浓度硝态氮的吸附动力学[14]。在吸附低浓度硝态氮过程中, 改性水生植物生物炭对硝态氮的吸附量随吸附时间的延长而增加, 在初始4 h内吸附速率较快, 之后吸附量缓慢上升, 到24 h时基本达到平衡, 平衡时Fe-XC对硝态氮的吸附量最大(图 3)。
|
图 3 不同改性水生植物生物炭对硝态氮的吸附动力学曲线 Figure 3 Adsorption kinetics of nitrate on the modified biochar prepared with different macrophytes Fe-ZC、Fe-XC和Fe-LC分别为铁改性再力花、香蒲和芦苇生物炭。 |
对比3种模型拟合结果发现, 准二级模型的R2值最高, 达到0.99, 表明准二级动力学模型能更好地表征改性生物炭对硝态氮的吸附过程, 这与李丽等[5]的研究结果相一致。准二级吸附模型包含了迁移、扩散、表面化学吸附和颗粒内部物理扩散等过程[15], 能更为全面地反映改性生物炭对硝态氮的吸附机制。改性水生植物生物炭对硝态氮的吸附主要为化学吸附[16], 表明吸附是由Fe—O基团引起的[17], 这一结果使铁改性水生植物生物炭用于富营养化水体深度脱氮成为可能。
王荣荣等[16]研究发现花生壳生物炭对800 mg·L-1硝态氮溶液中硝态氮的饱和吸附量为40 mg·g-1。但有研究表明太湖水体中总氮质量浓度为0.68~2.65 mg·L-1[18], 2006—2010年苏南湖泊群水体中ρ(总氮)最大值约为5 mg·L-1, 其中硝态氮约占总氮的76%[19]。笔者研究中将初始ρ(硝态氮)设置为2 mg·L-1, 以更好地模拟实际水体中生物炭对硝态氮的吸附过程, 为启用铁改性水生植物生物炭控制水体富营养化提供理论依据。
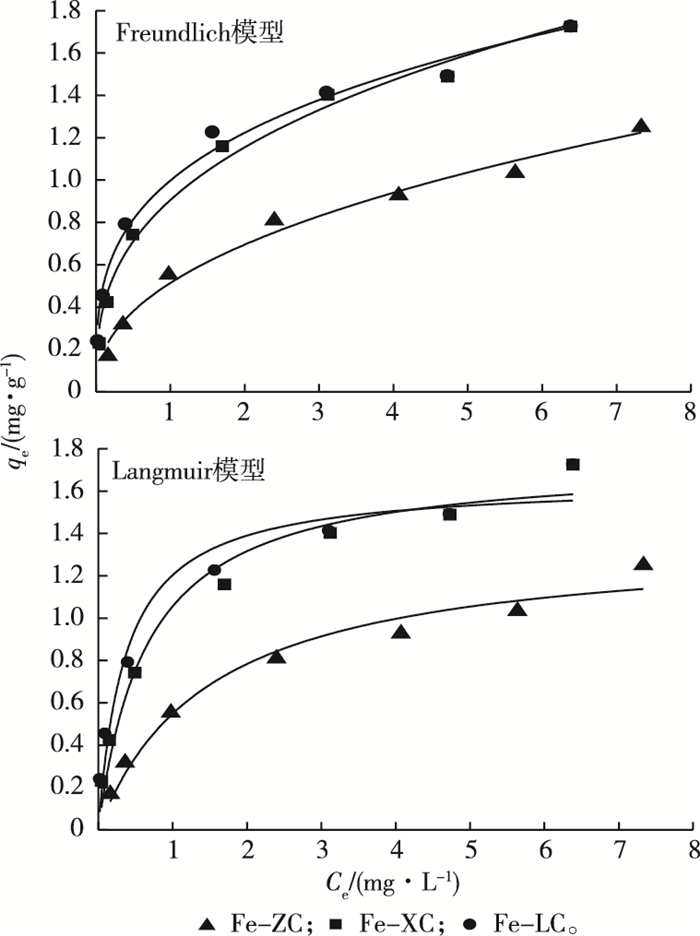
2.3 改性水生植物生物炭对硝态氮的吸附热力学采用Freundlich和Langmuir热力学模型[20]拟合得到3种改性水生植物生物炭对硝态氮的吸附等温线(图 4)。
|
图 4 Freundlich和Langmuir拟合的不同改性水生植物生物炭对硝态氮吸附等温线 Figure 4 Freundlich and Langmuir adsorption isotherms of nitrate on modified biochar prepared Fe-ZC、Fe-XC和Fe-LC分别为铁改性再力花、香蒲和芦苇生物炭。 qe为平衡吸附量; Ce为吸附平衡时硝态氮质量浓度。 |
结果表明, Freundlich模型能有效拟合水生植物生物炭对低浓度硝态氮吸附过程, 决定系数R2均在0.98以上, 这表明改性生物炭对硝态氮的吸附是非均一多分子层吸附, 与大多数生物炭吸附污染物的机理[20-21]相一致。Freundlich模型中,n为经验常数, 1/n越小,则吸附能力越强[15], 0.1 < 1/n < 1时极易吸附。铁改性后芦苇、香蒲和再力花生物炭的1/n分别为0.35、0.29和0.43, 表明3种改性水生植物生物炭极易吸附低浓度硝态氮, 有利于硝态氮的去除。
利用Langmuir模型拟合水生植物生物炭吸附低浓度硝态氮过程, 决定系数R2均在0.95以上, 得到的理论最大吸附量具有参考意义。Fe-ZC、Fe-XC和Fe-LC对硝态氮的理论最大吸附量分别为1.370、1.747和1.644 mg·g-1。ZHANG等[22]利用铁改性花生壳生物炭对20 mg·L-1硝态氮溶液的理论最大吸附量为1.170 mg·g-1, 李丽等[5]研究表明铁改性小麦秸秆生物炭对20 mg·L-1硝态氮溶液的理论最大吸附量为1.285 mg·g-1。笔者研究中经过铁改性的水生植物生物炭对硝态氮最大吸附量均高于上述研究结果, 表明由水生植物制备的生物炭能有效去除富营养化水体中硝态氮, 其中铁改性香蒲生物炭对低浓度硝态氮吸附潜力最大。由于水生植物取材于湖泊水体, 制成的生物炭又用于去除湖泊营养盐, 不仅降低了生物炭的生产成本, 而且实现了水生植物的资源化利用。生物炭的吸附性能主要由生物质原料结构、热解条件和改性方式决定, 因此, 需要不断优化生物炭的生产条件, 提升改性方法, 从而获得吸附性能更好的生物炭。
3种改性水生植物生物炭的最适添加量计算公式为
| $ a = {C_0}/{q_{\rm{e}}}。$ | (3) |
式(3)中, a为生物炭最适添加量, g·L-1; C0为初始硝态氮质量浓度, mg·L-1; qe为平衡吸附量, mg·g-1。
计算得到Fe-ZC、Fe-XC和Fe-LC的最适添加量分别为1.50、1.14和1.22 g·L-1。在高初始硝态氮浓度下, 物质传输驱动力更大, 生物炭对硝态氮的吸附量更大。已有研究发现, 对于初始质量浓度为20 mg·L-1的硝态氮溶液, 投加28 g·L-1花生壳炭对硝态氮有较好的去除效果[5]。笔者在初始硝态氮浓度较低情况下投加的生物炭量少, 去除效果好, 且具经济性, 因此, 改性后水生植物生物炭在去除水体中低浓度硝态氮方面具有良好的应用前景。
2.4 溶液pH值对改性水生植物生物炭吸附硝态氮的影响由表 2可知, pH值为3.0~9.0对改性生物炭吸附硝态氮量没有较大影响; 但pH值达到11.0时3种改性生物炭对硝态氮的吸附能力都明显下降, Fe-ZC、Fe-XC和Fe-LC对硝态氮吸附量分别为0.074、0.069和0.274 mg·g-1, 分别下降86.2%、91.2%和62.8%。这是由于pH值较高情况下, 溶液中OH-与生物炭表面的正电荷基团结合, 降低了表面正电荷数量, 与硝酸根离子之间的静电作用减弱, 导致吸附性能下降[23]。
|
|
表 2 溶液初始pH值对不同改性水生植物生物炭吸附硝态氮的影响 Table 2 Effects of initial pH on nitrate sorption of modified biochar prepared with different macrophytes |
有研究表明初始溶液只有为中性时, 竹炭对硝态氮的去除率才较高[24], 酸性条件更有利于盐酸改性的水生植物生物炭对硝态氮的吸附, 初始溶液pH值为2.0时花生壳生物炭对高浓度硝态氮的吸附效果最好[16]。而笔者研究结果表明, 铁改性水生植物生物炭对硝态氮吸附受pH值的影响较小, 在非强碱条件下都有很好的吸附效果。人工湿地和太湖等水环境中pH值分别为6.90~7.20和6.26~7.66, 平均值为7.00[18, 25], 水体pH值不会对铁改性生物炭吸附硝态氮产生不利影响。此外, 有研究表明生物炭对底泥氨氮、COD和磷酸盐的释放有抑制作用, 可用于受污染底泥修复[26]。因此, 可从湿地或者湖泊中收割水生植物制备成改性生物炭, 然后投加回湿地或湖泊中吸附水中硝态氮和抑制底泥中氮磷释放, 有助于污染水体的有效净化。同时, 利用水生植物制备改性生物炭还能减轻水生植物腐烂对水体的二次污染, 实现水生植物的资源化利用以及碳在人工湿地或湖泊中的内循环。
3 结论(1) 经过铁改性, 大量Fe3+负载在水生植物制备的生物炭表面, 并形成Fe—O基团, 大幅提升生物炭对硝态氮的吸附性能。铁改性再力花、香蒲和芦苇生物炭对低浓度硝态氮的吸附动力学均符合准二级动力学方程, Freundlich模型能更好地描述吸附热力学过程, 表明其对低浓度硝态氮的吸附过程是非均一多分子层吸附, 以化学吸附为主。通过计算得到3种改性生物炭中铁改性香蒲生物炭的理论最大吸附量为1.747 mg·g-1, 改性生物炭对低浓度硝态氮的去除具有很好的应用前景。
(2) 改性生物炭对硝态氮的吸附受pH影响较小, 只需避免应用在强碱性环境下。在非碱性条件下, 向2 mg·L-1硝态氮溶液中投加1.14 g·L-1铁改性香蒲生物炭, 就能获得很好的硝态氮去除效果。将水生植物制备成生物炭投加到富营养化水体中, 可在深度脱氮的同时实现水生植物资源化利用, 能消除由于水生植物未及时收割所产生的二次污染。
为了更好地将水生植物制备的生物炭应用于低浓度硝态氮水体实际治理中, 还需要进一步开展长期的野外试验, 评价其吸附作用的长期效应, 并需探索其生态安全性。
| [1] |
LEHMANN J, GAUNT J, RONDON M. Bio-Char Sequestration in Terrestrial Ecosystems:A Review[J]. Mitigation and Adaptation Strategies for Global Change, 2006, 11(2): 403-427. DOI:10.1007/s11027-005-9006-5 (  0) 0) |
| [2] |
孔丝纺, 姚兴成, 张江勇, 等. 生物质炭的特性及其应用的研究进展[J]. 生态环境学报, 2015, 24(4): 716-723. KONG Si-fang, YAO Xing-cheng, ZHANG Jiang-yong, et al. Review of Characteristics of Biochar and Research Progress of Its Applications[J]. Ecology and Environmental Sciences, 2015, 24(4): 716-723. (  0) 0) |
| [3] |
袁金华, 徐仁扣. 稻壳制备的生物质炭对红壤和黄棕壤酸度的改良效果[J]. 生态与农村环境学报, 2010, 26(5): 472-476. YUAN Jin-hua, XU Ren-kou. Effects of Rice-Hull-Based Biochar Regulating Acidity of Red Soil and Yellow Brown Soil[J]. Journal of Ecology and Rural Environment, 2010, 26(5): 472-476. (  0) 0) |
| [4] |
DEMIRAL H, GUNDUZOGLU G. Removal of Nitrate From Aqueous Solutions by Activated Carbon Prepared From Sugar Beet Bagasse[J]. Bioresource Technology, 2010, 101(6): 1675-1680. DOI:10.1016/j.biortech.2009.09.087 (  0) 0) |
| [5] |
李丽, 陈旭, 吴丹, 等. 固定化改性生物质炭模拟吸附水体硝态氮潜力研究[J]. 农业环境科学学报, 2015, 34(1): 137-143. LI Li, CHEN Xu, WU Dan, et al. Adsorption of Aqueous Nitrate-N by Immobilized Modified Biochar[J]. Journal of Agro-Environment Science, 2015, 34(1): 137-143. DOI:10.11654/jaes.2015.01.020 (  0) 0) |
| [6] |
崔丽娟, 李伟, 张曼胤, 等. 不同湿地植物对污水中氮磷去除的贡献[J]. 湖泊科学, 2011, 23(2): 203-208. CUI Li-juan, LI Wei, ZHANG Man-yin, et al. Different Wetland Plant Roles of Removing Nitrogen and Phosphorus on Sewage Water[J]. Journal of Lake Sciences, 2011, 23(2): 203-208. DOI:10.18307/2011.0207 (  0) 0) |
| [7] |
张振华, 高岩, 郭俊尧, 等. 富营养化水体治理的实践与思考:以滇池水生植物生态修复实践为例[J]. 生态与农村环境学报, 2014, 30(1): 129-135. ZHANG Zhen-hua, GAO Yan, GUO Jun-yao, et al. Practice and Reflections of Remediation of Eutrophicated Waters:A Case Study of Haptophyte Remediation of the Ecology of Dianchi[J]. Journal of Ecology and Rural Environment, 2014, 30(1): 129-135. (  0) 0) |
| [8] |
李际会, 吕国华, 白文波, 等. 改性生物炭的吸附作用及其对土壤硝态氮和有效磷淋失的影响[J]. 中国农业气象, 2012, 33(2): 220-225. LI Ji-hui, LÜ Guo-hua, BAI Wen-bo, et al. Effect of Modified Biochar on Soil Nitrate Nitrogen and Available Phosphorus Leaching[J]. Chinese Journal of Agrometeorology, 2012, 33(2): 220-225. (  0) 0) |
| [9] |
BHATNAGAR A, JI M, YANG H C, et al. Removal of Nitrate From Water by Adsorption Onto Zinc Chloride Treated Activated Carbon[J]. Separation Science and Technology, 2008, 43(4): 886-907. DOI:10.1080/01496390701787461 (  0) 0) |
| [10] |
SWIATKOWSKI A, PAKULA M, BINIAK S, et al. Influence of the Surface Chemistry of Modified Activated Carbon on Its Electrochemical Behaviour in the Presence of Lead (Ⅱ) Ions[J]. Carbon, 2004, 42(15): 3057-3069. DOI:10.1016/j.carbon.2004.06.043 (  0) 0) |
| [11] |
LIU Z G, ZHANG F S, SASAI R. Arsenate Removal From Water Using Fe3O4:Loaded Activated Carbon Prepared From Waste Biomass[J]. Chemical Engineering Journal, 2010, 160(1): 57-62. DOI:10.1016/j.cej.2010.03.003 (  0) 0) |
| [12] |
吕欣田, 张文, 刘茜, 等. 改性香蒲炭模拟水体氮、磷吸附效果研究[J]. 广州化工, 2017, 45(15): 75-78. LÜ Xin-tian, ZHANG Wen, LIU Qian, et al. Study on Adsorption of Nitrogen and Phosphorus From Modified Cattail Biochars[J]. Guangzhou Chemical Industry, 2017, 45(15): 75-78. DOI:10.3969/j.issn.1001-9677.2017.15.027 (  0) 0) |
| [13] |
唐登勇, 黄越, 胥瑞晨, 等. 改性芦苇生物炭对水中低浓度磷的吸附特征[J]. 环境科学, 2016, 37(6): 2195-2201. TANG Deng-yong, HUANG Yue, XU Rui-chen, et al. Adsorption Behavior of Low Concentration Phosphorus From Water Onto Modified Reed Biochar[J]. Environmental Science, 2016, 37(6): 2195-2201. (  0) 0) |
| [14] |
GERENTE C, LEE V K C, CLOIREC P L, et al. Application of Chitosan for the Removal of Metals From Wastewaters by Adsorption:Mechanisms and Models Review[J]. Critical Reviews in Environmental Science and Technology, 2007, 37(1): 41-127. DOI:10.1080/10643380600729089 (  0) 0) |
| [15] |
杜衍红, 蒋恩臣, 李治宇, 等. 稻壳炭对铵态氮的吸附机理研究[J]. 农业机械学报, 2016, 47(2): 193-199. DU Yan-hong, JIANG En-chen, LI Zhi-Yu, et al. Adsorption Mechanism of Ammonium Nitrogen Onto Rice Husk Biochar[J]. Transactions of the Chinese Society for Agricultural Machinery, 2016, 47(2): 193-199. DOI:10.6041/j.issn.1000-1298.2016.02.025 (  0) 0) |
| [16] |
王荣荣, 赖欣, 李洁, 等. 花生壳生物炭对硝态氮的吸附机制研究[J]. 农业环境科学学报, 2016, 35(9): 1727-1734. WANG Rong-rong, LAI Xin, LI Jie, et al. Adsorption of Nitrate Nitrogen by Peanut Shell Biochar[J]. Journal of Agro-Environment Science, 2016, 35(9): 1727-1734. DOI:10.11654/jaes.2016-0230 (  0) 0) |
| [17] |
LOGANATHAN P, VIGNESWARAN S, KANDASAMY J. Enhanced Removal of Nitrate From Water Using Surface Modification of Adsorbents:A Review[J]. Journal of Environmental Management, 2013, 131: 363-374. (  0) 0) |
| [18] |
吴筱清. 太湖水环境特征及沉积物有机质来源识别[D]. 南京: 南京大学, 2015. WU Xiao-qing. Water Environmental Characters and Sediment Organic Matter Source Identification of Lake Taihu[D]. Nanjing: Nanjing University, 2015. (  0) 0) |
| [19] |
陈小华, 李小平, 王菲菲, 等. 苏南地区湖泊群的富营养化状态比较及指标阈值判定分析[J]. 生态学报, 2014, 34(2): 390-399. CHEN Xiao-hua, LI Xiao-ping, WANG Fei-fei, et al. Research on the Difference in Eutrophication State and Indicator Threshold Value Determination Among Lakes in the Southern Jiangsu Province, China[J]. Acta Ecologica Sinica, 2014, 34(2): 390-399. (  0) 0) |
| [20] |
CHUNG H K, KIM W H, PARK J, et al. Application of Langmuir and Freundlich Isotherms to Predict Adsorbate Removal Efficiency or Required Amount of Adsorbent[J]. Journal of Industrial and Engineering Chemistry, 2015, 28: 241-246. DOI:10.1016/j.jiec.2015.02.021 (  0) 0) |
| [21] |
CHINTALA R, MOLLINEDO J, SCHUMACHER T E, et al. Nitrate Sorption and Desorption in Biochars From Fast Pyrolysis[J]. Microporous and Mesoporous Materials, 2013, 179: 250-257. DOI:10.1016/j.micromeso.2013.05.023 (  0) 0) |
| [22] |
ZHANG M, GAO B, YAO Y, et al. Synthesis of Porous MgO-Biochar Nanocomposites for Removal of Phosphate and Nitrate From Aqueous Solutions[J]. Chemical Engineering Journal, 2010, 210: 26-32. (  0) 0) |
| [23] |
YAO Y, GAO B, ZHANG M, et al. Effect of Biochar Amendment on Sorption and Leaching of Nitrate, Ammonium and Phosphate in a Sandy Soil[J]. Chemosphere, 2012, 89(11): 1467-1471. DOI:10.1016/j.chemosphere.2012.06.002 (  0) 0) |
| [24] |
李雅竹. 氮、磷面源污染生物炭控制技术[D]. 湘潭: 湖南科技大学, 2014. LI Ya-zhu. Control Technology of Nitrogen and Phosphorus Non-Point Source Pollution With Biochar[D]. Xiangtan: Hunan University of Science and Technology, 2014. (  0) 0) |
| [25] |
张涛, 宋新山. 潜流人工湿地理化性质及不同形态氮素的空间分布[J]. 生态环境学报, 2010, 19(6): 1343-1347. ZHANG Tao, SONG Xin-shan. Physicochemical Character and Nitrogen Changes in Subsurface Flow Constructed Wetland[J]. Ecology and Environmental Sciences, 2010, 19(6): 1343-1347. (  0) 0) |
| [26] |
李扬, 李锋民, 张修稳, 等. 生物炭覆盖对底泥污染物释放的影响[J]. 环境科学, 2013, 34(8): 3071-3078. LI Yang, LI Feng-min, ZHANG Xiu-wen, et al. Effects of Biochar Covering on the Release of Pollutants From Sediment[J]. Environmental Science, 2013, 34(8): 3071-3078. (  0) 0) |




