2. 环境保护部南京环境科学研究所, 江苏 南京 210042
2. Nanjing Institute of Environmental Sciences, Ministry of Environmental Protection, Nanjing 210042, China
节肢动物群落在农田生态系统中有重要作用, 尤其是昆虫群落更是为农田生态系统提供了多种生态服务功能[1]。不同作物甚至不同品种间的田间节肢动物群落都会有所不同, 通过对田间节肢动物群落组成成分的调查, 可以在一定程度上反映不同农田生态系统的差异。近年来, 转基因作物在全球范围内大面积推广种植, 据国际农业生物技术应用服务组织(The International Service for the Acquisition of Agri-biotech Applications, ISAAA)统计, 2015年全球28个国家选择种植转基因作物, 种植面积达1.797亿hm2, 比1996年增长100倍以上[2]。转基因作物大面积推广种植的同时, 科学评估其对生态环境可能产生的影响也越来越受到关注[3-7], 其中对田间节肢动物的影响就是一个重要指标。
关于转基因作物对节肢动物的影响已有很多报道, 主要集中在水稻、大豆、甜菜这几类作物上。对转Bar基因水稻稻田生态系统的研究发现, 转基因抗除草剂水稻对于稻田节肢动物生物多样性存在一定影响, 但是还没有发现普遍规律[8-11]。有研究显示转基因抗除草剂大豆对田间节肢动物无显著影响[12-13], 转抗虫基因Cry1Ac大豆同样也没有对节肢动物群落产生不利影响[14]。另外还有研究显示, 转基因抗除草剂的甜菜对田间节肢动物无显著影响[15]。至今大部分研究结果都倾向于转基因作物对田间节肢动物没有显著的不利影响, 但也有一部分研究显示转基因作物会对田间节肢动物群落产生一些影响[3, 16]。由此可见, 不同转基因作物对于同种节肢动物的影响具有明显的差异, 同种转基因作物对不同节肢动物的影响也存在差异。对于任何转基因作物品种来说, 遵循“逐案(case by case)”原则进行相关研究是对其安全性研究的必要步骤。
目前我国已有一批拥有自主知识产权的转基因玉米(Zea Mays)材料, 在这些新材料进行田间释放和获得环境安全证书之前, 有必要对其可能产生的生态环境影响进行评价[17-18]。笔者于2015年玉米生长季系统调查了转基因耐草甘膦(EPSPS)草铵膦(pat)玉米C0010.1.1田间节肢动物种类和数量, 通过对比转基因玉米与对照农田中节肢动物群落多样性与结构, 研究了转基因玉米对田间节肢动物的影响, 为转基因耐除草剂玉米的生态安全评价提供科学支持。
1 材料与方法 1.1 实验地点、材料及取样时间研究样地位于中国吉林省四平市伊通满族自治县(43°15′ N, 125°19′ E)。供试玉米材料为转基因耐草甘膦/草铵膦玉米转化体C0010.1.1、受体玉米品种178和常规玉米品种先玉335。上述材料均由北京大北农生物技术有限公司提供。取样时间为2015年6月24日至2015年9月23日。
1.2 实验处理及小区设计依据农业部953号公告—10.4—2007 《转基因植物及其产品环境安全检测抗虫玉米第4部分:生物多样性影响》、农业部953号公告—11.4—2007 《转基因植物及其产品环境安全检测抗除草剂玉米第4部分:生物多样性影响》和NY/T 720.3—2003 《转基因玉米环境安全监测技术规范第3部分:对生物多样性影响的检测》, 实验小区设置采用随机区组排列。小区大小为10 m×15 m, 小区之间设有1.0 m的隔离带。玉米按条播方式进行播种, 行距60 cm, 株距25 cm。实验处理包括喷施除草剂(参考有关专利, 剂量为2倍剂量, 将除草剂草甘膦施用量为420 g·hm-2定为1倍剂量)与未喷施除草剂的转基因玉米、未喷施除草剂的受体玉米品种和未喷施除草剂的常规玉米(以上3组未喷施除草剂的处理进行定期人工除草), 每个处理重复3次。实验全生育期(2015年6月7日至2015年9月30日)不喷施杀虫剂。
1.3 实验方法对未喷施和喷施除草剂的转化体C0010.1.1、受体品种178及常规品种先玉335全生育期均进行调查。每小区采用对角线5点取样, 采用以下2种方法进行调查。
1.3.1 直接观察调查法在田间直接观察并记录植株上节肢动物种类和数量。从定苗10 d至成熟, 每7 d调查1次, 每取样点调查10株玉米。记录玉米植株上所有节肢动物的种类及其发育阶段。对田间不能识别的种类进行编号, 带回室内鉴定。
1.3.2 陷阱调查法用于调查地表节肢动物的种类和数量。在玉米定苗后10 d开始至成熟, 每14 d调查1次。每取样点埋设3个陷阱(7 cm×8 cm), 间隔0.5 m, 杯中放有φ为5%的洗涤剂水, 水量为杯容积的1/3, 过夜后调查杯中的节肢动物种类和数量。不易识别的种类进行编号, 带回室内鉴定。
1.4 数据分析根据各个类群数量占总数的百分比, 将调查发现的节肢动物进行多度等级划分, 即该类群个体数占总个体数的百分比>10%为优势类群, 1%~10%为常见类群, < 1%为稀有类群[19-20]。用节肢动物群落的多样性指数、均匀性指数、优势集中性指数和群落相似性系数4个指标, 分析比较各玉米材料田间节肢动物群落的动态。各指标计算方法为
| $ D = 1-\sum\limits_{i = 1}^n {\frac{{{N_i}\left( {{N_i}-1} \right)}}{{N\left( {N-1} \right)}}}, $ | (1) |
| $ H =-\sum\limits_{i = 1}^S {{P_i}\ln {P_i}}, $ | (2) |
| $ R = \left( {S-1} \right)/\ln N, $ | (3) |
| $ J = H/\ln \mathit{S, } $ | (4) |
| $ \mathit{C = }\sum\limits_{i = 1}^n {{{\left( {{N_i}/N} \right)}^2}}, $ | (5) |
| $ \mathit{C}'2w/\left( {a + b} \right)。$ | (6) |
式(1)~(6)中, D为Simpson多样性指数; Ni为第i个物种的个体数; N为总个体数; H为Shannon-Wiener多样性指数; Pi为Ni/N比值; R为Margalef指数; S为物种数; J为均匀性指数; C为优势集中性指数; C′为相似性系数; w为A、B群落样本中同物种较小个体数的总和; a、b分别为A、B群落样本中所有物种个体数总和。
符合正态分布的变量使用t检验对2组数据的差异显著性进行分析, 采用单因素方差分析(one-way AVOVA)对转基因玉米、受体玉米和常规玉米之间的差异进行分析; 对于不能确定其分布的变量, 采用非参数检验分析其差异;2组数据使用Mann-Whitney检验, 多于2组数据则采用Kruskal-Wallis检验。显著性水平均设为0.05。
2 结果与分析 2.1 田间节肢动物主要类群和功能群供试玉米材料调查结果表明, 2015年全生育期玉米植株上的节肢动物群落由13目、41科节肢动物组成(表 1)。
|
|
表 1 玉米田间节肢动物数量在不同目、科的分布 Table 1 Patterns of arthropod from maize field in different orders and families |
2015年全生育期内玉米田间节肢动物群落中主要功能群统计结果见表 2。玉米材料上的主要害虫是蚜虫科(Aphididae)、叶甲科(Chrysomelidae), 捕食性节肢动物主要为草蛉科(Chrysopidae)、瓢虫科(Coccinellidae)和蜘蛛科(Araneida)等。相比先玉335和受体178, 转化体C0010.1.1的功能群未表现出明显差异。
|
|
表 2 整个生育期玉米材料上主要功能群中各物种累计数量 Table 2 The accumulated number of each species in main functional groups on maize materials during the whole growing period |
转化体C0010.1.1喷施2倍草甘膦除草剂后第2周和第4周, 对其田间节肢动物种类及数量进行调查发现, 先玉335小区蚜虫数量明显高于受体和转化体小区, 这也可能是导致以蚜虫为食的瓢虫数量有所差异的主要原因。在其他指标上, 与喷施除草剂处理的转化体C0010.1.1相比, 受体品种178、常规种先玉335和转化体C0010.1.1功能群在种类和数量上无显著差异(表 3)。
|
|
表 3 施药后2周和4周喷施2倍草甘膦后主要功能群中物种数量的变化 Table 3 The number of major functional groups at the time of 2 and 4 weeks after spraying glyposate |
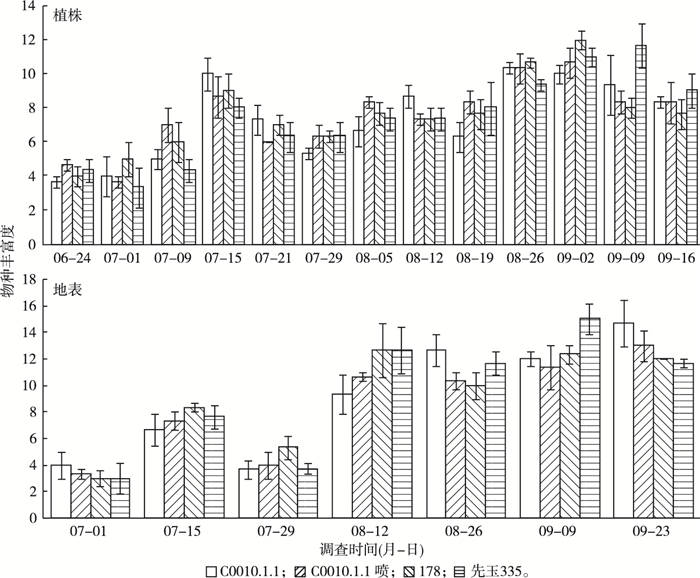
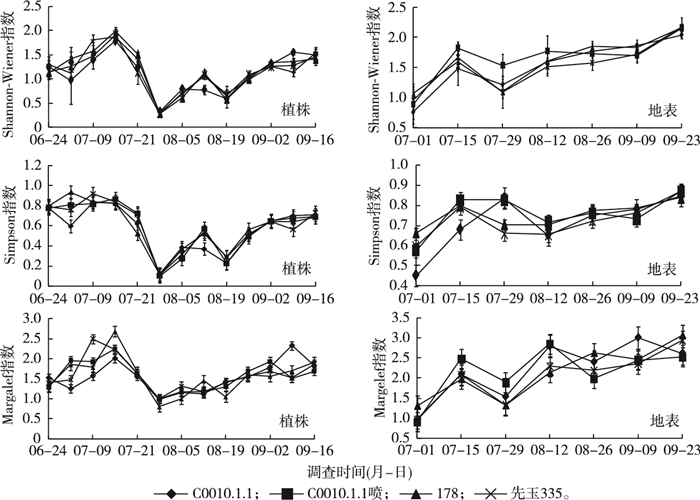
Shannon-Wiener指数、Simpson指数和Margalef指数均是反映农田系统中节肢动物发生情况的综合指数, 既包括该系统中节肢动物物种的丰富度(图 1), 又包括该群落结构的相关信息。通过分析得到3种玉米材料田间节肢动物多样性指数, 进一步得到这3种玉米材料田间节肢动物多样性在整个生育期的动态变化(图 2)。
|
图 1 田间节肢动物群落物种丰富度动态 Figure 1 The species richness dynamic of arthropod community in the fields C0010.1.1为转化体品种, C0010.1.1喷为喷施过除草剂的转化体, 178为受体品种, 先玉335为常规玉米品种。 |
|
图 2 田间节肢动物多样性指数动态 Figure 2 Dynamic of biodiversity index of arthropod community in the fields C0010.1.1为转化体品种, C0010.1.1喷为喷施过除草剂的转化体, 178为受体品种, 先玉335为常规玉米品种。 |
植株上节肢动物群落调查统计结果表明, 在6月底到7月中旬农田系统中节肢动物多样性指数较高, 其中Simpson指数较平稳, 而其余2个指数有明显的上升趋势, 这是因为稀有种增多; 7月底到8月初由于天气干旱少雨, 双斑萤叶甲(Monolepta hieroglyphica)大量暴发, 节肢动物的种类和数量出现波动, 多样性指数也出现波动, 急剧下降, 之后逐渐回升。由于8月之后蚜虫数量增长较多, 故多样性指数回升较缓慢。
地表节肢动物群落调查统计结果表明, 初期生物多样性指数较低, 之后逐渐增高。
总体来看, 3种多样性指数变化趋势相似, 各组数据无显著性差异, 转化体C0010.1.1与受体品种178、常规种先玉335的田间节肢动物群落多样性变化趋势一致, 转化体C0010.1.1对田间节肢动物多样性变化无显著影响。
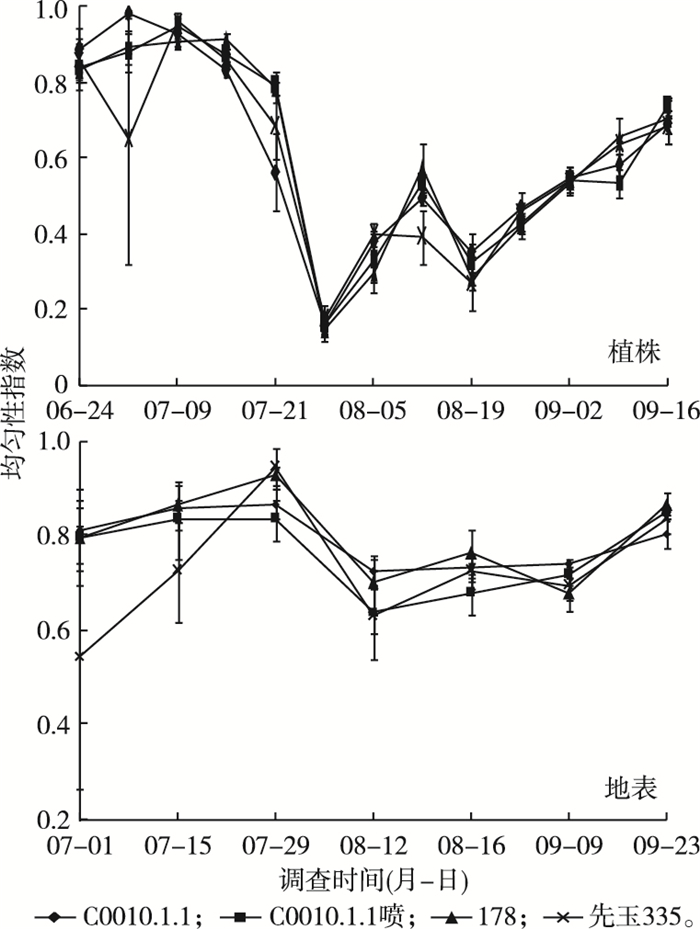
2.3 节肢动物群落均匀性变化3种玉米材料4个处理的田间节肢动物Pielou均匀性指数见图 3。植株和地表调查统计结果表明3种玉米材料的节肢动物群落均匀性变化大体一致。7月底, 玉米材料的田间节肢动物群落均匀性降至最低, 与双斑萤叶甲的暴发时间相符。植株和地表节肢动物群落均匀性指数变化趋势说明转化体C0010.1.1对节肢动物群落均匀性没有显著影响。
|
图 3 田间节肢动物物种均匀性动态 Figure 3 Dynamic of evenness index of field arthropod community C0010.1.1为转化体品种, C0010.1.1喷为喷施过除草剂的转化体, 178为受体品种, 先玉335为常规玉米品种。 |
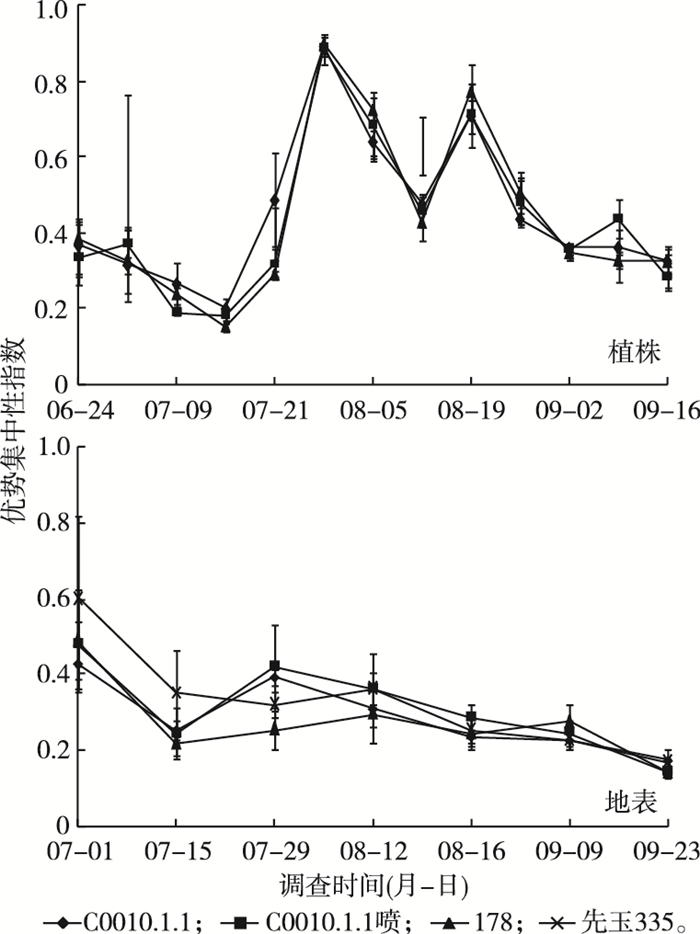
3种玉米材料4个处理的田间节肢动物优势集中性指数及其动态变化见图 4。植株上群落统计结果显示, 7月29日和8月19日3个玉米材料田间节肢动物的优势集中性指数分别达到峰值, 呈现双峰模式, 田间节肢动物群落优势类群集中在双斑萤叶甲和玉米蚜等几类上。
|
图 4 田间节肢动物优势集中性指数动态 Figure 4 Dynamic of dominant concentration index of field arthropod community C0010.1.1为转化体品种, C0010.1.1喷为喷施过除草剂的转化体, 178为受体品种, 先玉335为常规玉米品种。 |
这与3种玉米材料田间节肢动物的多样性指数变化正好相反, 反映了相同的变化趋势, 即节肢动物群落中物种数量明显下降, 个别物种个体数量增加。地表群落统计结果显示, 7月初地表节肢动物群落优势集中性指数较高, 之后呈缓慢下降趋势。3种玉米材料植株上节肢动物群落优势集中性变化趋势基本一致, 说明转化体C0010.1.1对节肢动物群落优势集中性方面没有显著影响。
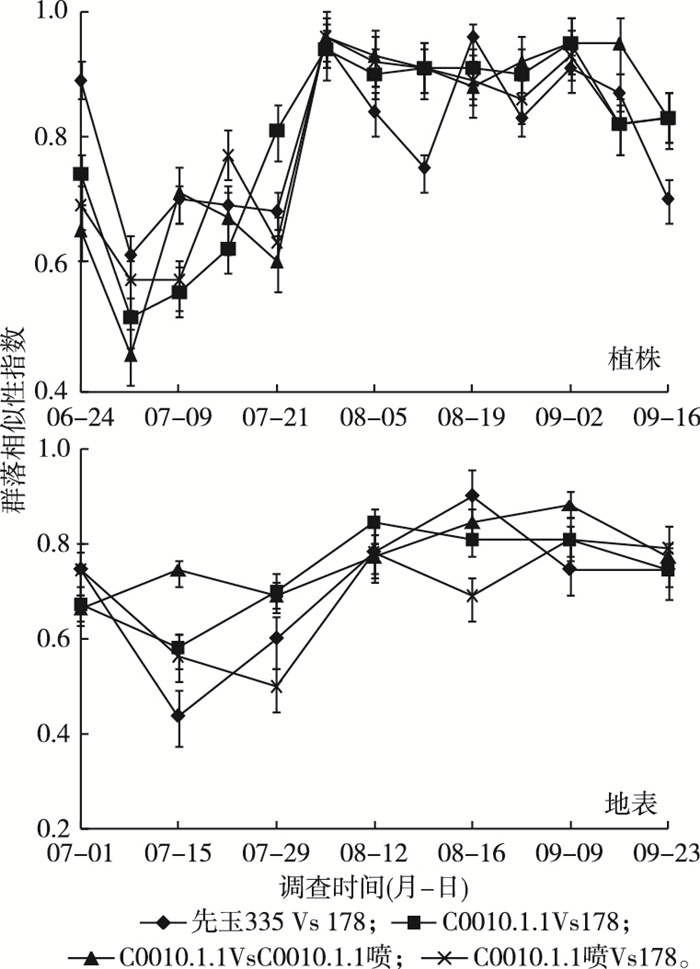
2.5 节肢动物群落相似性群落相似性系数的数值越接近1, 群落间相似性越高。通过调查常规种先玉335、受体品种178与转化体品种C0010.1.1田间节肢动物相同物种数量, 计算并绘制节肢动物群落相似系数变化图(图 5)。各组节肢动物群落相似性总体变化趋势一致, 喷施除草剂与未喷施除草剂的转化体, 未喷施除草剂的转化体与受体, 喷施除草剂的转化体与受体相比较, 除第1次调查外, 其植株上的节肢动物群落相似度均表现为初期较低, 之后明显上升, 后期维持在较高水平; 不同处理小区地表节肢动物群落相似度也有一致的表现。总体来看, 植株和地表上的节肢动物群落逐步趋于一致, 且地表上的群落相似性变化更为平缓。
|
图 5 田间节肢动物群落相似性动态 Figure 5 Dynamic of similarity index of field arthropod community C0010.1.1为转化体品种, C0010.1.1喷为喷施过除草剂的转化体, 178为受体品种, 先玉335为常规玉米品种。 |
近年来国内外在转基因作物的生态安全性评价方面已取得很大进展, 先后研究了转基因耐除草剂大豆、转基因抗虫棉花以及转基因抗虫水稻等对节肢动物群落结构的影响[13, 21-24]。国内研究最多的是转Bt基因抗虫棉对害虫和天敌的影响, 由于转基因玉米在我国尚未被批准商业化种植, 所以转基因玉米对节肢动物多样性影响的研究较少。目前尚无有力科学证据证明转基因作物对生物多样性的潜在影响是否与非转基因作物存在本质不同[5, 25]。从已有研究来看, 绝大多数实验结果都支持转基因耐除草剂作物对节肢动物多样性的影响较小。在美国佐治亚州(Georgia)南部进行大豆害虫种群调查的结果表明, 除了在个别取样时间发现转基因耐除草剂大豆对稻绿蝽(Nezara viridula)种群密度有影响外, 耐除草剂大豆对昆虫群落各物种影响极小[13]; 1997年和1998年在美国爱荷华州(Iowa)进行的研究也表明, 转基因大豆品种对昆虫群落没有显著影响[26]。在对耐除草剂油菜的调查中也得到了相似结果, 耐草铵膦油菜田的蜜蜂科(Apidae)、胡蜂科(wasp)等授粉昆虫多样性和密度与非转基因对照油菜田相似[27]; 转基因耐除草剂油菜田中弹尾目昆虫的全年总量较非转基因对照田大, 对其他无脊椎动物的影响极小[28]。转基因耐草铵膦甜菜田间杂食性节肢动物的稳定性调查结果表明, 除了某些采样时期的密度和物种组成在统计学上有差异外, 转基因处理与非转基因对照之间无显著差异[29]; STRANDBERG等[30]对转基因耐草甘膦甜菜田的调查研究表明, 第1次施用草甘膦的时间(即田间无除草剂的时间长短)对节肢动物生物多样性保护有重要作用。转Bar基因耐除草剂水稻Bar68-1对稻飞虱、叶蝉、盲蝽和蜘蛛田间自然种群的影响与非转基因水稻基本相同[31], 并且对稻田叶冠层节肢动物的群落组成和多样性无显著影响[32], 对稻纵卷叶螟(Cnaphalocrocis medinalis)自然种群的影响也与非转基因水稻基本一致[33]。
对转基因耐除草剂玉米田的研究也表明, 转基因玉米的种植与除草剂的施用没有对地表节肢动物产生任何有统计学意义的生态影响[34]; 连续种植转基因耐除草剂玉米对植物和无脊椎动物类群也不存在累积效应[35]。王尚等[36]研究表明, 无论是否喷施除草剂, 转基因玉米CC-2与其对应的非转基因对照郑58相比, 在田间节肢动物群落组成、群落结构以及田间主要节肢动物类群动态上均无显著差异。姜莹等[37]研究发现转EPSPS基因耐除草剂玉米CC-2对土壤动物群落无不利影响。目前转基因饲料也没有对畜禽营养、免疫、繁殖、肠道健康产生不利影响[38]。
同以上结果相似, 转基因玉米材料C0010.1.1在植株和地表的节肢动物生物多样性、群落优势集中性和群落均匀性等方面与对照相比均未发现显著差异。在目前的种植条件下, 该转基因材料对田间节肢动物群落的多样性及生物功能群物种数量和个体数量等没有显著影响。该结果还需要大量的相似研究来进一步明确, 并对其发生的原因和机制进行进一步的探究。
该研究中不同小区节肢动物群落多样性的变化趋势相似, 在7月中下旬出现明显波动, 结合气象记录和大田观察, 可以认为是干旱和双斑萤叶甲暴发而导致群落多样性水平下降, 这直接导致后续数据分析中优势集中度和均匀度的急剧变化, 双斑萤叶甲单个物种数量的变化对整体数据的分析产生了较大影响。在短期研究中, 个别害虫的集中暴发可能会对整个实验结果造成影响, 转基因作物的生态安全性评价还需要长期和全面的监测。除了节肢动物外, 对整个农田生态系统中的多个生态位的不同物种, 如土壤微生物, 进行监测会使结果更具有说服力[39-40]。另外, 在空间和时间上扩大监测尺度也能使结果更可信。环境影响指数(environmental impact quotient, EIQ)是评估有毒物质对环境影响的综合性指标, 其中包括对非靶标有机体的影响[41]。自大面积种植转基因作物以来, 美国耐除草剂大豆田间的环境影响指数明显减小, 种植转基因大豆并施用草甘膦对生态环境产生的压力明显小于种植转基因大豆之前[42]。BARFOOT等[43]对1996到2012年间全球转耐除草剂基因的大豆、玉米、棉花的田间EIQ指数的调查以及OLIVER等[44]对澳大利亚转耐除草剂基因的油菜(Brassica napus)的长期调查也得到了相似结果。这些国外研究者的工作也表明大田生物安全性评价研究的长期性和转基因生物大范围释放后监测的重要性。
转耐除草剂基因的玉米田间节肢动物群落在种类组成、数量和动态变化等方面与对照相比没有显著差异。在较短期的调查研究中, 期间某单种类物种(如双斑萤叶甲)的暴发可能会对实验结果产生较为重要的影响, 而为了得到更为可靠的结果, 需要更长期而广泛的研究确证, 即便是已获得国家证书商业化种植的品种也应进行持续监测。
| [1] |
戈峰, 欧阳芳, 赵紫华. 基于服务功能的昆虫生态调控理论[J]. 应用昆虫学报, 2014, 51(3): 597-605. GE Feng, OUYANG Fang, ZHAO Zi-hua. Ecological Management of Insects Based on Ecological Services at a Landscape Scale[J]. Chinese Journal of Applied Entomology, 2014, 51(3): 597-605. DOI:10.7679/j.issn.2095-1353.2014.071 (  0) 0) |
| [2] |
JAMESC. 2015年全球生物技术/转基因作物商业化发展态势[J]. 中国生物工程杂志, 2016, 36(4): 1-11. JAMES C. The Global Commercialization of Biotech Crops and Biotech Crop Highlights in 2015[J]. China Biotechnology, 2016, 36(4): 1-11. (  0) 0) |
| [3] |
LOSEY J E, RAYOR L S, CARTER M E. Transgenic Pollen Harms Monarch Larvae[J]. Nature, 1999, 399(6733): 214. (  0) 0) |
| [4] |
WOLFENBARGER L L, PHIFER P R. The Ecological Risks and Benefits of Genetically Engineered Plants[J]. Science, 2000, 290(5499): 2088-2093. DOI:10.1126/science.290.5499.2088 (  0) 0) |
| [5] |
DALE P J, CLARKE B, FONTES E M G. Potential for the Environmental Impact of Transgenic Crops[J]. Nature Biotechnology, 2002, 20: 567-574. (  0) 0) |
| [6] |
ANDOW D A, ZWAHLEN C. Assessing Environmental Risks of Transgenic Plants[J]. Ecology Letters, 2006, 9(2): 196-214. DOI:10.1111/j.1461-0248.2005.00846.x (  0) 0) |
| [7] |
ROMEIS J, BARTSCH D, BIGLER F, et al. Assessment of Risk of Insect-Resistant Transgenic Crops to Nontarget Arthropods[J]. Nature Biotechnology, 2008, 26: 203-208. DOI:10.1038/nbt1381 (  0) 0) |
| [8] |
APHIS (Animal and Plant Health Inspection Service), USDA. Docket No. 98-126-2: Availability of Determination of Nonregulated Status for Rice Genetically Engineered for Glufosinate Herbicide Tolerance[J]. Federal Register, 1999, 64(80): 22595.
(  0) 0) |
| [9] |
黄芊, 凌炎, 蒋显斌, 等. 转Bar基因水稻及草铵膦对褐飞虱取食和产卵行为的影响[J]. 南方农业学报, 2013, 44(7): 1110-1114. HUANG Qian, LING Yan, JIANG Xian-bin, et al. Impacts of Transgenic Tice With Bar Gene and Glufosinate on Feeding and Oviposition Behavior of Brown Planthopper, Nilaparvata lugens(Stål)[J]. Journal of Southern Agriculture, 2013, 44(7): 1110-1114. (  0) 0) |
| [10] |
蒋显斌, 黄芊, 凌炎. 利用黑肩绿盲蝽兼性取食特性评价转基因水稻生态风险[J]. 中国生物防治学报, 2016, 32(3): 311-317. JIANG Xian-bin, HUANG Qian, LING Yan, et al. Ecological Risk Assessment of Transgenic Rice by Using the Facultative Feeding of Cyrtorhinus lividipennis[J]. Chinese Journal of Biological Control, 2016, 32(3): 311-317. (  0) 0) |
| [11] |
谷荣辉, 成功, 李建钦, 等. 转基因水稻对土壤性质及土壤生物的影响[J]. 云南农业大学学报, 2014, 29(3): 448-457. GU Rong-hui, CHENG Gong, LI Jian-qin, et al. Effects of Transgenic Rice on Properties and Soil Organisms[J]. Journal of Yunnan Agricultural University, 2014, 29(3): 448-457. (  0) 0) |
| [12] |
BITZER R J, BUCKELEW L D, PEDIOGO L D. Effects of Transgenic Herbicide-Resistant Soybean Varieties and Systems on Surface-Active Springtails (Entognatha collembola)[J]. Environmental Entomology, 2002, 31(3): 449-461. DOI:10.1603/0046-225X-31.3.449 (  0) 0) |
| [13] |
MCPHERSON R M, JOHNSON W C, MULLINIX JR B G, et al. Influnce of Herbicide Tolerant Soybean Production Systems on Insect Pest-Induced Crop Damage[J]. Journal Economic Entomology, 2003, 96(3): 690-698. DOI:10.1093/jee/96.3.690 (  0) 0) |
| [14] |
YU H L, LI Y H, LI X J, et al. Arthropod Abundance and Diversity in Transgenic Bt Soybean[J]. Environmental Entomology, 2014, 43(4): 1124-1134. DOI:10.1603/EN13337 (  0) 0) |
| [15] |
VOLKMAR C, HUSSEIN L M, JANY D, et al. Ecological Studies on Epigeous Arthropod Populations of Transgenic Sugar Beet at Friemar (Thuringia, Germany)[J]. Agriculture, Ecosystems & Enviormnent, 2003, 95(1): 37-47. (  0) 0) |
| [16] |
韩兰芝, 白树雄, 赵建周, 等. 转基因抗虫棉花和玉米与节肢动物相关的生态安全性研究进展[J]. 昆虫学报, 2007, 50(7): 727-736. HAN Lan-zhi, BAI Shu-xiong, ZHOU Jian-zhou, et al. Progress in Ecological Biosafety of Insect-Resistant Transgenic Cotton and Corn in Relation to Arthropods[J]. Acta Entomologica Sinica, 2007, 50(7): 727-736. (  0) 0) |
| [17] |
DAVIS S. EPA Revokes Approval of Enlist Duo Herbicide to Study 'Synergistic Effects'. EB/OL]. 2016-09-26] http://www.agripulse.com/EPA-revokes-approval-of-Enlist-Duo-herbicide-to-studysynergistic-effects-11252015.asp.
(  0) 0) |
| [18] |
MANN R K, MASTERS R A, MCMASTER S, et al. Synergistic Herbicidal Weed Control From Combinations of 2, 4-D-Choline and Glyphosate[P]. U. S. Patent Appl 0173371 A1, 2015.
(  0) 0) |
| [19] |
梁文举, 闻大中. 土壤生物及其对土壤生态学发展的影响[J]. 应用生态学报, 2001, 12(1): 137-140. LIANG Wen-ju, WEN Da-zhong. Soil Biota and Its Role in Soil Ecology[J]. J]Chinese Journal of Applied Ecology, 2001, 12(1): 137-140. (  0) 0) |
| [20] |
王子健, 刘佳, 王尚, 等. 净月潭国家森林公园凋落物层土壤动物群落多样性[J]. 生态与农村环境学报, 2012, 28(4): 368-372. WANG Zi-jian, LIU Jia, WANG Shang, et al. Community Diversity of Litter Invertebrates in Jingyuetan National Forest Park of Changchun, China[J]. Journal of Ecology and Rural Environment, 2012, 28(4): 368-372. (  0) 0) |
| [21] |
吴奇, 彭德良, 彭于发. 抗草甘膦转基因大豆对非靶标节肢动物群落多样性的影响[J]. 生态学报, 2008, 28(6): 2622-2628. WU Qi, PENG De-liang, PENG Yu-fa. Effects of Herbicide Tolerant Soybean on Biodiversity of Non-Target Arthropods Communities[J]. Acta Ecologica Sinica, 2008, 28(6): 2622-2628. (  0) 0) |
| [22] |
LU Y H, WU K M, JIANG Y Y, et al. Mirid Bug Outbreaks in Multiple Crops Correlated With Wide-Scale Adoption of Bt Cotton in China[J]. Science, 2010, 328(5982): 1151-1154. DOI:10.1126/science.1187881 (  0) 0) |
| [23] |
雒珺瑜, 刘传亮, 张帅, 等. 转RRM2基因棉生长势和产量及对棉田节肢动物群落的影响[J]. 植物生态学报, 2014, 38(7): 785-794. LUO Jun-yu, LIU Chuan-liang, ZHANG Shuai, et al. Growth Vigour and Yield of Transgenic RRM2 (RNA Recognition Motif 2) Cotton and Their Effects on Arthropod Community in Cotton Field[J]. Chinese Journal of Plant Ecology, 2014, 38(7): 785-794. (  0) 0) |
| [24] |
季香云, 徐雪亮, 蒋杰贤, 等. 转Bt基因水稻"赣绿1号"对田间节肢动物群落的影响[J]. 应用昆虫学报, 2014, 51(3): 827-833. JI Xiang-yun, XU Xue-liang, JIANG Jie-xian, et al. Impact of Transgenic Bt Rice "Ganly 1" on an Arthropod Community[J]. Chinese Journal of Applied Entomology, 2014, 51(3): 827-833. DOI:10.7679/j.issn.2095-1353.2014.100 (  0) 0) |
| [25] |
CARPENTER J E. Impacts of GM Crops on Biodiversity[J]. GM Crops, 2011, 2(1): 7-23. DOI:10.4161/gmcr (  0) 0) |
| [26] |
BUCKELEW L D, PEDIGO L P, MERO H M, et al. Effects of Weed Management Systems on Canopy Insects in Herbicide-Resistant Soybeans[J]. Journal of Economic Entomology, 2000, 93(5): 1437-1443. DOI:10.1603/0022-0493-93.5.1437 (  0) 0) |
| [27] |
PIERRE J, MARSAULT D, GENECQUE E, et al. Effects of Herbicide-Tolerant Transgenic Oilseed Rape Genotypes on Honey Bees and Other Pollinating Insects Under Field Conditions[J]. Entomologia Experimentalis et Applicata, 2003, 108(3): 159-168. DOI:10.1046/j.1570-7458.2003.00081.x (  0) 0) |
| [28] |
BOHAN D A, BOFFEY C W H, BROOKS D R, et al. Effects on Weed and Invertebrate Abundance and Diversity of Herbicide Management in Genetically Modified Herbicide-Tolerant Winter-Sown Oilseed Rape[J]. Proceedings of the Royal Society of London B:Biological Sciences, 2005, 272(1562): 463-474. DOI:10.1098/rspb.2004.3049 (  0) 0) |
| [29] |
VOLKMAR C, HUSSEI L M, KREUTER T, et al. Does the Cultivation of Transgenic Sugar Beet Affect the Stability of Arthropod Coenoses (Results of a Four-Year Field Study)?[J]. Journal of Plant Diseases and Protection, 2002, 109: 1031-1038. (  0) 0) |
| [30] |
STRANDBERG B, PEDERSEN M B, ELMEGAARD N. Weed and Arthropod Populations in Conventional and Genetically Modified Herbicide Tolerant Fodder Beet Fields[J]. Agriculture, Ecosystems & Environment, 2005, 105(1/2): 243-253. (  0) 0) |
| [31] |
蒋显斌, 肖国樱. 抗除草剂转基因水稻对二种刺吸性害虫和二种天敌的影响[J]. 昆虫知识, 2010, 47(6): 1128-1133. JIANG Xian-bin, XIAO Guo-ying. Effects of Genetically Modified Herbicide Tolerant Rice (Oryza sativa) on Population Density of Two Sucking Insect Pests and Two Natural Enemies in Rice Fields[J]. Chinese Bulletin of Entomology, 2010, 47(6): 1128-1133. DOI:10.7679/j.issn.2095-1353.2010.202 (  0) 0) |
| [32] |
蒋显斌, 肖国樱. 转基因抗除草剂水稻对稻田叶冠层节肢动物群落多样性的影响[J]. 中国生态农业学报, 2010, 18(6): 1277-1283. JIANG Xian-bin, XIAO Guo-ying. Diversity of Arthropod Community in the Canopy of Genetically Modified Herbicide-Tolerant Rice (Oryza sativa L.)[J]. Chinese Journal of Eco-Agriculture, 2010, 18: 1277-1283. (  0) 0) |
| [33] |
蒋显斌, 肖国樱. 抗除草剂转基因水稻对稻纵卷叶螟田间自然种群的影响[J]. 植物保护, 2011, 37(2): 50-54. JIANG Xiao-bin, XIAO Guo-ying. Effects of Genetically Modified Herbicide-Tolerant Rice on Natural Populations of Rice Leaf Roller[J]. Plant Protection, 2011, 37(2): 50-54. (  0) 0) |
| [34] |
VOLKMAR C, HUSSEIN M, WETZEL T. Ecological Field Studies in Transgenic Maize at Friemar (Thuringia)[J]. Journal of Plant Diseases and Protection, 2004(19): 1017-1024. (  0) 0) |
| [35] |
HEARD M S, CLARK S J, ROTHERY P, et al. Effects of Successive Seasons of Genetically Modified Herbicide-Tolerant Maize Cropping on Weeds and Invertebrates[J]. Annals of Applied Biology, 2006, 149(3): 249-254. DOI:10.1111/aab.2006.149.issue-3 (  0) 0) |
| [36] |
王尚, 王柏凤, 严杜升, 等. 转EPSPS基因抗除草剂玉米CC-2对田间节肢动物多样性的影响[J]. 生物安全学报, 2014, 23(4): 271-277. WANG Shang, WANG Bai-feng, YAN Du-sheng, et al. Impacts of Transgenic Herbicide-Resistant Maize With EPSPS Gene on Arthropod Biodiversity in the Fields[J]. Journal of Biosafety, 2014, 23(4): 271-277. (  0) 0) |
| [37] |
姜莹, 王柏凤, 周琳. 转EPSPS基因抗除草剂玉米'CC-2'对土壤动物群落的短期影响[J]. 植物保护, 2017, 43(1): 34-39, 45. JIANG Ying, WANG Bai-feng, ZHOU Lin, et al. Impacts of Transgenic Herbicide-Resistant Maize With EPSPS Gene on Soil Fauna Community[J]. Plant Protection, 2017, 43(1): 34-39, 45. (  0) 0) |
| [38] |
陈亮, 黄庆华, 孟丽辉, 等. 转基因作物饲用安全性评价研究进展[J]. 中国农业科学, 2015, 48(6): 1205-1218. CHEN Liang, HUANG Qing-hua, MENG Li-hui, et al. Safety Evaluation of Feeds From Genetically Modified Crops on Livestock and Poultry[J]. Scientia Agricultura Sinica, 2015, 48(6): 1205-1218. DOI:10.3864/j.issn.0578-1752.2015.06.16 (  0) 0) |
| [39] |
刘玲, 杨殿林, 王生荣, 等. 转Bt基因玉米种植对土壤细菌数量及多样性的影响[J]. 生态与农村环境学报, 2011, 27(3): 42-47. LIU Ling, YANG Dian-lin, WANG Sheng-rong, et al. Effects of Transgenic Bt Maize on Populations and Diversity of Soil Bacteria[J]. Journal of Ecology and Rural Environment, 2011, 27(3): 42-47. (  0) 0) |
| [40] |
尹艳宁, 方志翔, 沈文静, 等. 转cry1Ac+cry2Ab基因棉对土壤细菌群落结构和功能多样性的影响[J]. 生态与农村环境学报, 2014, 30(2): 206-213. YIN Yan-ning, FANG Zhi-xiang, SHEN Wen-jing, et al. Impacts of Transgenic cry1Ac+cry2Ab Cotton on Community Structure and Functional Diversity of Soil Bacteria[J]. Journal of Ecology and Rural Environment, 2014, 30(2): 206-213. (  0) 0) |
| [41] |
KOVACH J, PETZOLDT C, DEGNI J, et al. A Method to Measure the Environmental Impact of Pesticides[J]. New York's Food and Life Sciences Bulletin, 1992(139): 8. (  0) 0) |
| [42] |
BONNY S. Herbicide-Tolerant Transgenic Soybean Over 15 Years of Cultivation:Pesticide Use, Weed Resistance, and Some Economic Issues.The case of the USA[J]. Sustainability, 2001, 3(9): 1302-1322. (  0) 0) |
| [43] |
BARFOOT P, BROOKES G. Key Global Environmental Impacts of Genetically Modified (GM) Crop Use 1996-2012[J]. GM Crops & Food, 2014, 5(2): 149-160. (  0) 0) |
| [44] |
OLIVER D P, KOOKANA R S, MILLER R B, et al. Comparative Environmental Impact Assessment of Herbicides Used on Genetically Modified and Non-Genetically Modified Herbicide-Tolerant Canola Crops Using Two Risk Indicators[J]. Science of the Total Environment, 2016, 557/558: 754-763. DOI:10.1016/j.scitotenv.2016.03.106 (  0) 0) |




