由于农业氮肥使用、畜牧业发展、污水灌溉和生活污水排放等原因, 地下水硝酸盐污染已经成为严重的全球性环境问题, 更重要的是对人体健康造成了严重的潜在威胁[1-2]。GB 5749—2006《生活饮用水卫生标准》规定以地下水为水源时硝酸盐质量浓度(以N计)限值为20 mg·L-1。因此, 开展地下水中硝酸盐的修复研究具有重要的现实意义。
原位生物反硝化因工艺简单、占地面积小、建设和运行费用低、处理效率高以及能源消耗小等优点, 受到国内外学者的普遍关注[3-4]。有机碳是异养反硝化所必需的电子供体和能量来源[5]。然而, 地下水中有机碳含量往往较低, 严重抑制了异养反硝化作用, 表现为含水层自净能力不强。为此, 以纤维素为基础的固体有机碳源的开发成为地下水原位生物反硝化的热点问题。树叶、木屑、秸秆、玉米芯、稻壳和芦苇等固体碳源已经被成功地应用于室内模拟研究甚至工程实践, 并取得了良好的修复效果[6-8]。尽管如此, 针对高浓度硝酸盐, 这些碳源缓慢的反硝化速率和释碳速率成为工程应用的限制性因素[9-10]。经腐熟后的堆肥物可以提供更多易利用的小分子有机物、更大的比表面积和更多的微生物附着点, 进而有望提高反硝化速率。另一方面, 有研究者发现, 零价铁与棉花联用可以增强生物反硝化能力, 主要缘于零价铁厌氧腐蚀产生阴极氢, 进而促进自养反硝化[11-12]。
该研究以地下水中硝酸盐为目标污染物, 利用柱实验模拟堆肥物和堆肥物与铁屑联用(以下简称堆肥物+铁屑)用于原位生物修复的动态过程, 考察生物反硝化的运行效果, 探讨水化学参数的变化, 分析硝酸盐的转化过程, 确认地下水流速和进水硝酸盐浓度的影响, 以期为拓展纤维素类固体有机碳源的种类,提高纤维素类固体有机碳源的反硝化速率,实现原位生物反硝化的工程实践提供理论依据和技术支持。
1 材料与方法 1.1 实验材料堆肥物:粒状, 粒径为0.15~0.45 mm, 暗褐色, pH值为7.8, 比表面积为1.38 m2·g-1, 阳离子交换量为55.6 cmol·kg-1, 主要以树枝、树叶、树皮和杂草为原料, 腐熟度(以终点和起点C/N比的比值计)为0.52, 4.0 ℃条件下保存。铁屑:粒状, 粒径为0.15~0.45 mm, 银白色。含水层介质:粒状, 粒径为0.15~0.45 mm, 取自抚顺市远郊区潜水含水层, 4.0 ℃条件下保存。卵石:粒状, 粒径为0.84~2.00 mm。模拟地下水配制方法:向1 L去离子水中投加NaNO3 130~418 mg、NH4Cl<0.2 mg、NaHCO3 376.4 mg、FeCl3·6H2O 0.6 mg、MgCl2·6H2O 45.0 mg、CaCl2·6H2O 24.3 mg、Na2MoO4·2H2O 0.6 mg、ZnSO4·10H2O 0.1 mg、NaNO2<0.1 mg、KH2PO4 96.5 mg、Na2EDTA 8.2 mg、MgSO4·7H2O 54.4 mg、NaCl 65.0 mg、CoCl2·6H2O 0.1 mg和MnCl2·4H2O 0.8 mg。采用Milli-Q(Millipore)超纯水(18.2 MΩ·cm)配制试剂溶液。如未特殊说明, 所有试剂均为分析纯。
1.2 接种菌液的静态培养与富集步骤1:向具盖棕色瓶内一次性投加去离子水、堆肥物、含水层介质和模拟地下水, 保证四者质量比为1: 1: 1: 9, 初始ρ(NO3-)为100 mg·L-1, 将棕色瓶置于恒温振荡培养箱(200 r·min-1, 15 ℃)中。步骤2:当水中硝酸盐完全消耗且无亚硝酸盐积累时, 立即取φ=10%的菌液移入另一棕色瓶, 再按顺序加入新鲜的堆肥物、含水层介质、模拟地下水, 保证四者质量比仍为1: 1: 1: 9, 初始ρ(NO3-)仍为100 mg·L-1。按照步骤2, 重复2~3次, 完成接种微生物的培养与富集, 备用。经PCR和16S rRNA分子生物学鉴定, 菌液中含有异养反硝化菌属(如Bacillus)、自养反硝化菌属(如Pseudomonas)以及好氧异养菌属(如Adhaeribacter)等。
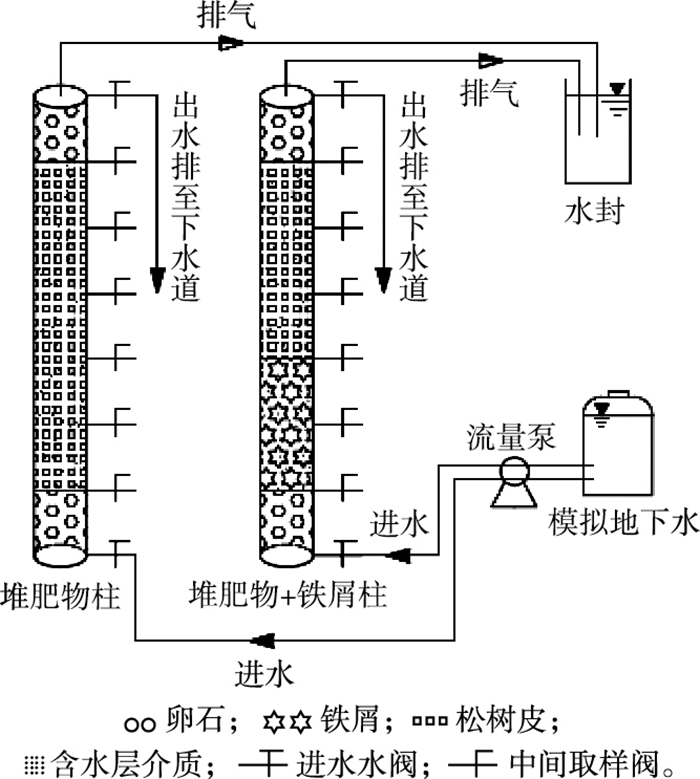
1.3 实验装置实验柱是自行设计的以渗透反应格栅为原型、有机玻璃为原料的圆柱形反应器, 内径8 cm, 高70 cm, 总体积3.52 L, 共计2根(图 1)。实验柱分为3个区域, 分别为布水区(高10 cm)、反应区(高50 cm)和出水区(高10 cm), 在布水区和出水区填充卵石。对于第1根柱(堆肥物柱), 在反应区填充堆肥物和含水层介质(质量比为1: 2, 混合均匀, 高50 cm); 对于第2根柱(堆肥物+铁屑柱), 在反应区水流上游填充铁屑和含水层介质(质量比为1: 2, 混合均匀, 高30 cm), 在下游填充堆肥物和含水层介质(质量比为1: 2, 混合均匀, 高20 cm)。沿柱高每间隔10 cm设置1个中间取样阀。
|
图 1 实验装置示意 Figure 1 Diagram of experimental apparatus |
首先, 关闭底部阀门, 由顶部阀门分别向堆肥物柱和堆肥物+铁屑柱投入接种菌液(占孔隙体积的35%~40%), 补充模拟地下水直至柱内饱水, 保证初始ρ(NO3-)为100 mg·L-1左右, 进行微生物静态挂膜, 历时3 d。其次, 通过底部阀门快速排空柱体, 每天1次, 并将排出的模拟水由顶部重新投入柱内, 促进生物膜(其中含异养反硝化菌和自养反硝化菌)在柱内均匀分布, 历时8 d。最后, 从12 d开始, 模拟地下水由底部阀门排出后经蠕动泵通过顶部阀门再次进入柱体, 进行微生物动态循环挂膜。在启动过程中, 硝酸盐消耗殆尽后向柱内及时补充硝酸盐, 确保底物充足。当取得稳定的硝酸盐去除率(>75%)时, 停止水循环, 完成挂膜, 启动结束, 历时16 d。
1.4.2 系统的稳定运行模拟地下水由柱底部进入堆肥物柱和堆肥物+铁屑柱, 流量由蠕动泵控制(BT100-1F, 保定兰格)。沿实验柱自下而上从进水端、中间取样口和出水端定期采集水样, 测定硝酸盐、亚硝酸盐、铵盐、总有机碳(TOC)、溶解氧(DO)浓度和pH值等。根据实验条件设定3个运行阶段(阶段Ⅰ、Ⅱ和Ⅲ), 具体运行条件见表 1。运行条件发生变化后, 实验柱连续进水5 d后开始累计运行时间。
|
|
表 1 实验柱各阶段的运行条件 Table 1 Operating conditions of the columns in different phases |
硝酸盐浓度采用紫外分光光度法测定(惠普8453, 美国)。亚硝酸盐浓度采用N-(1-萘基)乙二胺光度法测定(惠普8453, 美国)。铵盐采用钠氏试剂法测定(惠普8453, 美国)。pH值和水温由数显pH值计测定(赛多利斯PB-10, 德国)。DO浓度由便携式溶解氧仪测定(哈希HQ30d, 美国)。可溶性总铁浓度采用火焰原子吸收法测定(日立Z-5000, 日本)。室温由普通水银温度计测定。用于分析硝酸盐、亚硝酸盐、铵盐、DO、可溶性总铁浓度和pH值的水样均测试3次并计算标准偏差。
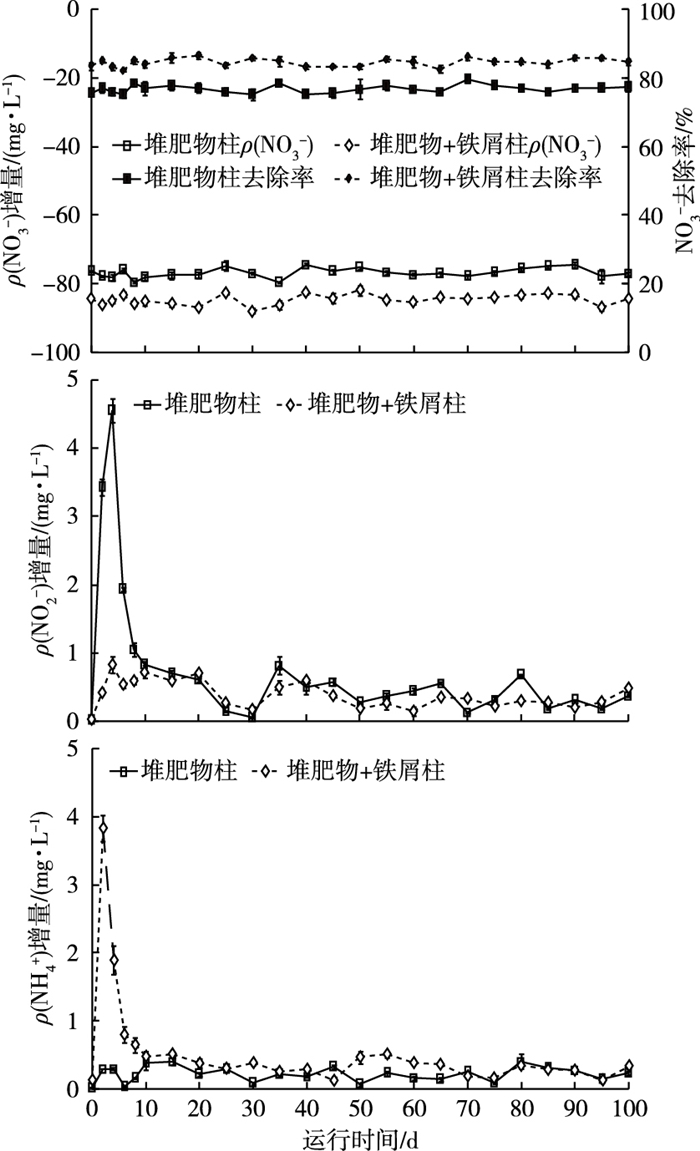
2 结果与讨论 2.1 反硝化效果评估由图 2可见,在阶段Ⅰ运行期间(0~100 d), 堆肥物柱出水ρ(NO3-)较进水大幅降低, 表现为ρ(NO3-)的负增量(-79.67~-74.43 mg·L-1)及高效的去除率(75.08%~79.57%); 出水ρ(NO2-)仅在运行初期(≤8 d)大幅增加, 增量>1.0 mg·L-1〔GB 5749—2006中ρ(NO2-)限值为1.0 mg·L-1〕, 最大值达4.55 mg·L-1; 出水ρ(NH4+)维持在较低水平, 增量介于0.01~0.40 mg·L-1之间。
|
图 2 阶段Ⅰ堆肥物柱和堆肥物+铁屑柱中反硝化效果随运行时间的变化 Figure 2 Changes in denitrification performances over operating time in the compost column and the compost+iron chip column in phase Ⅰ |
堆肥物+铁屑柱同样表现为ρ(NO3-)的负增量(-88.00~-82.00 mg·L-1)及高效的去除率(82.24%~86.48%); ρ(NO2-)增量较小, 最大值仅为0.84 mg·L-1; ρ(NH4+)增量却在运行初期(≤8 d)超过0.64 mg·L-1〔经换算, GB 5749—2006中ρ(NH4+)限值为0.64 mg·L-1〕。此外, 堆肥物柱和堆肥物+铁屑柱的反硝化速率分别为9.69和11.30 g·m-3·d-1(n=24), 显著高于锯屑的反硝化速率0.30 g·m-3·d-1[11]。可以看出, 堆肥物用于原位生物反硝化可行且高效, 堆肥物+铁屑更能增强NO3-的去除效果。在堆肥物柱内, 生物膜中异养反硝化菌以堆肥物作为有机碳源和电子供体, 以硝酸盐为电子受体, 将硝酸盐转化为亚硝酸盐、氮气等[10]。在堆肥物+铁屑柱内, 除了异养反硝化作用, 生物膜中自养反硝化菌还以铁屑腐蚀产生的阴极氢为电子供体, 将硝酸盐转化为其他形式[12]。因此, 与堆肥物柱中单一的异养反硝化作用相比, 堆肥物+铁屑柱中异养反硝化和自养反硝化耦合作用更有利于提高NO3-的去除率和反硝化速率。运行初期, 堆肥物易引起出水NO2-浓度超标, 然而堆肥物+铁屑易引起出水NH4+浓度超标。
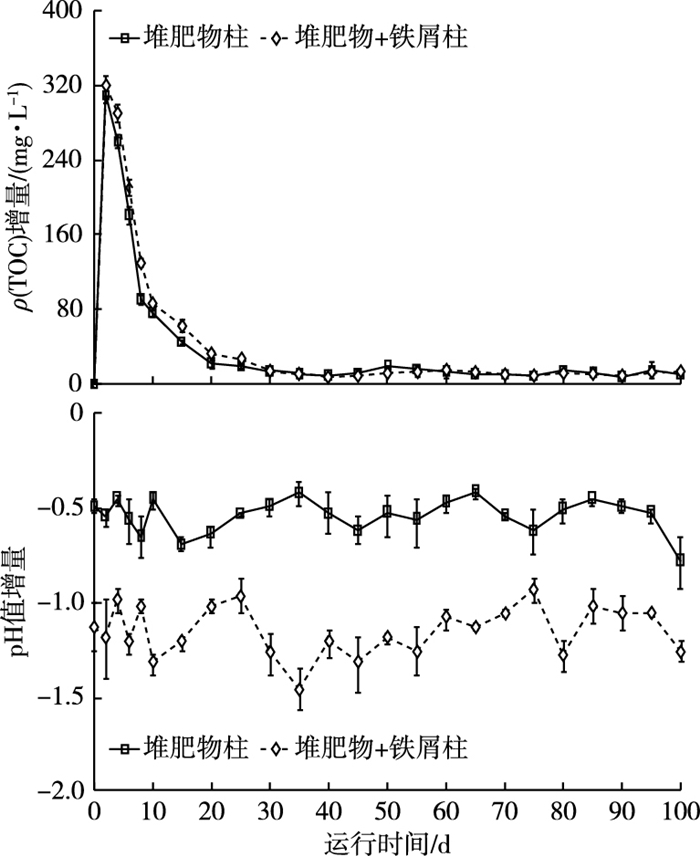
2.2 水化学参数的变化由图 3可见,对于堆肥物柱, 在阶段Ⅰ运行期间(0~100 d), 出水ρ(TOC)高于进水, 表现为ρ(TOC)的正增量; ρ(TOC)增量在运行之初(1 d)达到峰值(310.21 mg·L-1); 随着时间的增加(1~25 d), ρ(TOC)增量呈逐渐降低趋势; 25~100 d, ρ(TOC)增量始终维持在低水平(≤18.34 mg·L-1)。在运行初期(≤25 d), 出水中大量的TOC主要缘于易溶于水的物质及纤维素从堆肥物中迅速释放, 远远超过微生物的需求量。另一方面, 在运行期间(0~100 d), 出水pH值始终低于进水。
|
图 3 阶段Ⅰ堆肥物柱和堆肥物+铁屑柱中水化学参数随运行时间的变化 Figure 3 Changes in hydrochemical parameters over operating time in the compost column and the compost+iron chip column in phase Ⅰ |
堆肥物+铁屑柱ρ(TOC)和pH值的变化规律与堆肥物柱相似。但是, 堆肥物+铁屑柱中pH值的减量(0.93~1.45)远大于堆肥物柱(0.41~0.78)。此外, ρ(可溶性总铁)增量在8 d达到峰值(8.21 mg·L-1), 而16 d之后降低至0.14 mg·L-1。pH值减量和ρ(可溶性总铁)增量降低的原因之一是进水含有Cl-和SO42-, 与Fe2+及Fe3+反应生成H+和铁锈。
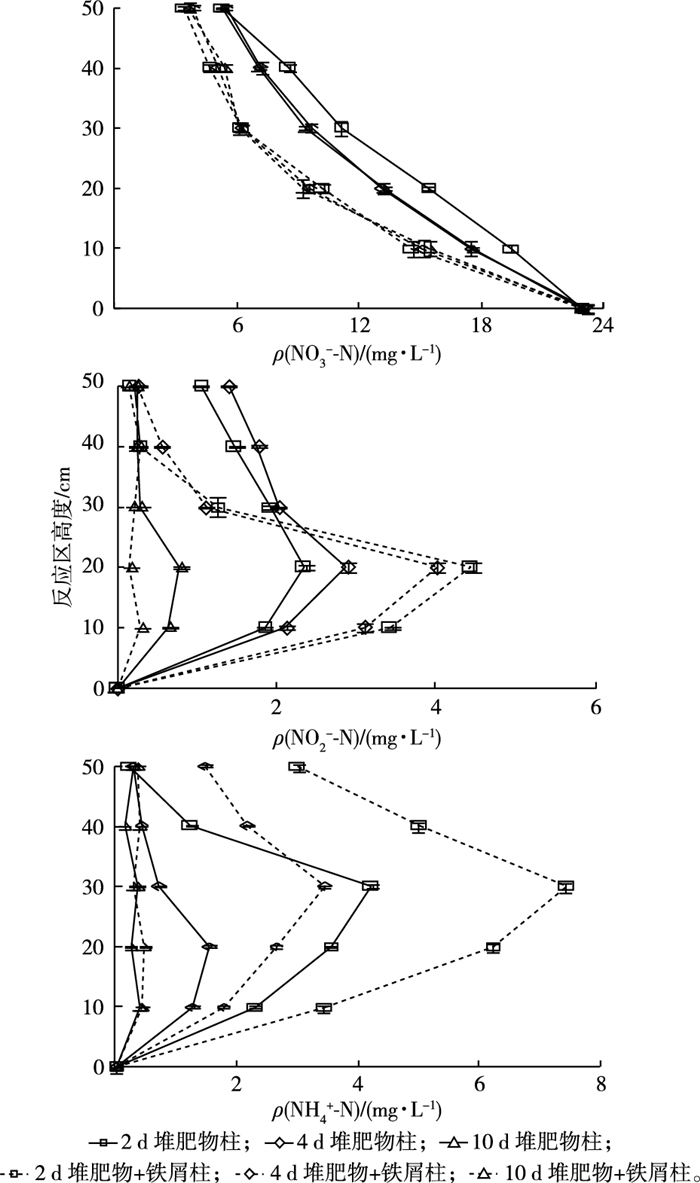
2.3 硝酸盐转化过程的分析由图 4可见,在阶段Ⅰ中,运行2、4和10 d时, 堆肥物柱中0~50 cm高度ρ(NO3--N)逐渐由23.0左右降低至<5.5 mg·L-1; ρ(NO2--N)在20 cm高度处达到峰值, 分别为2.36、2.89和0.78 mg·L-1, 在50 cm高度处分别降低至1.05、1.39和0.26 mg·L-1。
|
图 4 不同运行时间下堆肥物柱和堆肥物+铁屑柱中各形态氮在反应区内的空间变化 Figure 4 Changes in three nitrogens along the reaction zones in the compost column and the compost+iron chip column at the different operating time points |
运行2、4和10 d时, ρ(NH4+-N)分别在30、20和10 cm高度处达到峰值, 分别为4.23、1.56和0.42 mg·L-1, 在50 cm高度处分别降低至0.25、0.32和0.25 mg·L-1。运行2和4 d时, NH4+-N的产生缘于堆肥物含有有机氮, 其在脱氨基作用下发生了转化[13]; NH4+-N的减少缘于柱内含有厌氧氨氧化菌, 在其作用下发生了厌氧氨氧化反应(3NO3-+5NH4+→2N2+2H++9H2O)[14]。堆肥物+铁屑柱中不同高度NO3--N浓度明显低于堆肥物柱。运行2和4 d时, 0~20 cm高度NO2--N浓度明显高于堆肥物柱, 30~50 cm高度NO2--N浓度明显低于堆肥物柱, 说明铁屑改变了NO3--N转化的历程。运行10 d时, 0~50 cm高度NO2--N浓度并未明显高于堆肥物柱, 说明铁屑不再对NO3--N向NO2--N的转化产生影响。运行2和4 d时, 0~50 cm高度NH4+-N浓度明显高于堆肥物柱, 说明铁屑通过化学还原引起了NO3--N向NH4+-N的转化。从时间上看, 运行10 d时, 绝大部分NO3--N转化为气态氮。
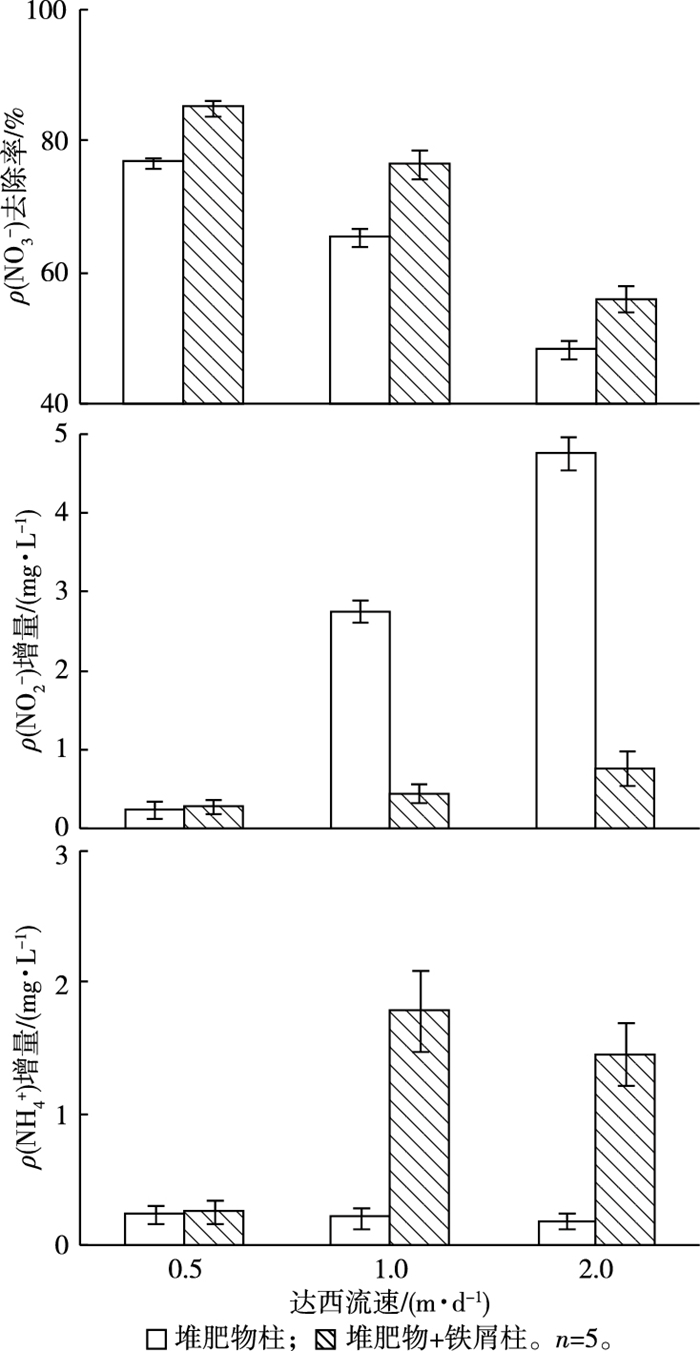
2.4 地下水流速的影响阶段Ⅱ反硝化效果与达西流速的关系见图 5。
|
图 5 阶段Ⅱ反硝化效果与达西流速的关系 Figure 5 Relationship between denitrification performance and Darcy velocity in phase Ⅱ |
由图 5可见,在阶段Ⅱ,对于堆肥物柱, 随着达西流速由0.5增加到2.0 m·d-1, NO3-去除率由76.84%降低至48.32%, ρ(NO2-)增量由0.25增加至4.75 mg·L-1, 而ρ(NH4+)增量则维持在0.18~0.24 mg·L-1之间。对于堆肥物+铁屑柱, 随着达西流速由0.5增加到2.0 m·d-1, NO3-去除率由85.22%降低至55.98%, ρ(NO2-)增量由0.28逐渐增加至0.77 mg·L-1, 而ρ(NH4+)增量则始终维持在0.25~1.78 mg·L-1之间。不难看出, 在既定结构尺寸和现有实验条件下, 从NO3-去除率和反硝化产物等角度考虑, 渗流速度显著影响堆肥物以及堆肥物+铁屑的生物反硝化效果。亚硝酸盐还原酶比硝酸盐还原酶对环境条件的变化敏感[15]。渗流速度越大, NO3-与异养和自养反硝化菌接触的时间越短, 对NO3-的去除越不利。
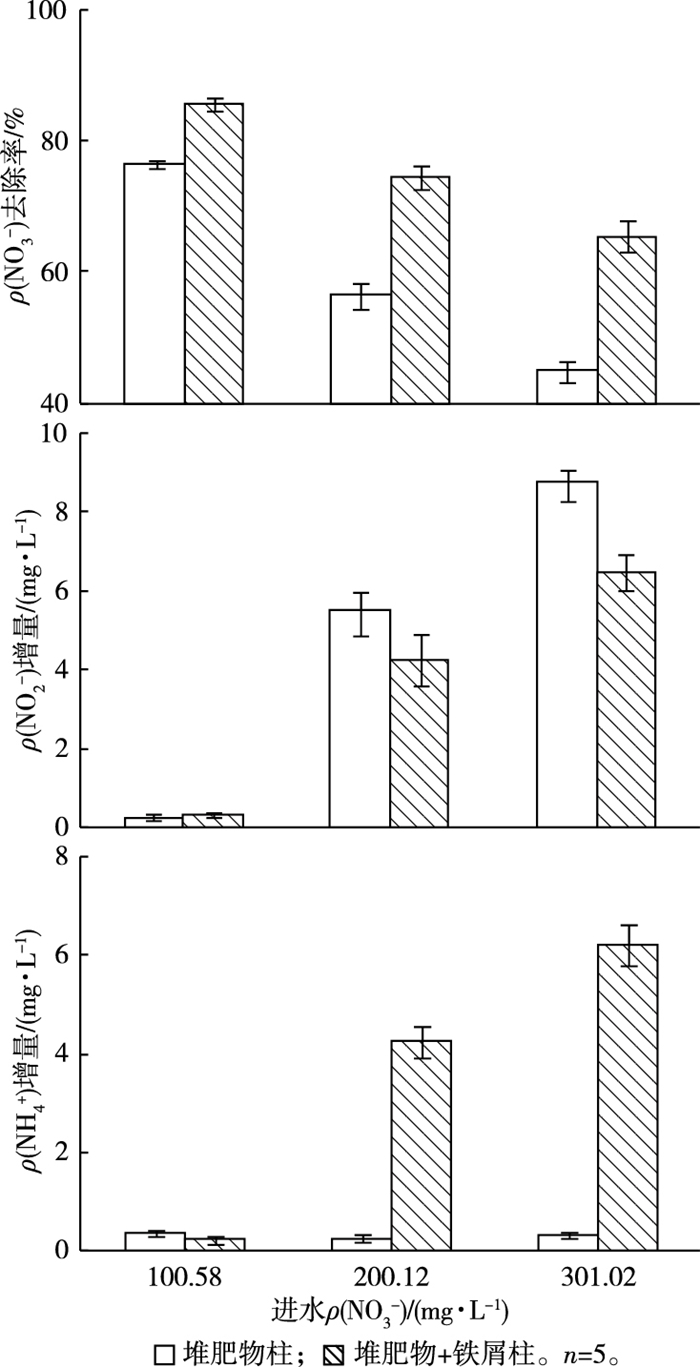
2.5 进水硝酸盐浓度的影响由图 6可见,在阶段Ⅲ对于堆肥物柱, 随着进水ρ(NO3-)由100.58增加到301.02 mg·L-1, NO3-去除率由76.44%降低至44.87%, ρ(NO2-)增量由0.23增加至8.75 mg·L-1, 而ρ(NH4+)增量则稳定维持在0.24~0.34 mg·L-1之间。
|
图 6 阶段Ⅲ反硝化效果与进水ρ(NO3-)的关系 Figure 6 Relationship between denitrification performance and influent NO3- concentration in phase Ⅲ |
对于堆肥物+铁屑柱, 随着进水ρ(NO3-)由100.58增加到301.02 mg·L-1, NO3-去除率由85.42%降低至65.46%, ρ(NO2-)增量由0.32增加至6.45 mg·L-1, 而ρ(NH4+)增量则由0.21增加至6.21 mg·L-1(图 6)。可以看出, 从NO3-去除率、ρ(NO2-)增量和ρ(NH4+)增量等角度考虑, 进水ρ(NO3-)显著影响堆肥物以及堆肥物+铁屑的生物反硝化效果。影响反硝化进程的环境因素主要有碳源、pH值、DO和水温等[16]。通过分析NO3-、TOC浓度和pH值的变化规律, 并结合实验柱在不同阶段的运行条件(表 1)可知, 这些环境因素不是导致去除率降低的原因。事实上, 随着进水底物浓度的增加, 反硝化菌数量和生物膜厚度亦增加, 反而造成生物膜内部深处的微生物活性降低和新陈代谢下降[17], 从而引起去除率下降。进水硝酸盐浓度越大, 底物越充足, 硝酸盐还原酶活性越大, 从而导致硝酸盐反硝化速率大于亚硝酸盐反硝化速率的现象越明显, 亚硝酸盐积累越严重。在高浓度下, 为了获得理想的去除率和减少亚硝酸盐的生成量, 可以考虑减少地下水流速和(或)增加反应区厚度, 以进一步增加水力停留时间。另一方面, 进水硝酸盐浓度增大之后, 硝酸盐与零价铁的活性点位接触机会增多, 被零价铁化学还原的硝酸盐增多, 进而导致氨氮的生成量增大。
3 结论(1) 堆肥物用于原位生物反硝化可行且高效(去除率为75.08%~79.57%), 而且堆肥物+铁屑更能增强NO3-的去除效果(去除率为82.24%~86.48%)。在运行初期(≤8 d), 堆肥物易引起出水NO2-浓度超标, 然而堆肥物+铁屑易引起出水NH4+浓度超标。
(2) 堆肥物和堆肥物+铁屑引起的ρ(TOC)增量在运行后期(25~100 d)维持在低水平; 出水pH值在运行期间(0~100 d)始终低于进水值。运行至10 d时, 堆肥物以及堆肥物+铁屑将绝大部分NO3--N转化为气态氮。
(3) 渗流速度显著影响堆肥物以及堆肥物+铁屑的生物反硝化效果。随着达西流速由0.5增加到2.0 m·d-1, 堆肥物柱的去除率由76.84%降低至48.32%, 堆肥物+铁屑柱的去除率由85.22%降低至55.98%。
(4) 进水NO3-浓度显著影响堆肥物以及堆肥物+铁屑的生物反硝化效果。随着进水ρ(NO3-)由100.58增加到301.02 mg·L-1, 堆肥物柱的去除率由76.44%降低至44.87%, 堆肥物+铁屑柱的去除率由85.42%降低至65.46%。
| [1] |
侯卫龙, 周鸿翔, 施加春, 等. 碳源、温度及水力停留时间对地下水硝酸盐的去除效果[J]. 浙江大学学报(农业与生命科学版), 2014, 40(3): 314-321. HOU Wei-long, ZHOU Hong-xiang, SHI Jia-chun, et al. Effects of Carbon Sources, Temperature and Hydraulic Retention Time on Nitrate Removal From Groundwater[J]. Journal of Zhejiang University(Agriculture & Life Sciences), 2014, 40(3): 314-321. DOI:10.3785/j.issn.1008-9209.2013.10.252 (  0) 0) |
| [2] |
张建美, 郝会玲. 地下水硝酸盐生物处理技术研究进展[J]. 长江大学学报(自科版), 2014, 11(1): 24-27. ZHANG Jian-mei, HAO Hui-ling. The Progress of Bioremediation for Removal Nitrate From Groundwater[J]. Journal of Yangtze University(Natural Science Edition), 2014, 11(1): 24-27. (  0) 0) |
| [3] |
ELEFSINIOTIS P, LI D. The Effect of Temperature and Carbon Source on Denitrification Using Volatile Fatty Acids[J]. Biochemical Engineering Journal, 2006, 28(2): 148-155. DOI:10.1016/j.bej.2005.10.004 (  0) 0) |
| [4] |
KHAN I A, SPALDING R F. Enhanced In-situ Denitrification for a Municipal Well[J]. Water Research, 2004, 38(14/15): 3382-3388. (  0) 0) |
| [5] |
董林, 张胜花, 马璐瑶, 等. 基于固态碳源强化作用下的反硝化系统应用研究进展[J]. 水处理技术, 2015, 41(9): 7-13. DONG Lin, ZHANG Sheng-hua, MA Lu-yao, et al. Research Progress on the Applications of Denitrifying Installations Using Solid Organic Matters as Carbon Sources[J]. Technology of Water Treatment, 2015, 41(9): 7-13. (  0) 0) |
| [6] |
徐锁洪, 施巍. 以稻壳为载体培养反硝化菌及硝酸盐氮的去除[J]. 大连铁道学院学报, 2001, 22(4): 98-101. XU Suo-hong, SHI Wei. Nitrate Removal and Denitrification Bacteria Cultivation Using Rice Chaff as a Medium[J]. Journal of Dalian Railway Institute, 2001, 22(4): 98-101. (  0) 0) |
| [7] |
邵留, 徐祖信, 金伟, 等. 农业废物反硝化固体碳源的优选[J]. 中国环境科学, 2011, 31(5): 748-754. SHAO Liu, XU Zu-xin, JIN Wei, et al. Optimization of Solid Carbon Source for Denitrification of Agriculture Wastes[J]. China Environmental Science, 2011, 31(5): 748-754. (  0) 0) |
| [8] |
张雯, 张亚平, 尹琳, 等. 以10种农业废弃物为基料的地下水反硝化碳源属性的实验研究[J]. 环境科学学报, 2016, 37(5): 1787-1797. ZHANG Wen, ZHANG Ya-ping, YIN Lin, et al. The Characteristics of Carbon sources for Denitrification in Groundwater From Ten Kinds of Agricultural Wastes[J]. Acta Scientiae Circumstantiae, 2016, 37(5): 1787-1797. (  0) 0) |
| [9] |
杨延梅, 吴鹏宇. 秸秆堆肥腐殖土PRB修复地下水硝酸盐污染研究[J]. 水资源保护, 2016, 32(6): 93-97. YANG Yan-mei, WU Peng-yu. Remidiation of Nitrate Pollution of Groundwater With Straw Compost Humus PRB[J]. Water Resources Protection, 2016, 32(6): 93-97. (  0) 0) |
| [10] |
FERNÁNDEZ-NAVA Y, MARAÑÍN E, SOONS J, et al. Denitrification of High Nitrate Concentration Wastewater Using Alternative Carbon Sources[J]. Journal of Hazardous Materials, 2010, 173(1/2/3): 682-688. (  0) 0) |
| [11] |
DELLA R C, BELGIORNO V, MERIC S. An Heterotrophic/Autotrophic Denitrification (HAD) Approach for Nitrate Removal From Drinking Water[J]. Process Biochemistry, 2006, 41(5): 1022-1028. DOI:10.1016/j.procbio.2005.11.002 (  0) 0) |
| [12] |
TILL B A, WEATHERS L J, ALVAREZ P J J. Fe(0)-Supported Autotrophic Denitrification[J]. Environmental Science & Technology, 1998, 32(5): 634-639. (  0) 0) |
| [13] |
DESIMONE L A, HOWES B L. Nitrogen Transport and Transformations in a Shallow Aquifer Receiving Wastewater Discharge:A Mass Balance Approach[J]. Water Resources Research, 1998, 34(2): 271-285. DOI:10.1029/97WR03040 (  0) 0) |
| [14] |
朱明石, 周少奇. 厌氧氨氧化-反硝化协同脱氮研究[J]. 化工环保, 2008, 28(3): 214-217. ZHU Ming-shi, ZHOU Shao-qi. Study on Anaerobic Ammonium Oxidation-Denitrification Synergistic Interaction[J]. Environmental Protection of Chemical Industry, 2008, 28(3): 214-217. (  0) 0) |
| [15] |
李思倩, 路立, 王芬, 等. 低温反硝化过程中pH对亚硝酸盐积累的影响[J]. 环境化学, 2016, 35(8): 1657-1662. LI Si-qian, LU Li, WANG Fen, et al. Effect of pH on Nitrite Accumulation During Denitrification at Low Temperature[J]. Environmental Chemistry, 2016, 35(8): 1657-1662. DOI:10.7524/j.issn.0254-6108.2016.08.2016011105 (  0) 0) |
| [16] |
李桂荣, 薛素勤, 方虎, 等. 生物滴滤池不同进水负荷处理生活污水试验研究[J]. 水处理技术, 2011, 37(11): 84-87. LI Gui-rong, XUE Su-qin, FANG Hu, et al. Study on Different Influent Loading of Bio-Tricking Filter[J]. Technology of Water Treatment, 2011, 37(11): 84-87. (  0) 0) |
| [17] |
张耀斌, 吴广华, 邢亚彬, 等. COD进水浓度对SBMBBR脱氮除磷效果影响[J]. 大连理工大学学报, 2008, 48(3): 329-333. ZHANG Yao-wu, WU Guang-hua, XING Ya-bin, et al. Effect of COD Concentration on Phosphorus and Nitrogen Removal in SBMBBR[J]. Journal of Dalian University of Technology, 2008, 48(3): 329-333. DOI:10.7511/dllgxb200803004 (  0) 0) |




