2. 中国科学院南京地理与湖泊研究所/湖泊与环境国家重点实验室, 江苏 南京 210008
2. State Key Laboratory of Lake Science and Environment/Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, Nanjing 210008, China
通过一系列的诸如风化作用、矿物分解、生物活动的自然过程和人类活动如开采矿业、耕种农田和生产制造等过程砷被排进地表水中, 造成自然水体和地下水污染[1-2]。砷含量超标已对人类健康构成巨大威胁。为了减少饮用水中砷含量, 世界卫生组织建议水中砷的最大质量浓度为10 μg·L-1。因此, 发展经济、有效、可靠的除砷技术至关重要。
砷在水溶液中主要有五价砷(Ⅴ)和三价砷(Ⅲ)2种存在形态, 后者具有更大的毒性、易溶解性和不稳定性[3-4]。在氧化态条件下, pH值小于6.9时, 带负电荷H2AsO4-是砷的主要存在形式, 然而在pH值高于6.9时, HAsO42-则是主要的存在形式。对于三价砷, 在还原态条件下, pH值小于9时, H3AsO3是主要的存在形式[5]。目前, 水体中砷的去除方法有凝结/沉淀法、吸附法和薄膜法。相比而言, 吸附法由于其具有简单、高效和经济性的特点, 被广泛应用于废水中砷的吸附[6]。在过去的几十年里, 人们研制了各种砷吸附剂, 这些吸附剂可分为基于纳米材料的铁和锆氧化物或者二元氧化物、树脂负载纳米材料、工业副产品、生物炭或改性生物炭和改性矿石[7-9]。
近些年来, 利用廉价易得的黏土矿物作为改性媒介吸附污染物已成为一种趋势。如姚乐[10]采用硫酸和高分子絮凝剂二甲基二烯丙基氯化铵(PDMDAAC)对膨润土进行改性处理, 在实际废水中ρ(砷)为1.97 mg·L-1时, 改性膨润土对砷的去除率达97%以上; 符浩等[11]利用硅藻土负载铁氧化物研究了对砷(Ⅲ)的吸附特性, 发现改性硅藻土对砷(Ⅲ)的最大吸附量达16 mg·g-1; XU等[12]基于氯化铝制备改性沸石, 显著提高了对水体中砷(Ⅴ)的吸附。
海泡石是一类含水富镁硅酸盐矿物, 这类矿物具有2:1型层链状结构, 并且具有抗盐性、流动性强以及表面积大等特点, 被广泛应用于石油化工、环境保护等领域[13]。有研究报道, 我国现有的海泡石黏土矿物中含有较高的碳酸盐类钙质杂质, 其氧化钙含量达30%(又可称为富钙海泡石), 极大地降低了海泡石矿质品位, 而这种低品位的黏土矿物对磷、砷等表现出极好的吸附性能[14]。该研究主要基于热处理方法对原状富钙海泡石进行改性, 采用批处理与柱实验方法, 研究高温热处理富钙海泡石对水体砷(As3+和As5+)的吸附特征以及pH值、竞争阴离子等对其吸附特征的影响。
1 材料与方法 1.1 材料的制备及分析材料:取自河南兴源的富钙海泡石, 105 ℃条件下烘干, 机械粉碎(过0.106 mm孔径筛)处理后, 置于马弗炉中, 不同温度(200~1 000 ℃)下煅烧2 h, 取出后自然冷却至室温, 放入干燥箱中贮存备用。
试剂:全部为分析纯, 用去离子水配制。砷标准溶液As(Ⅲ)储备液用一级纯As2O3配制, ρ(As3+)为1 g·L-1; As(Ⅴ)储备液用Na2HAsO4·7H2O配制, ρ(As5+)为1 g·L-1。
实验中用到的主要仪器包括:X-射线荧光光谱仪(ARL9800XP+, 美国赛默飞世尔科技有限公司), X-射线衍射仪(MiniFlex 600, 日本理学UItima Ⅳ型XRD仪), 扫描电子显微镜(SUPRATM 40/40VP, 美国赛默飞世尔科技有限公司), 电感耦合等离子质谱仪(ICAP-QC, 美国赛默飞世尔科技有限公司)。
1.2 热处理富钙海泡石对砷吸附性能的研究 1.2.1 材料的筛选准确称取0.5 g不同温度热改性的富钙海泡石, 置于50 mL聚四氟乙烯离心管中, 分别加入25 mL As3+和As5+溶液(400 mg·L-1), 调节溶液pH值至7, 25 ℃条件下置于恒温振荡器(QHZ-98A)中, 以180 r·min-1振荡24 h后, 7 500 r·min-1离心8 min(离心半径为20 cm), 取上清液, 再经0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
1.2.2 吸附等温线和吸附动力学吸附等温线:准确称取0.5 g热处理富钙海泡石, 置于50 mL聚四氟乙烯离心管中, 加入25 mL配制好的不同浓度As溶液(1、5、10、20、50、100、200、400、600和800 mg·L-1), 调节溶液pH值至7, 25 ℃条件下置于恒温振荡器(QHZ-98A)中, 以180 r·min-1振荡24 h后, 7 500 r·min-1离心8 min(离心半径为20 cm), 取上清液, 再经0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
吸附动力学:准确称取10 g热处理富钙海泡石, 置于1 000 mL锥形瓶中, 分别加入500 mL ρ为125 mg·L-1的As3+和As5+溶液, 调节溶液pH值至7, 在25 ℃条件下, 置于180 r·min-1恒温振荡器中, 每隔一段时间(0.16、0.5、1、2、4、8、16、24和32 h)取出1 mL溶液, 再经0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
1.2.3 粒径对砷吸附效果的影响准确称取0.5 g不同粒径(0~0.5、> 0.5~1.0和 > 1.0~2.0 mm)热处理富钙海泡石, 置于50 mL聚四氟乙烯离心管中, 分别加入25 mL As3+和As5+溶液(100 mg·L-1), 调节溶液pH值至7, 放入恒温振荡器中, 设置温度为25 ℃, 转速180 r·min-1。24 h后取出, 180 r·min-1离心8 min(离心半径为20 cm), 取上清液, 再经0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
1.2.4 pH值和阴离子对砷吸附特征的影响准确称取0.5 g热处理富钙海泡石于50 mL聚四氟乙烯离心管中, 加入25 mL的As3+和As5+溶液(100 mg·L-1), 将pH值调至1~12, 在25 ℃条件下置于180 r·min-1恒温振荡器中, 24 h后7 500 r·min-1离心8 min(离心半径为20 cm), 取上清液再经0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
准确称取0.5 g热处理富钙海泡石于50 mL聚四氟乙烯离心管中, 加入25 mL含有不同质量浓度(0~100 mg·L-1)竞争离子(SO42-、CO32-、PO43-)的100 mg·L-1的As3+和As5+溶液, 调节溶液pH值至7。25 ℃条件下置于180 r·min-1的振荡器中振荡24 h后, 7 500 r·min-1离心8 min(离心半径为20 cm), 用0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中砷浓度。
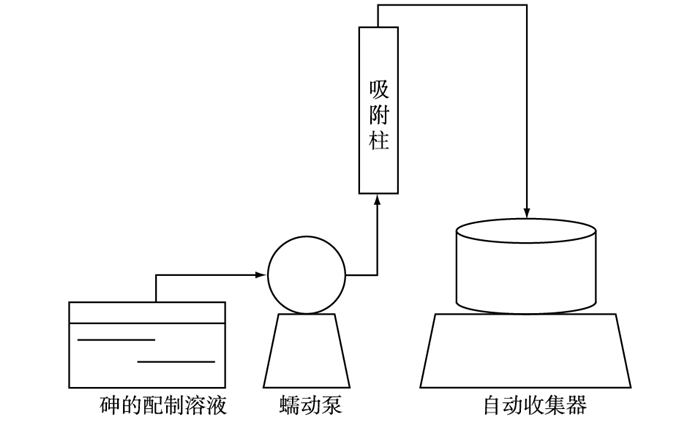
1.2.5 吸附材料对As3+和As5+的动态吸附图 1为动态吸附实验装置, 分为吸附柱、蠕动泵和自动样品收集器。吸附柱是一根长30 cm、内径15 mm的玻璃圆柱。称取2 g热处理富钙海泡石置于吸附柱中, 在富钙海泡石的下面和上面放入少量石英砂, 以避免吸附材料的散失。用去离子水分别配制ρ为200 μg·L-1的As3+和As5+溶液, 作为模拟实际废水中的砷浓度, 设置不同的流速让砷溶液在蠕动泵带动下, 从吸附柱的底部进入吸附柱, 由吸附柱顶部流出, 流出来的砷溶液每过一定时间(40 min)被自动收集器收集。收集的样品用0.45 μm孔径滤膜过滤, 用ICP-MS测定溶液中剩余砷的浓度。实验中以热处理富钙海泡石床体积(BV)为1个单元(1.81 mL)绘制吸附曲线。
|
图 1 动态吸附模拟装置 Figure 1 Dynamic adsorption simulation device |
分别采用Langmuir等温方程和Freundlich等温方程对实验数据进行非线性拟合。
Langmuir等温方程表达式为
| $ {q_{\text{e}}} = {q_{\text{m}}}b{C_{\text{e}}}/\left( {1 + b{C_{\text{e}}}} \right)。$ | (1) |
式(1) 中,qe为平衡吸附量,mg·g-1; Ce为平衡质量浓度,mg·L-1; qm为单位表面达到饱和吸附量的最大吸附量,mg·g-1; b为表征吸附表面强度的常数,L·mg-1。
Freundlich经验式为
| $ {q_{\text{e}}} = K{C_{\text{e}}}^{1/n}。$ | (2) |
式(2) 中,吸附系数K表示吸附能力的强弱,mg·g-1; 1/n表示吸附量随浓度增长的强度, 其值可表示吸附的难易。
分别采用准一级动力学模型和准二级动力学模型对动力学吸附过程进行拟合。
准一级动力学模型表达式为
| $ {\text{ln}}\left( {{q_{\text{e}}} - {q_t}} \right) = \ln {q_{\text{e}}}{\text{ - }}{{K}_{\text{1}}}t。$ | (3) |
准二级动力学模型表达式为
| $ t/{q_t} = 1/{K_2}{q_{\text{e}}}^2 + t/{q_{\text{e}}}。$ | (4) |
式(3)~(4) 中,qe和qt分别为吸附平衡和t时的吸附量,mg·g-1; K1为一级吸附速率常数,h-1;K2为二级吸附速率常数,g·(mg·h)-1。
2 结果与讨论 2.1 热处理富钙海泡石的结构特征由原状及热处理富钙海泡石的XRF分析可知, 原状富钙海泡石和热处理富钙海泡石的主要成分都是二氧化硅、氧化钙和氧化镁, w分别为32.1%、21.5%、20.4%和38.3%、34.7%、29.9%。热处理过程中大大提高了海泡石的氧化物含量, 这主要是由于有机物、碳酸盐类物质在高温条件下被烧结或者发生相态的转变。
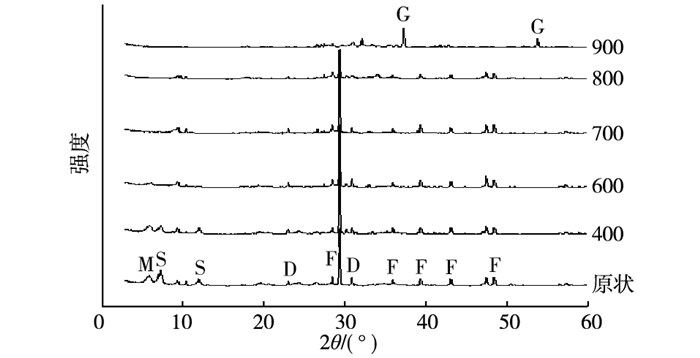
图 2为富钙海泡石在不同温度处理条件下的X-射线衍射(XRD)图谱。由图 2可知, 原状海泡石矿物主要成分为蒙脱石(M)、白云石(D)、海泡石(S)和方解石(F), 这与YIN等[15]的研究结果相似。热处理会明显改变富钙海泡石的组成, 随着热处理温度的升高, 除方解石(F)外其他成分的衍射峰明显减弱, 800 ℃时原矿物衍射峰基本消失, 表明矿物发生分解, 取而代之生成了如氧化钙(G)、氢氧化钙以及钙硅等化合物。理论上, 这些化合物对磷、砷等具有较高的吸附能力。
|
图 2 富钙海泡石的XRD图 Figure 2 XRD graphs of natural and modified calcium-rich sepiolite M—蒙脱石;S—海泡石;D—白云石;F—方解石;G—氧化钙及钙硅化合物。 |
图 3为原状富钙海泡石和热处理富钙海泡石的扫描电镜图。原状富钙海泡石呈现聚集在一起的棒状结构。热处理过程是富钙海泡石的棒状结构发生了显著变化, 由棒状的纤维结构变为层状的细纤维结构, 表面为紧凑多孔结构, 内部为更小的纤维结构, 热处理过程除去了富钙海泡石内部的水分, 使部分孔道坍塌, 纤细结构更加明显。

|
图 3 富钙海泡石的扫描电镜(SEM)图 Figure 3 SEM graph of calcium-rich sepiolite |
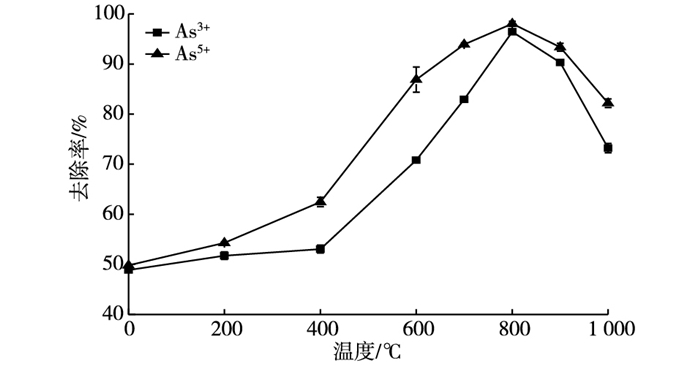
图 4为不同温度(200~1 000 ℃)热处理富钙海泡石对砷的吸附效果。
|
图 4 不同温度热处理富钙海泡石对砷的吸附效果 Figure 4 Arsenic adsorption of modified calcium-rich sepiolite relative to modification temperature |
热处理能够增加富钙海泡石对砷的去除效率。热处理改性富钙海泡石对As5+吸附效果比较明显。在改性温度低于800 ℃时, 随着改性温度的增大, 富钙海泡石对As3+和As5+吸附效果均显著增强, 且在改性温度为800 ℃时, 富钙海泡石对As3+和As5+的吸附效果达最大值, 最大去除率分别为96.44%和98.05%。若再增加改性温度,富钙海泡石对As3+和As5+的吸附去除率均会下降。实验采用的是800 ℃热处理富钙海泡石, 这是由于在该温度下海泡石的化学成分发生了巨大转变, 生成的钙氧化合物较多。若再升高改性温度,富钙海泡石对砷的去除率逐渐下降, 这可能是因为海泡石的内部孔道塌陷, 减少了比表面积以及可交换态的活性成分。
热处理富钙海泡石之所以能增强对砷(As3+和As5+)的吸附效果可能与加热过程中富钙海泡石的结构和组成成分发生变化有关。在改性温度为800 ℃时, 材料中的方解石和白云石发生分解, 生成氧化钙, 增强对砷的吸附能力。随着改性温度的增高, 生成的氧化钙可能会与材料中的二氧化硅结合成硅酸盐, 从而降低其吸附性能。
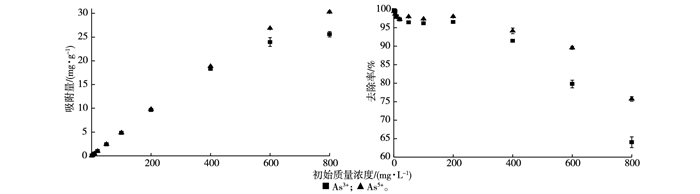
2.3 吸附等温线和吸附动力学图 5为热处理富钙海泡石对As3+和As5+的吸附等温线。在初始质量浓度低于600 mg·L-1时, 吸附量曲线的斜率较大, 即热处理富钙海泡石对As3+和As5+的吸附量增加较快; 高于600 mg·L-1时, 砷的吸附量增加很小, 吸附曲线的斜率较为平稳; 热处理富钙海泡石对As3+和As5+的去除率随着砷初始浓度的增大而逐渐降低, 但是对As3+和As5+的吸附量逐渐增大, 最大吸附量分别为25.61和30.30 mg·g-1。
|
图 5 砷在热处理富钙海泡石上的吸附等温线 Figure 5 As adsorption isotherm of modified calcium-rich sepiolite |
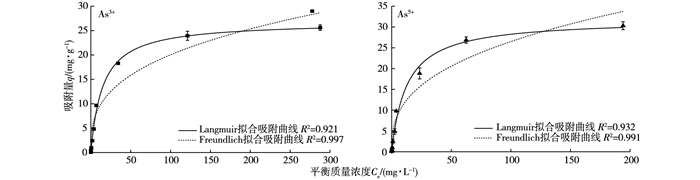
热处理富钙海泡石对As3+和As5+等温线的拟合曲线见图 6,等温线拟合曲线参数值见表 1。热处理富钙海泡石对As3+和As5+的吸附能够很好地拟合Langmuir吸附等温线, 决定系数R2均大于0.990, 具有很高的相关性, 而对Freundlich公式的拟合不是很理想, 表明热处理富钙海泡石对砷的吸附为单分子层吸附。
|
图 6 热处理富钙海泡石对砷吸附等温线拟合曲线 Figure 6 Fitting curve of As adsorption isotherm of modified calcium-rich sepiolite |
|
|
表 1 热处理富钙海泡石对砷Langmuir和Freundlich吸附等温式拟合参数 Table 1 Fitting parameters of Langmuir and Freundlich adsorption isotherm euqations for As adsorption on modified calcium-rich sepiolite |
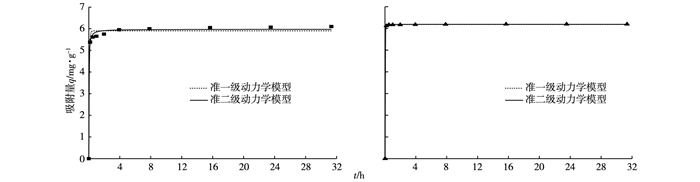
热处理富钙海泡石对As3+和As5+的动力学吸附曲线见图 7,动力学拟合曲线的参数值见表 2。热处理富钙海泡石对As3+和As5+的吸附效率很高, 在10 min内基本达到吸附饱和。准一级和准二级动力学模型对热处理富钙海泡石吸附As3+的拟合参数都在0.990以上, 但是准二级动力学模型拟合更好, 表明热处理富钙海泡石对As3+的吸附更符合准二级动力学方程, 且主要为化学吸附过程; 2种动力学模型对热处理富钙海泡石对As5+的拟合度非常好, 均在0.999以上, 表明热处理富钙海泡石对As5+的吸附不仅是单纯的化学吸附,还有物理吸附。
|
图 7 热处理富钙海泡石对砷吸附动力学拟合曲线 Figure 7 Fitting curve of As adsorption dynamics of modified calcium-rich sepiolite |
|
|
表 2 热处理富钙海泡石对砷动力学拟合曲线参数 Table 2 Fitting parameters of arsenic adsorption dynamics of modified calcium-rich sepiolite |
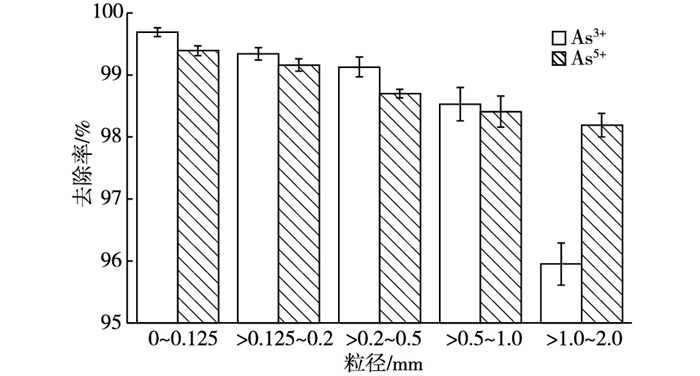
粒径的大小会影响吸附材料对吸附质的吸附性能, 图 8为热处理富钙海泡石粒径对As3+和As5+的吸附影响。由图 8中可知, 热处理富钙海泡石对As3+和As5+的去除率会随着粒径的增大而逐渐降低, 但是下降趋势不同, 粒径的改变对As3+的去除效果更明显, 而对As5+的影响不大。
|
图 8 粒径对热处理富钙海泡石吸附砷的影响 Figure 8 Effect of particle size on arsenic adsorption capacity of modified calcium-rich sepiolite |
吸附剂材料的比表面积是影响吸附性能的重要因素, 随着热处理富钙海泡石粒径的增大, 其比表面积会逐渐减少, 能够提供的吸附位变少, 相应的吸附量也会减小。粒径小于2.0 mm时, 粒径的大小对热处理富钙海泡石吸附As5+的影响很小, 基本上没有影响, 这一研究对吸附材料的实际应用具有重大意义。热处理富钙海泡石实地净化受污染的水体时, 粒径的大小将会影响净化效果, 若粒径太小, 容易在水体中形成悬浮物, 造成水体的再次污染。粒径为 > 1.0~2.0 mm时, 热处理富钙海泡石对砷(Ⅴ)仍有较好的去除效果, 因此实际应用中可以选用粒径较大的热处理富钙海泡石。
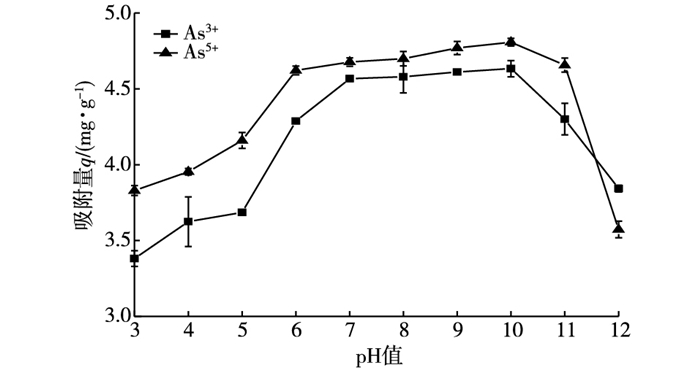
2.5 pH值对砷吸附的影响溶液的pH值能够改变吸附剂表面的特点, 从而影响吸附剂材料的吸附性能[16]。如图 9所示, 溶液pH值对热处理富钙海泡石对As3+和As5+去除率有显著影响。
|
图 9 pH值对热处理富钙海泡石对砷吸附效果影响 Figure 9 Effect of pH on arsenic adsorption capacity of modified calcium-rich sepiolite |
当pH值为1~7时, 随着pH值的增加,热处理富钙海泡石对As3+和As5+的吸附量增加; 当pH值为7~11时, 热处理富钙海泡石对As3+和As5+的吸附量变化不大, 吸附量达到最大值; 当pH值高于11时, 热处理富钙海泡石对As3+和As5+的吸附量开始下降。
原状富钙海泡石的等电点(pHpzc)大约在6.9左右, 热处理过程减少了富钙海泡石中部分羟基, 造成富钙海泡石等电点增大, 800 ℃改性的富钙海泡石pHpzc大约为10.02[17]。在水体中, As3+和As5+的主要存在形式为H2AsO3-和H2AsO4-离子, 当pH值为 > 6~10时富钙海泡石表面带有正电荷, 与H2AsO3-和H2AsO4-离子相互吸引, 易于形成亚砷酸盐〔Ca3(AsO3)2〕和砷酸盐〔Ca3(AsO4)2〕;当pH值小于6时, 吸附表面生成的钙亚砷酸盐和砷酸盐易分解, 重新生成H2AsO3-和H2AsO4-离子, 使得溶液中砷离子浓度增加, 吸附量降低; 当pH值大于10时, 富钙海泡石带有负电荷, 与H2AsO3-和H2AsO4-离子之间存在排斥力, 不易生成亚砷酸盐和砷酸盐, 富钙海泡石对砷的吸附量降低。
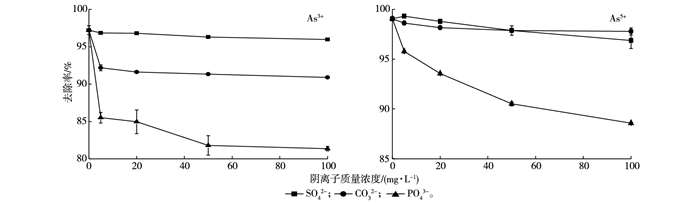
2.6 共存阴离子对砷吸附的影响在实际的自然水体中, 常存在一些阴离子如CO32-、SO42-和PO43-等, 这些阴离子可能会附着在吸附剂表面的反应点位上, 降低吸附剂的吸附量。CO32-、SO42-和PO43-离子对热处理富钙海泡石吸附砷的影响如图 10所示。
|
图 10 不同浓度竞争离子对热处理富钙海泡石吸附砷的影响 Figure 10 Effects of competitive ions on arsenic adsorption capacity of modified calcium-rich sepiolite |
CO32-和SO42-对热处理富钙海泡石吸附As3+的影响较小, 而PO43-对吸附As3+的影响较大。这些共存阴离子对热处理富钙海泡石吸附As5+的影响相似, 溶液中PO43-降低了As5+在热处理富钙海泡石上的吸附, 这可能是由于P和As位于同一主族, PO43-具有和As5+相似的分子结构, 因此, 共存PO43-可能强烈地和As5+竞争吸附剂表面的吸附点位, 造成As5+在热处理富钙海泡石上的吸附量降低。这与ZHANG等[18]研究的阴离子对纳米氧化铁/氧化铜吸附水体中砷的影响相似。
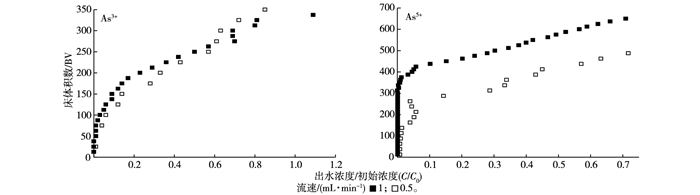
2.7 热处理富钙海泡石对砷动态吸附的影响我国GB 3838—2002《地表水环境质量标准》中规定Ⅲ类及以上地表水ρ(砷)最大值为0.05 mg·L-1, 该实验模拟的热处理富钙海泡石对实际废水中砷吸附过程中, 设置C/C0=0.25作为临界值, 即当出水ρ(砷)达0.05 mg·L-1时为突破点。图 11为模拟热处理富钙海泡石吸附实际废水中砷的动态吸附曲线图。
|
图 11 热处理富钙海泡石对砷的吸附效果曲线 Figure 11 Curve of As adsorption of modified calcium-rich sepiolite |
对于模拟热处理富钙海泡石对As3+的动态吸附实验, 溶液流速对As3+的动态吸附有显著影响, 流速为0.5和1 mL·min-1时达到设定C/C0值的BV数分别为220和170;同样, 溶液流速会影响As5+的动态吸附, 当流速为0.5和1 mL·min-1时达到设定C/C0值的BV数分别为450和310。随着溶液流速的增加, 到临界值的BV数逐渐降低, 这说明热处理富钙海泡石能用于农村低浓度砷污染水体的处理。
3 结论(1) 热处理过程能改变富钙海泡石的组成成分和晶体结构。在高温处理过程中, 海泡石的孔道结构发生了崩塌, 部分孔道被堵塞, 纤维结构更加明显; 800 ℃热处理使得富钙海泡石发生分解, 生成钙氧化物及钙硅化合物, 增加了表面活性位, 有利于对砷的吸附。
(2) 热处理富钙海泡石显著提高了砷的吸附性能。800 ℃热处理富钙海泡石对As3+和As5+的吸附等温线更符合Langmuir公式, 最大吸附量分别为25.61和30.30 mg·g-1, 决定系数R2均在0.990以上; As3+动力学吸附拟合符合准二级动力学模型, As5+动力学吸附符合准一级动力学模型和准二级动力学模型, 决定系数均大于0.999。
(3) 粒径对热处理富钙海泡石吸附砷的影响较小; 热处理富钙海泡石对砷吸附的最适pH值范围为6~11;共存离子中PO43-对热处理富钙海泡石吸附砷的影响最大; 流速能够影响热处理富钙海泡石对砷的动态吸附, 不同流速下出水量达到临界值的BV数不同, 这对于热处理富钙海泡石在农村低浓度砷污染水体中的应用有重要意义。
| [1] |
LI W G, GONG X J, WANG K, et al. Adsorption Characteristics of Arsenic From Micro-Polluted Water by an Innovative Coal-Based Mesoporous Activated Carbon[J]. Bioresource Technology, 2014, 165: 166-173. DOI:10.1016/j.biortech.2014.02.069 (  0) 0) |
| [2] |
CHAMMUI Y, SOOKSAMITI P, NAKSATA W, et al. Removal of Arsenic From Aqueous Solution by Adsorption on Leonardite[J]. Chemical Engineering Journal, 2014, 240: 202-210. DOI:10.1016/j.cej.2013.11.083 (  0) 0) |
| [3] |
XIA Y J, LIU J. An Overview on Chronic Arsenism via Drinking Water in China[J]. Toxicology, 2004, 198(1/2/3): 25-29. (  0) 0) |
| [4] |
SUN G F. Arsenic Contamination and Arsenicosis in China[J]. Toxicology and Applied Pharmacology, 2004, 198(3): 268-271. DOI:10.1016/j.taap.2003.10.017 (  0) 0) |
| [5] |
BHATTACHARYA P. Arsenic in Hydrological Processes:Sources, Speciation, Bioavailability and Management[J]. Journal of Hydrology, 2014, 518(Part C): 279-283. (  0) 0) |
| [6] |
YOUN Y K, SIM H S, KIM J Y, et al. Epidemiology and Control of an Outbreak of Vancomycin-Resistant Enterococci in the Intensive Care Units[J]. Yonsei Medical Journal, 2009, 50(5): 637-643. DOI:10.3349/ymj.2009.50.5.637 (  0) 0) |
| [7] |
梁美娜. 铁、铝及其复合氢氧化物去除水中砷(Ⅴ)的吸附研究[D]. 桂林: 桂林工学院, 2006. http://cdmd.cnki.com.cn/Article/CDMD-10596-2008042343.htm
(  0) 0) |
| [8] |
于志红, 黄一帆, 廉菲, 等. 生物炭-锰氧化物复合材料吸附砷(Ⅲ)的性能研究[J]. 农业环境科学学报, 2015, 34(1): 155-161. DOI:10.11654/jaes.2015.01.022 (  0) 0) |
| [9] |
BISWAS B K, INOUE J I, INOUE K, et al. Adsorptive Removal of As(Ⅴ) and As(Ⅲ) From Water by a Zr(Ⅳ)-Loaded Orange Waste Gel[J]. Journal of Hazardous Materials, 2008, 154(1/2/3): 1066-1074. (  0) 0) |
| [10] |
姚乐. 改性膨润土吸附处理含砷废水实验研究[J]. 科学技术与工程, 2010, 10(16): 4093-4095, 4104. DOI:10.3969/j.issn.1671-1815.2010.16.070 (  0) 0) |
| [11] |
符浩, 魏钟波, 王翠兰, 等. 偶联剂改性凹凸棒土处理含汞(Ⅱ)废水的研究[J]. 环境工程学报, 2011, 5(5): 1106-1110. (  0) 0) |
| [12] |
XU Y H, NAKAJIMA T, OHKI A. Adsorption and Removal of Arsenic(Ⅴ) From Drinking Water by Aluminum-Loaded Shirasu-Zeolite[J]. Journal of Hazardous Materials, 2002, 92(3): 275-287. DOI:10.1016/S0304-3894(02)00020-1 (  0) 0) |
| [13] |
ÖZDEMIR O, ÇLNAR M, SABAH E, et al. Adsorption of Anionic Surfactants Onto Sepiolite[J]. Journal of Hazardous Materials, 2007, 147(1/2): 625-632. (  0) 0) |
| [14] |
孙约兵, 徐应明, 史新, 等. 海泡石对镉污染红壤的钝化修复效应研究[J]. 环境科学学报, 2012, 32(6): 1465-1472. (  0) 0) |
| [15] |
YIN H B, YE Y, ZHANG Y L, et al. Phosphate Removal From Wastewaters by a Naturally Occurring, Calcium-Rich Sepiolite[J]. Journal of Hazardous Materials, 2011, 198: 362-369. DOI:10.1016/j.jhazmat.2011.10.072 (  0) 0) |
| [16] |
WANG J, WANG W, LI R Q, et al. The Diploid Genome Sequence of an Asian Individual[J]. Nature, 2008, 456(7218): 60-65. DOI:10.1038/nature07484 (  0) 0) |
| [17] |
孔明, 尹洪斌, 吴雨琛, 等. 热处理对天然富钙粘土矿物除磷能力的影响[J]. 环境科学学报, 2013, 33(12): 3211-3218. (  0) 0) |
| [18] |
ZHANG G S, REN Z M, ZHANG X W, et al. Nanostructured Iron(Ⅲ)-Copper(Ⅱ) Binary Oxide:A Novel Adsorbent for Enhanced Arsenic Removal From Aqueous Solutions[J]. Water Research, 2013, 47(12): 4022-4031. DOI:10.1016/j.watres.2012.11.059 (  0) 0) |




