矿山开采和冶炼过程中会产生粉尘、废石和尾矿砂, 其中的重金属随地表径流、风力传送和雨水淋滤等自然作用污染周边土壤, 产生的环境问题已引起广泛关注。2014年环境保护部和国土资源部发布的《全国土壤污染状况调查公报》指出, 工矿业活动是造成土壤污染或超标的主要原因之一, 矿区土壤超标点位占33.4%, 主要污染物为Cd、Pb和As等。因此, 矿区重金属污染土壤的治理对于实现污染土壤的修复利用和保障农产品安全刻不容缓。
化学钝化修复是国内外常用的土壤重金属治理方法之一, 具有处理时间短、经济廉价和适用范围广等优点[1]。近年来, 生物炭作为一种高效、廉价的改良剂,在治理水体和土壤重金属污染中表现出潜在利用价值, 引起研究者们的高度关注。已有研究指出, 生物炭对Pb2+、Cd2+、Cu2+和Zn2+等重金属均具有固持作用[2-4], 这些研究多在溶液体系或短期外源添加的污染土壤中进行。而长时间重金属污染的矿区土壤中污染元素较多, 重金属之间的相互作用使得生物炭对其的吸附固持存在差异[5];另一方面, 外源添加污染土壤往往有效态重金属含量较高[6-7], 容易被生物炭吸附, 造成净吸附量偏高[8]。因此, 有必要对复合污染土壤进行研究, 以更好地评价生物炭的修复效果。
土壤中的重金属不能被微生物降解, 因此生物炭对重金属的影响主要是改变重金属的赋存形态, 进而影响其在土壤中的迁移性和生物可利用性。侯艳伟等[9]发现, 施用50 g·kg-1鸡粪和木屑生物炭后,土壤中残渣态Cu和Zn所占比例有所降低, 而残渣态Cd和Pb所占比例略有增加。JIN等[10]指出, 鸡粪和绿肥制备的生物炭添加量w为15%时, 射击场污染土壤中可交换态和碳酸盐结合态Cu、Cd和Pb含量降低, 而有机结合态和残渣态含量增加。HOUBEN等[11]研究发现, 秸秆生物炭的施用促进Cd和Zn由可交换态向碳酸盐结合态转换, 而其他组分几乎不发生改变。甘文君等[12]对电镀厂污染土壤的研究发现, 秸秆生物炭添加量为50 g·kg-1时土壤残渣态Cu、Zn、Ni和Cr含量明显增加。可见, 由于污染土壤类型、生物炭施用量及制备材料的不同, 生物炭对土壤中重金属赋存形态的影响仍然存在不确定性。该研究以矿区周边复合污染土壤为供试对象, 研究不同生物炭施用量对重金属形态转化的影响, 同时通过土壤pH值和有机碳含量的分析, 结合生物炭的元素组成和结构表征探讨其转化机理, 以期为应用生物炭修复矿区污染土壤提供更为全面的科学参考。
1 材料与方法 1.1 试验材料污染土壤采自安徽省铜陵市新桥矿区林地内(30.924 8° N, 117.994 6° E), 土壤类型为棕红壤, 质地为中壤土。多点采集土样, 采样深度为0~20 cm, 去除杂质后混合均匀, 于室内风干、压碎、磨细过2 mm孔径尼龙筛备用。土壤基本理化性质:pH值为7.62,电导率为0.60 mS·cm-1(土水质量比为1:2.5), 全氮含量为2.57 g·kg-1, 有机碳含量为37.4 g·kg-1, CaCO3含量为118 g·kg-1, 黏粒、粉粒和砂粒含量w分别为9%、57.5%和33.5%。由于距离采矿点较近, 供试土壤重金属污染严重, 总Cd和总Cu含量分别为27.2和3 551 mg·kg-1, 是GB 15618—1995《土壤环境质量标准》中二级标准限值的45.3和35.5倍, 总Pb和总Zn含量分别为762.7和1 785.1 mg·kg-1, 是二级标准限值的2.2和6.0倍。生物炭购自河南三利新能源公司, 原料为小麦秸秆, 热裂解炭化温度为350~500 ℃, pH值为10.53,电导率为5.98 mS·cm-1(物水质量比为1:10), 总Cd、总Cu、总Pb和总Zn含量分别为0.06、20.2、5.68和51.0 mg·kg-1。
1.2 试验设计用于培养试验的生物炭过0.5 mm孔径筛后未经其他处理。每盆装土1.0 kg, 设置4种生物炭添加量, w分别为0(B0)、1%(B1)、2%(B2) 和5%(B5), 每个处理重复3次。将生物炭与土壤充分混匀后装于塑料盆钵中, 用塑料膜封口, 并扎多个小孔以保证盆内外空气自由流通, 于室温下培养。定期加入去离子水, 使含水量保持在土壤最大田间持水量的70 %。培养150 d后将各处理盆钵内的土样翻匀进行采样, 测定土壤pH值、有机碳含量和不同形态重金属含量。
1.3 测定方法采用BCR连续提取法测定培养结束后土壤中酸提取态、可还原态、可氧化态和残渣态重金属含量, 具体方法为:称取0.500 g土壤样品于50 mL离心管中, 经过以下3个步骤顺序提取:0.11 mol·L-1 HAc溶液提取酸提取态, 0.5 mol·L-1 NH2OH·HCl溶液提取可还原态, H2O2和1 mol·L-1 NH4OAc溶液提取可氧化态。将各提取液离心后, 过0.45 μm孔径滤膜, 用原子吸收分光光度计(日立Z5000) 测定Cu、Zn、Cd和Pb含量。残渣态含量采用重金属总量减去以上形态含量获得。
重金属总量采用HNO3-HF-HClO4消化后原子吸收分光光度计测定。土壤和生物炭pH值和电导率采用水浸提后, 酸度计(雷磁PHB-4) 和电导率仪(雷磁DDBJ-350) 测定。土壤全氮和有机碳含量分别采用凯氏定氮法和重铬酸钾外加热法测定, CaCO3和黏粒含量采用中和滴定法和比重计法测定。试验所用器皿均用φ=10%的HNO3浸泡过夜, 以去除表面吸附的重金属, 并用去离子水清洗干净。
生物炭中C、N和H元素的质量分数通过元素分析仪(德国Elementar Vario EL Ⅲ)测定, 其他元素采用能谱仪(美国EDAX Octane Super)测定。生物炭采用溴化钾压片法制样, 使用傅里叶红外光谱(德国Bruker VERTEX80) 分析表面含有的官能团。矿物相组分采用X射线粉末衍射仪(北京普析XD-3) 分析。
1.4 数据统计用SPSS 17.0软件进行数据统计分析。采用one-way ANOVA分析进行各处理间比较, 采用Duncan法进行差异显著性分析, 采用Pearson双侧显著检验进行相关性分析。采用Excel 2010和Origin 8.0软件作图。
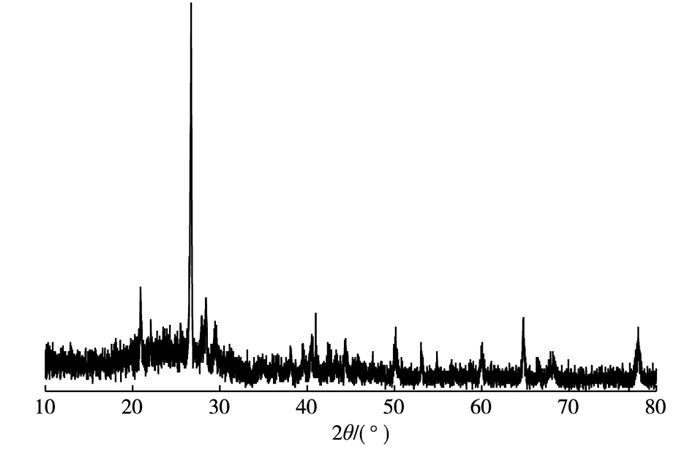
2 结果与分析 2.1 生物炭的组成特征元素分析表明, 供试秸秆生物炭以C为主, C、N和H含量w分别为43.58%、1.20%和1.64%, 同时还含有K、Ca、Mg、Si和Al等元素, w分别为5.00%、1.75%、0.78%、1.05%和0.52%。通过X射线衍射(XRD)进行矿物组分分析(图 1) 发现, 生物炭样品的衍射图谱在衍射角(2θ)位置为20.92°、26.70°、50.14°和60.06°处分别出现4.243 6、3.336 6、1.818 2和1.539 4 nm的尖锐峰, 表明其主要的无机矿物组分为SiO2; 同时出现3.140 6、2.224 3和1.815 2 nm的特征衍射峰, 对应的2θ位置分别为28.40°、40.53°和50.23°, 表明生物炭还含有部分KCl。
|
图 1 生物炭的X射线衍射图 Figure 1 XRD graphs of biochar |
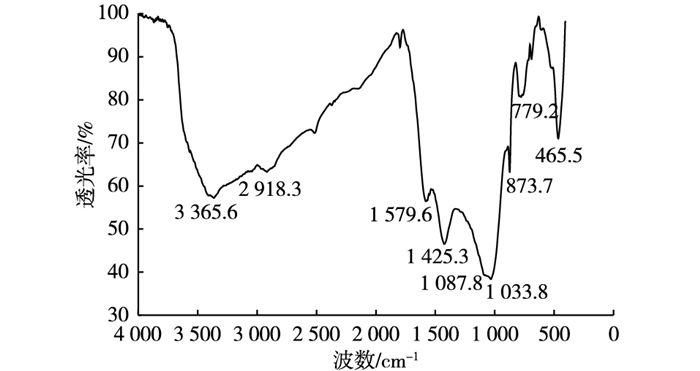
红外光谱分析(图 2) 发现, 3 365.6 cm-1处出现—OH的伸缩振动, 2 918.3 cm-1处出现—CH2不对称伸缩振动[13], 1 579.6和1 425.3 cm-1处为木质素中芳环C=C和C=O键的伸缩振动[14], 1 033.8 cm-1处为纤维素的C—O—C键[15], 1 087.8、779.2和465.5 cm-1处的吸收峰对应Si—O—Si的振动吸收[16], 873.7 cm-1处为芳环C—H的变形振动[17], 说明生物炭表面除存在SiO2外, 还含有丰富的羟基、羧基和羰基等含氧官能团, 这些官能团能够与重金属发生金属-配体的络合作用[10]。
|
图 2 生物炭的红外谱图 Figure 2 FTIR graphs of biochar |
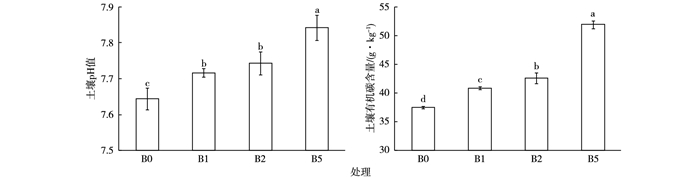
由图 3可见, 培养150 d后各处理土壤pH值在7.64~7.84之间, 施用生物炭可显著提高污染土壤pH值。相较于不施用生物炭的B0处理, w为1%、2%和5%施用量下土壤pH值分别提高0.96%、1.31%和2.62%, 其中w为5%施用量处理显著高于其余2个施用量处理(P < 0.05)。土壤有机碳含量也表现出随生物炭施用量增加而增加的趋势, 相较于B0处理, 施用生物炭处理的土壤有机碳含量提高9.1%~38.6%, 各处理之间差异均达显著水平(P < 0.05)。
|
图 3 生物炭对污染土壤pH值和有机碳含量的影响 Figure 3 Effects of biochar on pH value and organic carbon content in contaminated soils B0、B1、B2和B5的生物炭添加量w分别为0、1%、2%和5%。同一幅中直方柱上方英文小写字母不同表示各处理间某指标差异显著(P < 0.05)。 |
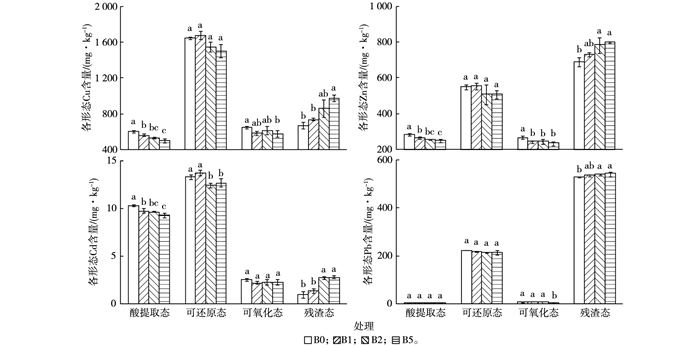
BCR连续提取法是欧盟标准物质局提出并建立的方法, 能够较好地反映土壤中重金属元素的形态分布情况。生物炭对复合污染土壤中不同重金属元素的形态分布有不同影响。由图 4可以看出, 污染土壤中Cu主要以可还原态形式存在, 占总量的比例在42.3%~47.2%之间, 其次是残渣态(18.7%~27.5%), 而可氧化态(16.2%~18.2%)和酸提取态Cu(14.0%~16.9%)所占比例较低。施用生物炭可显著降低土壤中酸提取态Cu含量(P < 0.05), 相较于B0处理, w为1%、2%和5%施用量下酸提取态Cu含量分别降低7.0%、11.7%和16.9%。生物炭对土壤可还原态Cu含量没有明显影响, w为5%施用量处理可显著降低可氧化态Cu含量(P < 0.05)。污染土壤中残渣态Cu含量随生物炭施用量的增加而增加, w为1%、2%和5%施用量下残渣态Cu含量较B0处理分别提高10.6%、29.3%和46.8%, 其中w为5%施用量处理与B0处理间差异达显著水平(P < 0.05)。
|
图 4 生物炭对污染土壤各形态Cu、Zn、Cd和Pb含量的影响 Figure 4 Effects of biochar on fractions and contents of different forms of Cu, Zn, Cd and Pb in contaminated soils B0、B1、B2和B5的生物炭添加量w分别为0、1%、2%和5%。同一幅图中同一组直方柱上方英文小写字母不同表示各处理间某指标差异显著(P < 0.05)。 |
污染土壤中Zn主要以可还原态和残渣态形式存在, 分别占总量的28.4%~30.9%和38.6%~44.7%, 高于酸可提取态(13.9%~15.8%)和可氧化态(13.0%~14.9%)。生物炭施用显著降低酸提取态Zn含量, 较B0处理的下降幅度为6.7%~11.8%。与Cu类似, 施用生物炭没有明显改变土壤中可还原态Zn含量, 但能显著降低可氧化态Zn含量(P < 0.05)。相较于B0处理, w为1%、2%和5%施用量下可氧化态Zn含量分别降低9.4%、8.1%和12.5%。随生物炭施用量的增加, 污染土壤中残渣态Zn含量明显提高, 增加幅度为5.9%~15.7%, 其中w为2%和5%施用量处理与B0处理间差异达显著水平(P < 0.05)。
Cd在污染土壤中主要以酸提取态和可还原态为主(图 4), 分别占总量的34.4%~38.0%和45.9%~50.8%, 可氧化态(8.2%~9.3%)和残渣态(3.2%~10.3%)所占比例较小。施用生物炭对Cd形态的影响主要是由酸提取态和可还原态向残渣态转变, 而对可氧化态Cd含量无明显影响。施用生物炭处理酸提取态Cd含量较B0降低5.3%~9.6%, w为2%和5%施用量处理可还原态和残渣态Cd含量与B0处理差异显著(P < 0.05), 可还原态Cd含量分别下降6.6%和4.6%, 而残渣态Cd含量分别增加185.5%和191.9%。可见, 施用生物炭对污染土壤中残渣态Cd的形成有明显促进作用。
与其余3种元素不同, 污染土壤中Pb主要以残渣态形式存在(图 4), 占总量的69.3%~71.2%, 其次是可还原态Pb(28.0%~29.4%), 而酸提取态和可氧化态Pb仅占0.3%~0.9%。生物炭施用对土壤酸提取态和可还原态Pb含量无显著影响, 可氧化态Pb含量仅在w为5%施用量下显著低于B0处理。残渣态Pb含量在施用生物炭处理中有一定程度提高, 增加幅度为1.5%~2.6%。相较而言, 施用生物炭对供试污染土壤Pb形态转化的影响较小。
2.4 土壤理化性质与不同形态重金属的相关性分析由表 1可知, 土壤pH值分别与酸提取态Cu、Zn、Cd含量呈极显著负相关(P < 0.01), 相关系数分别为-0.854、-0.791和-0.837, 而与酸提取态Pb无显著相关性。土壤有机碳含量与酸提取态Cu、Zn、Cd、Pb含量呈显著或极显著负相关(P < 0.05或P < 0.01), 相关系数为-0.871~-0.639。可还原态和可氧化态含量与土壤理化性质间的相关性在不同重金属上有不同表现, 其中可还原态、可氧化态Cu和Zn以及可氧化态Pb与土壤pH值间相关性达显著或极显著水平(P < 0.05或P < 0.01)。土壤有机碳含量与可还原态Cu、Zn、Cd、Pb均无显著相关性, 与可氧化态Zn和Pb含量呈显著或极显著负相关(P < 0.05或P < 0.01)。除Pb以外, 其余残渣态重金属含量与土壤pH值和有机碳含量均呈显著或极显著正相关关系, 相关系数分别在0.811~0.847和0.656~0.756之间。
|
|
表 1 土壤pH值和有机碳(TOC)含量与不同形态重金属含量之间的相关系数 Table 1 Correlation coefficients of fractions and contents of different forms of heavy metals with soil pH and organic carbon content |
从重金属总量和各形态分布来看, 供试污染土壤中Cd的环境风险最大, 其总量约为二级标准限值的45.3倍, 且4种元素中,酸提取态Cd占Cd总量的比例最高, 为34.4%~38.0%, 具有较大的生物可利用性和迁移性。Cu也表现出较大的环境风险, 总量超标35.5倍, 同时可还原态和可氧化态2种潜在有效态含量之和所占比例为58.5%~64.4%, 在环境条件改变时可能会转化为有效态。该研究所用土壤采集于铜陵新桥矿区山脚下, 该矿区以含铜黄铁矿(CuFeS2)为主, 伴有闪锌矿(ZnS)和方铅矿(PbS)等其他含硫矿物, 采矿过程中Cu、Zn和Cd氧化形成CuSO4、ZnSO4、CdSO4、ZnCO3和CdCO3等, 在酸雨和酸性矿山废水的作用下溶解迁移污染周边土壤。与Cu和Zn相比, Cd在酸性溶液中的溶出度更高, 因此酸提取态比例较高[18]。几种重金属元素中, Pb的酸提取态仅占0.3%左右, 这可能与该矿区中Pb主要以PbS形式存在有关,其在风化和迁移过程中易形成不易溶解的铅矾(PbSO4), 当遇到碳酸盐岩时, 即形成不溶或极难溶的白铅矿(PbCO3)[19], 因此以残渣态为主。
该研究结果表明, 生物炭能够显著降低复合污染土壤中酸提取态Cu、Cd和Zn含量, 残渣态重金属含量在w为2%和5%施用量下显著增加。试验所用秸秆生物炭包含多种无机矿物元素, 如Si、Ca和Mg等, 这些矿物组分对重金属的吸附作用是生物炭固定重金属的主要方式之一。陈再明等[20]指出, 水稻秸秆生物炭吸附重金属的主要矿物组分可能是裂解过程中产生的SiO2。同时, 生物炭可以提高土壤pH值, 使得土壤中重金属离子形成氢氧化物、碳酸盐或磷酸盐而沉淀[21]。此外, pH值升高还使得有效硅含量增加, 与重金属离子形成结构稳定的硅酸盐沉淀, 从而使残渣态比例增加[22]。因此, 生物炭施用使重金属元素向更加稳定的状态转化, 降低其环境风险, 这与以往研究结论[5-7]一致, 但在重金属形态转化程度上有不同结论。如杨惟薇等[7]通过45 d的培养试验发现, 生物炭施入显著降低土壤中酸提取态和可还原态Cd含量, 提高可氧化态和残渣态Cd含量,而可还原态和可氧化态重金属均有不同程度减少, 这可能与培养时间和土壤理化性质有关。可氧化态和可还原态为潜在有效态, 与酸提取态和残渣态重金属之间处于动态转化平衡状态, 在一定物理化学条件下会释放出来而具有生物有效性[23]。高瑞丽等[24]指出, 添加水稻秸秆生物炭后, Cd由酸提取态和可还原态向可氧化态转化, 残渣态Cd变化不显著, 其推测是由于培养时间(30 d)较短, 可氧化态Cd转化为残渣态的过程较弱。林爱军等[25]也认为, 骨炭对重金属的吸附固定是一个相对缓慢的过程。笔者研究设置的培养时间为150 d, 相较以上报道的修复时间更长, 重金属由有效态向难利用态转化的程度较高。另一方面, 笔者所用土壤偏碱性, 本底CaCO3含量较高, 施用生物炭后pH值进一步提高, 有利于重金属元素与CO32-通过化学反应形成难溶的CdCO3和Pb3(CO3)2(OH)2沉淀而转化为残渣态[3]。XU等[26]研究指出, 牛粪生物炭对重金属的吸附中CO32-和PO43-的沉淀作用可以占到75%~80%。此外, 4种重金属元素中, 生物炭对酸提取态、可还原态和可氧化态Pb所占比例大多无明显影响, 仅w为5%施用量下可氧化态Pb比例显著下降。这可能是由于供试污染土壤中Pb主要以残渣态存在(约70%), 而酸提取态和可氧化态Pb所占比例较低, 不到1%, 因此生物炭施用对这2种形态重金属的作用效果不明显。
该研究中, 生物炭施用显著提高土壤pH值和有机碳含量, 相关性分析表明, 两者与酸提取态Cd、Cu、Zn含量间呈显著负相关, 而与残渣态Cd、Cu、Zn含量呈正相关。土壤pH值升高可能从以下几个方面影响重金属有效性:(1) 使土壤胶体Zeta电位向负值方向位移, 促进土壤表面胶体所带负电荷量增加, 进而增加重金属离子的静电吸附量[2, 7];(2) 导致金属阳离子羟基态的形成, 相较于自由态金属离子, 其与土壤吸附点位的亲和力更强[2];(3) 增加土壤溶液中OH-浓度, 阳离子重金属可与OH-结合生成难溶的沉淀[27]。生物炭增加的有机碳可以通过羟基和羧基等含氧官能团增加土壤表面的吸附位点, 从而使交换态重金属通过表面络合被吸附[28], 因此有机碳含量与酸提取态重金属含量表现出显著相关性。可还原态(铁锰氧化物态)重金属含量受土壤pH值和氧化还原条件影响较大, 可氧化态重金属是由土壤动植物残骸、腐殖质和矿物颗粒与重金属螯合而成[23]。该研究中这2种形态重金属含量与土壤pH值和有机碳含量间的相关性在不同元素上有不同表现, 这可能与土壤性质、试验条件以及重金属离子间的相互作用等有关。如有研究发现, 生物炭施用后土壤有机碳含量与Cd各化学形态间没有表现出明显相关性[7]。总体而言, 酸提取态和残渣态重金属含量与土壤pH值和有机碳含量间的相关性高于可还原态和可氧化态。
4 结论(1) 供试秸秆生物炭以C为主, 同时含有N、K、Si、Ca和Mg等元素。XRD和红外分析结果表明, 其主要无机矿物组分为SiO2, 同时表面含有丰富的羧基、羟基和羰基等含氧官能团。
(2) 污染土壤pH值和有机碳含量随生物炭施用量的增加而增加, 两者与酸提取态重金属含量间呈显著或极显著负相关, 而与残渣态重金属含量间呈显著或极显著正相关。
(3) 生物炭能够显著降低复合污染土壤中酸提取态Cu、Cd和Zn含量, 而对酸提取态Pb含量影响较小; 残渣态Cu、Cd、Zn、Pb比例在w为2%和5%施用量下显著增加。供试污染土壤上施用生物炭能够促进重金属元素由酸提取态、可还原态和可氧化态向残渣态转化, 有利于降低重金属的迁移性和生物可利用性。
| [1] |
SUMAN RAJ D S, APARNA C, REKHA P, et al. Stabilization and Solidification Technologies for the Remediation of Contaminated Soils and Sediments:An Overview[J]. Land Contamination and Reclamation, 2005, 13(1): 23-48. DOI:10.2462/09670513.645 (  0) 0) |
| [2] |
蒋田雨, 姜军, 徐仁扣, 等. 不同温度下烧制的秸秆炭对可变电荷土壤吸附Pb(Ⅱ)的影响[J]. 环境科学, 2013, 34(4): 1598-1604. JIANG Tian-yu, JIANG Jun, XU Ren-kou, et al. Effects of Different Temperatures Biochar on Adsorption of Pb(Ⅱ) on Variable Charge Soils[J]. Environmental Science, 2013, 34(4): 1598-1604. (  0) 0) |
| [3] |
XU R K, ZHAO A Z. Effect of Biochars on Adsorption of Cu(Ⅱ), Pb(Ⅱ) and Cd(Ⅱ) by Three Variable Charge Soils From Southern China[J]. Environmental Science and Pollution Research, 2013, 20(12): 8491-8501. DOI:10.1007/s11356-013-1769-8 (  0) 0) |
| [4] |
王震宇, 刘国成, MONICAX, 等. 不同热解温度生物炭对Cd(Ⅱ)的吸附特性[J]. 环境科学, 2014, 35(12): 4735-4744. WANG Zhen-yu, LIU Guo-cheng, MONICA X, et al. Adsorption of Cd(Ⅱ) Varies With Biochars Derived at Different Pyrolysis Temperatures[J]. Environmental Science, 2014, 35(12): 4735-4744. (  0) 0) |
| [5] |
梁媛, 李飞跃, 杨帆, 等. 含磷材料及生物炭对复合重金属污染土壤修复效果与修复机理[J]. 农业环境科学学报, 2013, 32(12): 2377-2383. LIANG Yuan, LI Fei-yue, YANG Fan, et al. Immobilization and Its Mechanisms of Heavy Metal Contaminated Soils by Phosphate-Containing Amendment and Biochar[J]. Journal of Agro-Environment Science, 2013, 32(12): 2377-2383. DOI:10.11654/jaes.2013.12.010 (  0) 0) |
| [6] |
李明遥, 杜立宇, 张妍, 等. 不同裂解温度水稻秸秆生物炭对土壤Cd形态的影响[J]. 水土保持学报, 2013, 27(6): 261-264. LI Ming-yao, DU Li-yu, ZHANG Yan, et al. Influence of Pyrolysis Temperatures of Biochar Obtained From the Rice Straw on Cadmium Forms[J]. Journal of Soil and Water Conservation, 2013, 27(6): 261-264. (  0) 0) |
| [7] |
杨惟薇, 张超兰, 曹美珠, 等. 4种生物炭对镉污染潮土钝化修复效果研究[J]. 水土保持学报, 2015, 29(1): 239-243. YANG Wei-wei, ZHANG Chao-lan, CAO Mei-zhu, et al. Immobilization and Remediation of Cadmium Contaminated Soil With Four Kinds of Biochars[J]. Journal of Soil and Water Conservation, 2015, 29(1): 239-243. (  0) 0) |
| [8] |
张晶, 苏德纯. 不同镉污染农田土壤上秸秆和炭化秸秆分解动态及其对土壤镉的吸附特征[J]. 环境工程学报, 2013, 7(10): 4097-4102. ZHANG Jing, SU De-chun. Decomposition Dynamic and Cd Adsorption Characteristic of Crop Straw and Biochar in Different Cd-Contaminated Farmland Soils[J]. Chinese Journal of Environmental Engineering, 2013, 7(10): 4097-4102. (  0) 0) |
| [9] |
侯艳伟, 曾月芬, 安增莉. 生物炭施用对污染红壤中重金属化学形态的影响[J]. 内蒙古大学学报(自然科学版), 2011, 42(4): 460-466. HOU Yan-wei, ZENG Yue-fen, AN Zeng-li. Effects of the Application of Biochar on the Chemical Fraction of Heavy Metals in Polluted Red Soil[J]. Journal of Inner Mongolia University (Natural Science Edition), 2011, 42(4): 460-466. (  0) 0) |
| [10] |
JIN H P, CHOPPALA G K, BOLAN N S, et al. Biochar Reduces the Bioavailability and Phytotoxicity of Heavy Metals[J]. Plant and Soil, 2011, 348(1): 439-451. (  0) 0) |
| [11] |
HOUBEN D, EVRARD L, SONNET P. Mobility, Bioavailability and pH-Dependent Leaching of Cadmium, Zinc and Lead in a Contaminated Soil Amended With Biochar[J]. Chemosphere, 2013, 92(11): 1450-1457. DOI:10.1016/j.chemosphere.2013.03.055 (  0) 0) |
| [12] |
甘文君, 何跃, 张孝飞, 等. 秸秆生物炭修复电镀厂污染土壤的效果和作用机理初探[J]. 生态与农村环境学报, 2012, 28(3): 305-309. GAN Wen-jun, HE Yue, ZHANG Xiao-fei, et al. Effects and Mechanisms of Straw Biochar on Remediation Contaminated Soil in Electroplating Factory[J]. Journal of Ecology and Rural Environment, 2012, 28(3): 305-309. (  0) 0) |
| [13] |
CHEN B, ZHOU D, ZHU L. Transitional Adsorption and Partition of Nonpolar and Polar Aromatic Contaminants by Biochars of Pine Needles With Different Pyrolytic Temperatures[J]. Environmental Science and Technology, 2008, 42(14): 5137-5143. DOI:10.1021/es8002684 (  0) 0) |
| [14] |
CAO X, HARRIS W. Properties of Dairy-Manure-Derived Biochar Pertinent to Its Potential Use in Remediation[J]. Bioresource Technology, 2010, 101(14): 5222-5228. DOI:10.1016/j.biortech.2010.02.052 (  0) 0) |
| [15] |
LIU Q, WANG S, ZHENG Y, et al. Mechanism Study of Wood Lignin Pyrolysis by Using TG-FTIR Analysis[J]. Journal of Analytical and Applied Pyrolysis, 2008, 82(1): 170-177. DOI:10.1016/j.jaap.2008.03.007 (  0) 0) |
| [16] |
YANG H, XU R, XUE X, et al. Hybrid Surfactant-Templated Mesoporous Silica Formed in Ethanol and Its Application for Heavy Metal Removal[J]. Journal of Hazardous Materials, 2008, 152(2): 690-698. DOI:10.1016/j.jhazmat.2007.07.060 (  0) 0) |
| [17] |
MORENO-CASTILLA C, LÓPEZ-RAMÓN M V, CARRASCO-MARI'N F. Changes in Surface Chemistry of Activated Carbons by Wet Oxidation[J]. Carbon, 2000, 38(14): 1995-2001. DOI:10.1016/S0008-6223(00)00048-8 (  0) 0) |
| [18] |
张鑫. 安徽铜陵矿区重金属元素释放迁移地球化学特征及其环境效应研究[D]. 合肥: 合肥工业大学, 2005. ZHANG Xin.Geochemical Characteristics and Environmental Effects of Heavy-Metal Elements Releasing and Migrating in Tongling Mine Area, Anhui Province[D]. Hefei:Hefei University of Technology, 2005. (  0) 0) |
| [19] |
周涛发, 殷汉琴, 张鑫, 等. 铜陵矿区土壤中铅的存在形态及生物有效性[J]. 合肥工业大学学报(自然科学版), 2005, 28(9): 1146-1150. ZHOU Tao-fa, YIN Han-qin, ZHANG Xin, et al. Speciation and Bioavailability of Lead in Tongling Mining Soil[J]. Journal of Hefei University of Technology (Natural Science Edition), 2005, 28(9): 1146-1150. (  0) 0) |
| [20] |
陈再明, 方远, 徐义亮, 等. 水稻秸秆生物碳对重金属Pb2+的吸附作用及影响因素[J]. 环境科学学报, 2012, 32(4): 769-776. CHEN Zai-ming, FANG Yuan, XU Yi-liang, et al. Adsorption of Pb2+ by Rice Straw Derived-Biochar and Its Influential Factors[J]. Acta Scientiae Circumstantiae, 2012, 32(4): 769-776. (  0) 0) |
| [21] |
BEESLEY L, MORENO-JIMÉNEZ E, GOMEZ-EYLES J L, et al. A Review of Biochars' Potential Role in the Remediation, Revegetation and Restoration of Contaminated Soils[J]. Environmental Pollution, 2011, 159(12): 3269-3282. DOI:10.1016/j.envpol.2011.07.023 (  0) 0) |
| [22] |
NEUMANN D, NIEDEN U Z. Silicon and Heavy Metal Tolerance of Higher Plants[J]. Phytochemistry, 2001, 56(7): 685-692. DOI:10.1016/S0031-9422(00)00472-6 (  0) 0) |
| [23] |
韩春梅, 王林山, 巩宗强, 等. 土壤中重金属形态分析及其环境学意义[J]. 生态学杂志, 2005, 24(12): 1499-1502. HAN Chun-mei, WANG Lin-shan, GONG Zong-qiang, et al. Chemical Forms of Soil Heavy Metals and Their Environmental Significance[J]. Chinese Journal of Ecology, 2005, 24(12): 1499-1502. DOI:10.3321/j.issn:1000-4890.2005.12.025 (  0) 0) |
| [24] |
高瑞丽, 朱俊, 汤帆, 等. 水稻秸秆生物炭对镉、铅复合污染土壤中重金属形态转化的短期影响[J]. 环境科学学报, 2016, 36(1): 251-256. GAO Rui-li, ZHU Jun, TANG Fan, et al. Fractions Transformation of Cd, Pb in Contaminated Soil After Short-Term Application of Rice Straw Biochar[J]. Acta Scientiae Circumstantiae, 2016, 36(1): 251-256. (  0) 0) |
| [25] |
林爱军, 张旭红, 苏玉红, 等. 骨炭修复重金属污染土壤和降低基因毒性的研究[J]. 环境科学, 2007, 28(2): 232-237. LIN Ai-jun, ZHANG Xu-hong, SU Yu-hong, et al. Chemical Fixation of Metals in Soil Using Bone Char and Assessment of the Soil Genotoxicity[J]. Environmental Science, 2007, 28(2): 232-237. (  0) 0) |
| [26] |
XU X, CAO X, ZHAO L, et al. Removal of Cu, Zn, and Cd From Aqueous Solutions by the Dairy Manure-Derived Biochar[J]. Environmental Science and Pollution Research, 2013, 20(1): 358-368. DOI:10.1007/s11356-012-0873-5 (  0) 0) |
| [27] |
廖敏, 黄昌勇, 谢正苗. pH对镉在土水系统中的迁移和形态的影响[J]. 环境科学学报, 1999, 19(1): 81-86. LIAO Min, HUANG Chang-yong, XIE Zheng-miao. Effect of pH on Transport and Transformation of Cadmium in Soil-Water System[J]. Acta Scientiae Circumstantiae, 1999, 19(1): 81-86. (  0) 0) |
| [28] |
佟雪娇, 李九玉, 姜军, 等. 添加农作物秸秆炭对红壤吸附Cu(Ⅱ)的影响[J]. 生态与农村环境学报, 2011, 27(5): 37-41. TONG Xue-jiao, LI Jiu-yu, JIANG Jun, et al. Effect of Biochars Derived From Crop Straws on Cu(Ⅱ) Adsorption by Red Soils[J]. Journal of Ecology and Rural Environment, 2011, 27(5): 37-41. (  0) 0) |



