2. 环境保护部南京环境科学研究所, 江苏 南京 210042
2. Nanjing Institute of Environmental Sciences, Ministry of Environmental Protection, Nanjing 210042, China
双酚A(bisphenol A, BPA)用于制造环氧树脂(epoxyresin)、聚碳酸酯(polycarbonate)以及精细化工产品(如农药、橡胶防老剂、婴儿奶瓶和瓶盖等)[1], 是应用最广泛的工业化学品之一。研究表明, BPA具有干扰内分泌等毒性作用, 对雄性生殖系统有一定的损害[2], 可能会引起性早熟[3], 对胚胎也会有一定的影响[4]。在低浓度长时间暴露的情况下, BPA对亲代和子代生殖系统、脑和神经系统及免疫系统等有不良影响, 可能会引发癌症、肥胖、糖尿病、生殖障碍和神经系统紊乱等多种疾病。考虑到BPA的潜在低剂量效应, 尤其是对婴幼儿等敏感人群[5-6], 部分国家已经开始限制含BPA塑料制品的使用, 近年来越来越多的国家采取了禁用措施。为了应对这些限制, 一些双酚类似物如双酚B(bisphenol B, BPB)、双酚S(bisphenol S, BPS)和双酚F(bisphenol F, BPF)等被用来替代BPA用于环氧树脂、塑料、热敏纸和食品包装材料等的生产[7-9]。
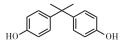
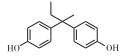
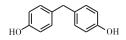
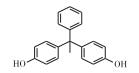
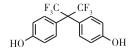
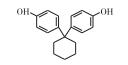
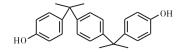
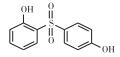
常见的双酚A类似物有BPB、BPF、BPAP、BPAF、BPZ、BPP和BPS等, 其CAS号及分子结构图如表 1所示。双酚A类似物与双酚A具有相似的分子结构, 都具有2个羟苯基, 但2个羟苯基之间碳桥上的取代基不同, 由于这类化合物具有性质较稳定、耐高温、延展性好、制作工艺简单和成本低等优点, 因此被广泛用于工业生产[10-12]。FIEGE等[13]研究发现BPS是酚醛树脂和电镀溶剂等的组分, 可增加物质的硬度和耐用度, 已被用于道路和桥梁建设中。LIAO等[14]研究发现热敏纸中存在BPS。随着双酚A类似物的大量使用, 污染物大量排入空气中, 许多研究表明双酚A分子可以从婴儿奶瓶或瓶体脱离, 进入水或食物中危害人体健康[15], 并可与食物结合进入生物体[16], 造成内分泌系统紊乱, 而且具有易富集和不易降解等特点, 因此对自然界生物体及人体带来越来越多的伤害[17]。
|
|
表 1 双酚A及其类似物的基本信息 Table 1 Basic information of bisphenol A and its analogues |
现阶段, 对双酚A类似物已经有一些生物体效应方面的研究。SONG等[18]以斑马鱼的胚胎和幼鱼为模式生物研究了3种卤代双酚A化合物(TBBPA、TCBPA和BPAF)的发育毒性, 半致死浓度值(LC50)的计算结果表明这几种物质的毒性由高到低为TCBPA、TBBPA和BPAF; KURUTO-NIWA等[19]将雄性和雌性斑马鱼暴露在BPS质量浓度为0.5~50 μg·L-1的水样中21 d后, 雌性和雄性斑马鱼血浆中的雌二醇含量显著升高, 而雄性斑马鱼血浆中的睾酮含量则显著降低。李圆圆等[20]研究了BPA、BPS和BPF对黑斑蛙胚胎及蝌蚪的急性毒性, 发现BPA的急性毒性与BPF相当, 但高于BPS。虽然已有双酚A类似物对水生生物急性毒性的研究报道, 但鲜见对几种检出率较高的双酚A类似物的系统研究, 为了更好地说明8种双酚A及其类似物对生物的急性毒性效应, 笔者采用模式生物斑马鱼及其胚胎来评价8种受试物对水生生物的潜在毒性效应, 以期为双酚A类似物的生态风险评价提供科学依据。
1 材料与方法 1.1 试验材料 1.1.1 受试生物试验所用斑马鱼(AB型)购于尧舜禹生物科技有限公司, 平均体长(3.2±0.4) cm, 平均体重0.15 g。斑马鱼胚胎购于尧舜禹生物科技有限公司, 胚胎期斑马鱼暴露试验以囊胚期开端(即受精后2 h, 2hpf)的胚胎作为起始。
1.1.2 试剂BPA、BPB、BPF、BPAP、BPAF、BPZ、BPP和BPS购自百灵威科技有限公司(上海), 以丙酮(色谱纯, 德国Merck公司)作溶剂配制成质量浓度为103~105mg·L-1的贮备液(置于4 ℃冰箱避光保存)。试验所有梯度稀释操作时均用丙酮作溶剂(丙酮体积分数为0.01%~0.5%), 去离子水由Mini-Q超纯水机制备(美国Miliipore公司)。
1.1.3 仪器设备硬度计(16900型, 美国哈希公司), 多功能水质参数测定仪(HQ40d, 美国哈希公司), 溶解氧测定仪(HQ30d, 美国哈希公司), 电子分析天平(AG135, 美国Mettler Toledo公司), 生态培养箱(CLIMACELL型, 德国MMM公司)。
1.2 试验方法斑马鱼成鱼及胚胎急性毒性试验方法参照文献[21-22]进行。
1.2.1 受试物浓度设置在正式试验之前先对8种物质进行较大范围浓度系列(0.1、1、10、100和1 000 mg·L-1)的预试验, 先在玻璃缸中装入经曝气处理的水3 L, 加入受试物贮备液, 不设平行组, 各试验容器放10尾斑马鱼, 试验期间不换水、不喂食, 观察记录鱼死亡数。
根据预试验得出的结果, 斑马鱼成鱼及胚胎正式试验浓度梯度设置见表 2。
|
|
表 2 正式试验中双酚A及类似物的浓度设置 Table 2 Concentrations of bisphenol A and its analogues set in the formal test |
试验期间(0~96 h)试验用水硬度(以CaCO3计)为180~190 mg·L-1, pH值为7.0~7.2, 溶解氧质量浓度为7.68~7.98 mg·L-1。
1.2.3 试验操作将斑马鱼成鱼置于循环水玻璃缸中驯养2周, 温度设置为(23±0.5) ℃, 光照周期为t(光照):t(黑暗)=16 h:8 h, 每天投喂2次丰年虾(Artemia salina), 7 d内死亡率小于5%, 可用于后续试验。
将斑马鱼成鱼随机放入含3 L药液的玻璃缸中, 每个缸中放入10条已驯养斑马鱼, 每个受试物浓度设3个平行, 所有玻璃缸放到恒温水槽中, 水槽温度设置为(23±0.5) ℃, 光照周期为t(光照):t(黑暗)=16 h:8 h。分别在6、24、48、54、72和96 h时记录斑马鱼死亡数, 观察斑马鱼的异常行为, 及时清除死鱼。
将斑马鱼受精卵放入50 mL小烧杯中, 每个烧杯20粒, 每个受试物浓度设3个平行, 将烧杯置于生态培养箱, 设定照度为50 lx, 光照周期为t(光照):t(黑暗)=16 h:8 h, 温度为(23±0.5) ℃。每天统计胚胎死亡数, 用显微镜观察畸形情况, 及时清除死亡胚胎。
1.3 统计学方法采用美国环境保护局修正的斯皮尔曼-卡伯分析软件(Trimmed Spearman-Karber Method)计算LC50及95%置信区间, 通过Origin 8.0软件拟合浓度-效应曲线。
2 试验结果 2.1 成年斑马鱼及胚胎的中毒现象斑马鱼中毒时一般表现为侧翻、身体扭曲、串游和上浮等, 死亡一段时间后沉入缸底。500 mg·L-1 BPS试验组中, 6 h内出现死亡现象; 5、6 mg·L-1的BPAF、BPZ和8、10 mg·L-1 BPB试验组中, 16 h内出现全部死亡现象; 4、5 mg·L-1BPAP, 12、14 mg·L-1 BPA和14 mg·L-1 BPF试验组中, 24 h内出现全部死亡现象。1 mg·L-1 BPP试验组中, 30 h内出现全部死亡现象。
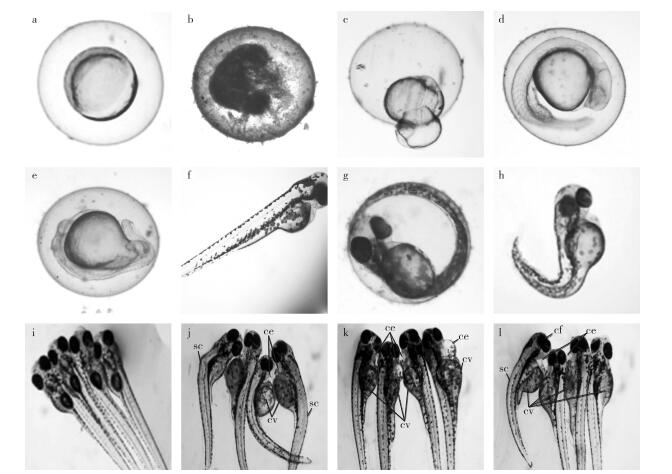
在高浓度暴露下早期阶段的受精卵颜色出现变化, 由透明变成白色半透明并死亡。胚胎中毒后出现畸形或身体由半透明变为不透明并死亡。仔鱼中毒后出现畸形或无呼吸无心脏跳动死亡(图 1)。
|
图 1 斑马鱼胚胎的双酚A及其类似物染毒症状 Figure 1 Toxication symptoms of zebrafish embryo exposed to bisphenol A and its analogues a—6 h时发育正常的卵; b—6 h时的卵凝结; c—6 h时发育异常的卵; d—20 h时发育正常的卵; e—20 h时发育阻滞的胚胎; f—78 h时发育正常的胚胎; g—78 h时发育阻滞的胚胎; h—78 h时脊柱弯曲的胚胎; i、j、k、l—96 h时发育畸形的胚胎。ce—心包水肿; cv—卵黄囊肿; sc—脊柱弯曲; cf—颅面畸形。 |
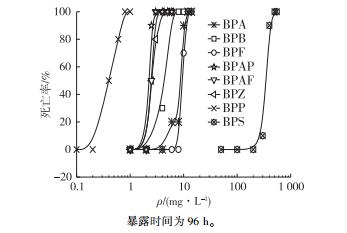
表 3是成鱼24、48、72和98 h的LC50及95%置信区间。图 2是试验96 h时8种受试物暴露下成年斑马鱼的死亡率曲线图, 对于同一种受试物, 随着暴露浓度的升高死亡率也逐渐升高。8种受试物中BPP的死亡率首先达到100%, 然后依次是BPAP、BPAF、BPB、BPA、BPF和BPS。
|
|
表 3 双酚A及其类似物对斑马鱼成鱼的半致死浓度(LC50) Table 3 Half lethal concentration (LC50)of bisphenol A and its analogues for adult zebrafish |
|
图 2 双酚A及其类似物对斑马鱼成鱼死亡率的影响 Figure 2 Mortality of adult zebrafish exposed to bisphenol A and its analogues for 96 h |
根据GB 30000.28—2013《化学品分类和标签规范第28部分:对水生环境的危害》对受试物的急性水环境毒性的分级标准(96 h的LC50:≤1 mg·L-1为Ⅰ级, >1~10 mg·L-1为Ⅱ级, >10~100 mg·L-1为Ⅲ级)[23], 结合图 2和表 3, 判定BPP为毒性Ⅰ级, BPA、BPB、BPF、BPZ、BPAP和BPAF为毒性Ⅱ级。
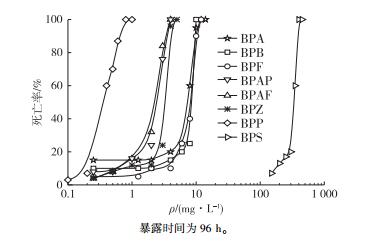
图 3是8种受试物暴露96 h时斑马鱼胚胎的死亡率曲线。随着受试物浓度升高, 死亡率也逐渐升高, 这与成鱼的试验结果一致。8种受试物比较而言, BPP的效应浓度最低, BPS的效应浓度最高, BPAF和BPAP对胚胎的浓度-效应曲线比较接近, 说明它们对胚胎的急性毒性强度较接近, 随后依次为BPZ、BPB、BPA和BPF。
|
图 3 双酚A及其类似物对斑马鱼胚胎死亡率的影响 Figure 3 Mortality of zebrafish embryo exposed to bisphenol A and its analogues for 96 h |
表 4是胚胎24、48、72和96 h的LC50及95%置信区间。结合图 3和表 4, 判定BPP为毒性Ⅰ级, BPA、BPB、BPF、BPZ、BPAP和BPAF为毒性Ⅱ级。
|
|
表 4 双酚A及类似物对斑马鱼胚胎的半致死浓度(LC50) Table 4 Half lethal concentration (LC50)of bisphenol A and its analogues for zebrafish embryo |
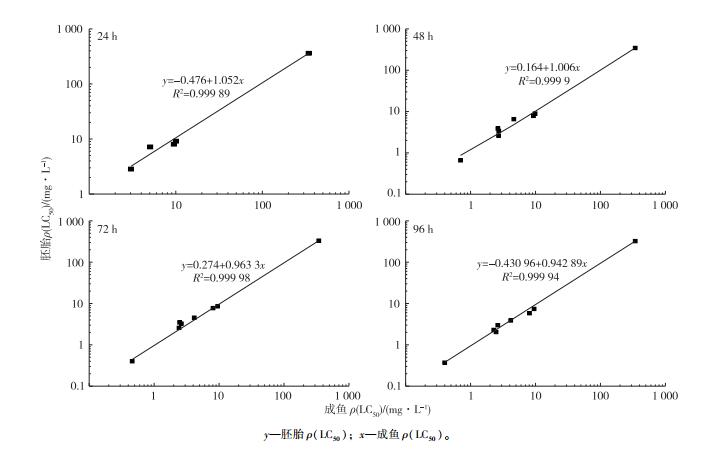
斑马鱼成鱼和胚胎96 h时的LC50对比如图 4所示。从图 4可知, 8种受试物对成鱼和胚胎的LC50相差不大。斑马鱼成鱼(x)和胚胎(y)的毒性相关性见图 5, 24 h时毒性回归方程为y=-0.476+1.052x, R2为0.999 89;48 h时毒性回归方程为y=0.164+1.004x, R2为0.999 9;72 h时毒性回归方程为y=0.274+0.963 3x, R2为0.999 98;96 h时毒性回归方程为y=-0.430 96+0.942 89 x, R2为0.999 94。由图 5可以看出, 当某种受试物对成年斑马鱼的LC50高时, 则该受试物对胚胎的LC50也较高, 说明双酚A及其类似物对斑马鱼成鱼与胚胎的毒性效应有高度的一致性。

|
图 4 斑马鱼成鱼和胚胎96 h时的半致死浓度(LC50) Figure 4 96 h LC50 of bisphenol A and its analogues for adult zebrafish and embryo |
|
图 5 斑马鱼成鱼与胚胎的毒性相关性 Figure 5 Correlation of toxicity of bisphenol A and its analogues to embryo with that to adult zebrafish |
双酚A是被研究较多的环境内分泌干扰物, 关于双酚A及其类似物的毒性比较研究较少, 该试验对BPA及其7种类似物BPB、BPF、BPAP、BPAF、BPZ、BPP、BPS进行了比较研究, 发现BPP对斑马鱼成鱼及胚胎的毒性最大, BPS毒性最小, 根据GB 30000.28—2013对受试物的急性水环境毒性的分级标准[23], 判定BPP为毒性Ⅰ级, BPA、BPB、BPF、BPZ、BPAP和BPAF为毒性Ⅱ级。
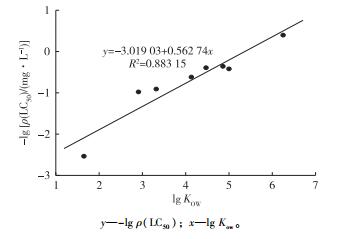
根据Verhaar分类方法, 具有麻醉致毒机制的化合物, 其毒性与化合物的辛醇-水分配系数KOW(lg KOW值由EPI Suit 4.1软件计算)具有较好相关性。图 6显示了8种受试物的KOW与96 h的LC50的线性关系, 可以看出两者拟合度较好, 说明这些受试物的毒性与本身的疏水性密切相关。它们具有相似的分子结构, 都具有2个羟苯基, 但2个羟苯基之间碳桥上的取代基不同, 取代基的疏水性大小决定了其毒性大小, 疏水性越大毒性越大。例如BPA的碳桥上连了2个甲基, 而BPP比BPA多2个甲基和1个苯环, 所以BPP的疏水性大, 毒性大于BPA。BPA比BPF多2个甲基, 所以BPA的疏水性大, 毒性大于BPF。BPS的碳桥被硫氧基取代, 所以疏水性变小, 毒性比BPA小。综上可知, 8种双酚A及其类似物是具有麻醉致毒机制的化合物。
|
图 6 双酚A及其类似物的辛醇-水分配系数(KOW)与毒性的相关性 Figure 6 Correlation of octanol-water partition with the toxic of bisphenol A and its analogues |
这些双酚类有毒物质在水体中被广泛检出, GONG等[24]测得珠江水ρ(BPA)为0.04~0.64 μg·L-1。WU等[25]测得黄浦江ρ(BPA)平均值为22.93 ng·L-1。YANG等[26]对浙江杭州湾嘉兴段BPAF生产区的河水研究发现, 除了ρ(BPAF)较高(254.59 ng·L-1)以外, 还检测出了不同浓度的BPS、BPF和BPA; SONG等[27]对BPAF制造厂周围不同环境介质的分析发现, 大部分环境介质中均检测到不同浓度的BPAF, 其中, 河水中质量浓度为<最低检测限(LOD)~1.53×104 ng·L-1, 虽然在水环境中的检出量小于效应值, 但由于双酚A及其类似物很难降解, 会在水生生物体内不断积累, 造成长期影响, 所以仍需持续关注。
鱼类对污染物的暴露特别敏感, 有较多的毒性研究试验都以成年斑马鱼或稀有鮈鲫作为模式生物, 以胚胎作为受试生物的研究较少, 通过毒性相关性分析得知成鱼和胚胎毒性效应呈线性相关关系, 因此传统的成鱼毒性试验可以被胚胎毒性试验所代替, 鱼类胚胎毒性测试可用于化学品的急性毒性研究。
4 结论(1) 通过对斑马鱼成鱼及胚胎96 h的急性毒性试验, 发现BPS的毒性比BPA、BPB、BPF、BPAP、BPAF和BPZ低2个数量级, 比BPP毒性低3个数量级。BPP对斑马鱼成鱼及胚胎的的毒性效应最大, 需要加强防范。
(2) 根据GB 30000.28—2013对受试物的急性水环境毒性的分级标准, 判定BPP为毒性Ⅰ级, BPA、BPB、BPF、BPZ、BPAP和BPAF为毒性Ⅱ级; 双酚A及其类似物是具有麻醉致毒机制的化合物, 其毒性大小与疏水性密切相关, 疏水性越大毒性越大。
(3) 双酚A及其类似物对斑马鱼成鱼与胚胎的毒性效应有一致性。
| [1] |
WILLHITE C C, BALL G L, MCLELLAN C J. Derivation of a Bisphenol Oral Reference Dose (RfD) and Drinking-Water Equivalent Concentration[J]. Journal of Toxicology & Environmental Health (Part B:Critical Reviews), 2008, 11(2): 69-146. (  0) 0) |
| [2] |
LI D K, ZHOU Z, MIAO M, et al. Urine Bisphenol-A (BPA) Level in Relation to Semen Quality[J]. Fertility and Sterility, 2011, 95(2): 625-630. DOI:10.1016/j.fertnstert.2010.09.026 (  0) 0) |
| [3] |
乔丽丽, 郑力行, 蔡德培. 性早熟女童血清中双酚A、辛基酚、4-壬基酚测定和分析[J]. 卫生研究, 2010, 95(1): 625-630. QIAO Li-li, ZHENG Li-xing, CAI De-pei. Study on the Levels of the Bisphenol A, Octylphenol, 4-Nonylphenol in Serum of Precocious Girls[J]. Journal of Hygiene Research, 2010, 95(2): 625-630. (  0) 0) |
| [4] |
CAN A, SEMIZ O, CINAR O. Bisphenol A Induces Cell Cycle Delay and Alters Centrosome and Spindle Microtubular Organization in Oocytes During Meiosis[J]. Molecular Human Reproduction, 2005, 11(6): 389-396. DOI:10.1093/molehr/gah179 (  0) 0) |
| [5] |
NAGEL S C, VOM SAAL F S, THAYER K A, et al. Relative Binding Affinity-Serum Modified Access (RBA-SMA) Assay Predicts the Relative in Vivo Bioactivity of the Xenoestrogens Bisphenol A and Octylphenol[J]. Environmental Health Perspectives, 1997, 105(1): 70-76. DOI:10.1289/ehp.9710570 (  0) 0) |
| [6] |
TIAN Y H, BAEK J H, LEE S Y, et al. Prenatal and Postnatal Exposure to Bisphenol a Induces Anxiolytic Behaviors and Cognitive Deficits in Mice[J]. Synapse, 2010, 64(6): 432-439. DOI:10.1002/syn.v64:6 (  0) 0) |
| [7] |
KURUTO-NIWA R, NOZAWA R, MIYAKOSHI T, et al. Estrogenic Activity of Alkylphenols, Bisphenol S, and Their Chlorinated Derivatives Using a GFP Expression System[J]. Environmental Toxicology and Pharmacology, 2005, 19(1): 121-130. DOI:10.1016/j.etap.2004.05.009 (  0) 0) |
| [8] |
SUEIRO R A, SUÂREZ S, ARAUJO M, et al. Mutagenic and Genotoxic Evaluation of Bisphenol F Diglycidyl Ether (BFDGE) in Prokaryotic and Eukaryotic Systems[J]. Mutation Research/ Genetic Toxicology and Environmental Mutagenesis, 2003, 536(1/2): 39-48. (  0) 0) |
| [9] |
SATOH K, OHYAMA K, AOKI N, et al. Study on Anti-Androgenic Effects of Bisphenol a Diglycidyl Ether (BADGE), Bisphenol F Diglycidyl Ether (BFDGE) and Their Derivatives Using Cells Stably Transfected With Human Androgen Receptor, AR-Ecoscreen[J]. Food and Chemical Toxicology, 2004, 42(6): 983-993. DOI:10.1016/j.fct.2004.02.011 (  0) 0) |
| [10] |
KITAMURA S, SUZUKI S, SANOH S, et al. Comparative Study of the Endocrine-Disrupting Activity of Bisphenol A and 19 Related Compounds[J]. Toxicological Sciences, 2005, 84(2): 249-259. DOI:10.1093/toxsci/kfi074 (  0) 0) |
| [11] |
GOODMAN J E, WITORSCH R J, MCCONNELL E E, et al. Weight-of-Evidence Evaluation of Reproductive and Developmental Effects of Low Dose of Bisphenol A[J]. Critical Reviews in Toxicology, 2009, 39(1): 1-75. DOI:10.1080/10408440802157839 (  0) 0) |
| [12] |
VAN DENBERG L N, COLBORN T, HAYES T B, et al. Hormones and Endocrine-Disrupting Chemicals:Low-Dose Effects and Nonmonotonic Dose Responses[J]. Endocrine Reviews, 2012, 33(3): 378-455. DOI:10.1210/er.2011-1050 (  0) 0) |
| [13] |
FIEGE H, VOGES H W, HAMAMOTO T, et al. Phenol Derivatives[M]. .
(  0) 0) |
| [14] |
LIAO C, LIU F, KANNAN K. Bisphenol S, A New Bisphenol Analogue, in Paper Products and Currency Bills and Its Association With Bisphenol a Residues[J]. Environmental Science & Technology, 2012, 46(12): 6515-6522. (  0) 0) |
| [15] |
COOPER J E, KENDIG E L, BELCHER S M. Assessment of Bisphenol A Released From Reusable Plastic, Aluminium and Stainless Steel Water Bottles[J]. Chemosphere, 2011, 85(6): 943-947. DOI:10.1016/j.chemosphere.2011.06.060 (  0) 0) |
| [16] |
GRUMETTO L, MONTESANO D, SECCIA S, et al. Determination of Bisphenol A and Bisphenol B Residues in Canned Peeled Tomatoes by Reversed-Phase Liquid Chromatography[J]. Journal of Agricultural and Food Chemistry, 2008, 56(22): 10633-10637. DOI:10.1021/jf802297z (  0) 0) |
| [17] |
CASALS-CASAS C, DESVERGNE B. Endocrine Disruptors:From Endocrine to Metabolic Disruption[J]. Annual Review of Physiology, 2011, 73: 135-162. DOI:10.1146/annurev-physiol-012110-142200 (  0) 0) |
| [18] |
SONG M Y, LIANG D, LIANG Y, et al. Assessing Developmental Toxicity and Estrogenic Activity of Halogenated Bisphenol A on Zebrafish (Danio rerio)[J]. Chemosphere, 2014, 112(1): 275-281. (  0) 0) |
| [19] |
KURUTO-NIWA R, NOZAWA R, MIYAKOSHI T, et al. Estrogenic Activity of Alkylphenols, Bisphenol S, and Their Chlorinated Derivatives Using a GFP Expression System[J]. Environmental Toxicology Pharmacology, 2005, 19(1): 121-130. DOI:10.1016/j.etap.2004.05.009 (  0) 0) |
| [20] |
李圆圆, 付旭锋, 赵亚娴, 等. 双酚A与其替代品对黑斑蛙急性毒性的比较[J]. 生态毒理学报, 2015, 10(2): 251-257. LI Yuan-yuan, FU Xu-feng, ZHAO Ya-xian, et al. Comparison on Acute Toxicity of Bisphenol A With Its Substitutes to Pelophylax nigromaculatus[J]. Asian Journal of Ecotoxicology, 2015, 10(2): 251-257. (  0) 0) |
| [21] |
OECD.Guidelines for the Testing of Chemicals, No. 203 Fish Acute Toxicity Test[Z].Paris, France:OECD, 1992.
(  0) 0) |
| [22] |
GB/T 27861-2011, 化学品鱼类急性毒性实验[S]. GB/T 27861-2011, Chemicals, Fish Acute Toxicity Test[S]. (  0) 0) |
| [23] |
GB 30000. 28-2013, 化学品分类和标签规范第28部分: 对水生环境的危害[S]. GB 30000. 28-2013, Rules for Classification and Labelling of Chemicals, Part 28: Hazardous to Aquatic Environment[S]. (  0) 0) |
| [24] |
GONG J, RAN Y, CHEN D Y, et al. Occurrence and Environmental Risk of Endocrine-Disrupting Chemicals in Surface Waters of the Pearl River, South China[J]. Environmental Monitoring and Assessment, 2009, 156(1/2/3/4): 199-210. (  0) 0) |
| [25] |
WU M, WANG L, XU G, et al. Seasonal and Spatial Distribution of 4-Tert-Octylphenol, 4-Nonylphenol and Bisphenol A in the Huangpu River and Its Tributaries, Shanghai, China[J]. Environmental Monitoring and Assessment, 2013, 185(4): 3149-3161. DOI:10.1007/s10661-012-2779-6 (  0) 0) |
| [26] |
YANG Y J, LU L B, ZHANG J, et al. Simultaneous Determination of Seven Bisphenols in Environmental Water and Solid Samples by Liquid Chromatography-Electrospray Tandem Mass Spectrometry[J]. Journal of Chromatography A, 2014, 132(8): 26-34. (  0) 0) |
| [27] |
SONG S, RUAN T, WANG T, et al. Distribution and Preliminary Exposure Assessment of Bisphenol AF (BPAF) in Various Environmental Matrices Around a Manufacturing Plant in China[J]. Environmental Science & Technology, 2012, 46(24): 13136-13143. (  0) 0) |