邻苯二甲酸酯(phthalic acid esters, PAEs)污染已经成为全球性环境问题。在全球各地的水、土壤、大气、生物体等环境介质中均检测到PAEs[1-5]。大量研究表明, PAEs具有多种潜在毒性。作为环境激素, 一些PAEs可以影响人和动物的内分泌系统, 导致生殖发育及行为异常[5-9]。另外, 一些PAEs具有致畸和致突变作用[5]。由于PAEs的毒性和污染问题, 美国环境保护署(EPA)在其制定的优先控制污染物名单中涵盖了6种PAEs[10], 我国水中优先控制污染物黑名单中包含了3种PAEs[11]。
饮用水水源地水质中含有的PAEs可以通过生物链在虾类、鱼类等水生生物体内蓄积[2], 对水生生态环境造成危害。一些研究者对饮用水水源地PAEs开展了广泛的调查研究, 发现我国主要的水源地河流、水库库区均检出PAEs[12-19]。其中, 黄河中下游干流水体中ρ(PAEs)为3.99~45.45 μg·L-1, 支流水体为15.80~349.53 μg·L-1[12]; 长江武汉段水体中ρ(PAEs)为0.034~132.12 μg·L-1[13-15], 沉积物中w(PAEs)为76.3~450.4 μg·g-1[13, 15]; 重庆两江源水中检出3种PAEs污染物, 其中邻苯二甲酸二异丁酯(DiBP)、邻苯二甲酸二正丁酯(DnBP)质量浓度分别达13.24和9.48 μg·L-1[16]; 三峡库区的几个断面水样中PAEs检出率也很高[17]。天津海河中DnBP和邻苯二甲酸二(2-乙基己基)酯(DEHP)质量浓度分别为0.35~40.68和3.54~101.1 μg·L-1[18]; 第二松花江下游水中ρ(DnBP)均值为717.24 μg·L-1, ρ(DEHP)为370.02 μg·L-1[19], 除了河流, 一些观赏景区湖泊中PAEs污染状况已不容乐观。在对贵州红枫湖的调查中, 大多数湖水水样中均可检出PAEs[20]; 南京玄武湖湖水样中均可检出6种PAEs, 质量浓度ρ达861~2 896 μg·L-1[21]; 安徽巢湖水体达3.65~250.98 μg·L-1[22]。
骆马湖是江苏省4大湖泊之一, 地处江苏省北部, 地跨宿迁、徐州二市, 共辖9个乡镇57个行政村。湖区南北直线长度约27 km, 东西平均宽13 km, 总面积375 km2。骆马湖作为典型的过水性湖泊, 具有防洪、灌溉等功能[23], 是徐州市除微山湖外, 另一个重要的饮用水水源地, 同时也是南水北调东线工程重要的中转站[23], 主要入湖河流有沂河、中运河及房亭河, 出湖河流主要有中运河南段、新沂河和徐洪河。工业废水、畜禽养殖废水和生活污水的下泄对水质造成了不良影响, 严重威胁骆马湖饮用水水质和灌溉功能[24]。因此, 该研究对骆马湖水体、沉积物和鱼类样品中11种常见的邻苯二甲酸酯类污染物进行检测, 对骆马湖水体、沉积物和鱼体中PAEs进行检测并开展相应的健康风险评价, 有助于全方位评估骆马湖受PAEs污染状况及可能带来的负面影响。
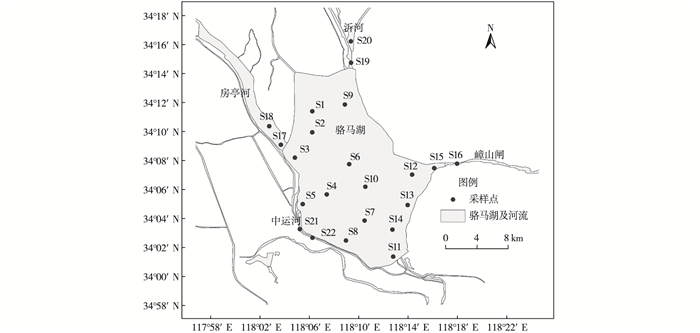
1 材料与方法 1.1 样品采集于2016年4月6日在骆马湖采集样品, 此时骆马湖处于平水期。在骆马湖共设置22个采样点(图 1), 其中, 骆马湖湖体设置14个采样点(S1~S14)、入湖的2条河流房亭河(S17~S18) 和沂河(S19~S20) 各设置2个采样点, 出湖的嶂山闸处(S15~S16) 和中运河南段(S21~S22) 各设置2个采样点。
|
图 1 骆马湖水体、沉积物采样点分布 Figure 1 Distribution of the water and sediment sampling sites in Lake Luoma |
所有采样点均采集水样, 并在湖中选取6个采样点(S1、S3、S9、S10、S11、S12) 采集沉积物样品, 通过现场捕捞方式采集2种湖中优势鱼类草鱼(F1~F4) 和鲈鲫(F5~F6) 作为鱼类样品(共6个)。
采样所用容器包括1 L棕色玻璃广口瓶(水样)、不锈钢饭盒(沉积物样、鱼样), 在使用前均经过正己烷润洗3次, 采样时先用湖水荡洗3次, 避免器皿可能对样品造成的污染。水样采集深度为100~150 cm, 使用铝制采水器采集; 使用金属合金抓斗式采样器采集沉积物。所有样品于采集后12 h内运回实验室, 4 ℃冰箱中保存。
1.2 仪器与试剂 1.2.1 仪器7890A-5975C气相色谱-质谱仪(Agilent, 美国); R210/B491/V850旋转蒸发仪(Buchi, 瑞士), 氮吹仪(EYELA, 日本); 固相萃取装置(Supelco, 美国), ASE300快速溶剂萃取仪(Dionex, 美国); T25均质机(IKA, 德国); 5412离心机(Eppendorf, 德国)。
1.2.2 试剂甲醇、二氯甲烷、正己烷、甲苯、乙腈均为色谱纯, 购自德国Merck公司, 氯化钠和无水硫酸钠为分析纯, 购自南京化学试剂有限公司; 硅藻土购自英国Alfa Aesa公司; 邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二异丁酯(DiBP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二戊酯(DNPP)、邻苯二甲酸二己酯(DNHP)、邻苯二甲酸二环己酯(DHP)、邻苯二甲酸二(2-乙基己基)酯(DEHP)、邻苯二甲酸二苯酯(DPP)和邻苯二甲酸二壬酯(DNP)均购自中国百灵威公司, 邻苯二甲酸二甲氧乙酯(BMEP)购自美国Sigma-Aldrich公司。
1.3 样品前处理 1.3.1 水样前处理Oasis HLB(500 mg, 6 mL)小柱依次用5 mL甲醇、5 mL超纯水活化; 取1 000 mL经玻璃纤维滤膜预滤过的水样, 以5 mL·min-1速度过柱富集。过柱结束后加入10 mL超纯水淋洗小柱, 抽真空干燥30 min, 最后以20 mL二氯甲烷洗脱。将洗脱液在微弱的氮气流中吹干, 最后用1 mL正己烷复溶, 以气相色谱-质谱联用仪(GC/MS)测定。
1.3.2 沉积物样前处理过程称取20 g沉积物样品, 加入10 g硅藻土搅拌均匀, 静置过夜, 使用加速溶剂萃取法(ASE)提取。提取溶剂:V(正己烷):V(二氯甲烷)=1:1;温度:100 ℃;压力:10 342.5 kPa;静态提取时间:5 min;淋洗体积:60%池体积。氮气吹扫60 s, 静态提取2次。提取液转移至浓缩瓶中, 温度控制在40 ℃浓缩至5 mL以下, 加入10 mL正己烷继续浓缩至1 mL待净化。Sep-Pak Silica固相萃取柱依次用4 mL二氯甲烷、10 mL正己烷活化。完全转移萃取浓缩液至萃取柱上, 用20 mL正己烷/二氯甲烷洗脱固相柱。收集流出液浓缩并定容至1 mL, 以GC/MS测定。
1.3.3 鱼样前处理过程称取20 g鱼肉样品(精确至0.01 g)于80 mL离心管中, 加入40 mL乙腈, 用均质器以15 000 r·min-1均质提取1 min, 加入5 g氯化钠, 再匀浆提取1 min, 以4 200 r·min-1离心5 min, 取上清液20 mL, 将提取液于40 ℃水浴中旋转蒸发至约1 mL, 待净化。在Oasis PRiME HLB柱中加入约2 cm高无水硫酸钠, 用10 mL乙腈-甲苯混合液(V:V=3:1) 预洗小柱。将上述样品浓缩液过柱, 用V(乙腈):V(甲苯)=3:1洗涤样液瓶, 洗涤3次, 每次2 mL, 并将洗涤液移入柱中, 再用15 mL乙腈-甲苯混合液洗涤小柱, 收集上述所有洗涤液于鸡心瓶中, 并在40 ℃水浴中旋转蒸发浓缩至约0.5 mL。加入正己烷进行溶剂交换2次, 每次5 mL, 最后使样液定容至1 mL, 以GC/MS测定。
1.4 GC / MS测试条件色谱条件:色谱柱, DB-1701(30 m×0.25 mm×0.25 μm)石英毛细管柱; 进样口温度:250 ℃; 进样方式:不分流进样, 0.75 min分流, 分流比为60:1;程序升温:40 ℃保持1 min, 然后以30 ℃·min-1升温至130 ℃, 再以5 ℃·min-1升温至250 ℃, 再以10 ℃·min-1升温至300 ℃, 保持5 min; 载气:高纯氦气; 流量:1.00 mL·min-1; 进样体积:1 μL。
质谱条件:离子源,EI源; 离子源温度,230 ℃; 离子化能量,70 eV; 扫描方式,选择离子扫描。溶剂延迟3 min, 传输线温度为280 ℃。选择离子监测:每种化合物分别选择1个定量离子, 1~2个定性离子。每组需要检测的离子按照出峰顺序分时段分别检测。具体的定量和定性离子见表 1。
|
|
表 1 11种邻苯二甲酸酯定性/定量离子 Table 1 Qualitative / quantitative ions of 11 kinds of PAEs |
采用混合标准外标法定量分析样品中邻苯二甲酸酯。实验的准确性由回收率实验、空白试验(包括现场空白和程序空白)以及实验室单一控制样来保证。测定结果显示, 所有现场空白及程序空白的各项数据均小于检出限, 单一控制样的回收率在可接受范围内。11种邻苯二甲酸酯不同浓度范围的标准曲线相关系数均在0.99以上; 水体中11种邻苯二甲酸酯的检出限0.02~1.06 μg·L-1, 回收率75.2%~119%;沉积物中11种邻苯二甲酸酯的检出限0.03~1.25 μg·kg-1, 回收率77.6%~109%;鱼体内11种邻苯二甲酸酯的检出限0.04~1.17 μg·kg-1, 回收率89.5%~107%。
1.6 健康风险计算PAEs的生物有效性通过液相(胃液+肠液)中PAEs与总PAEs比值得到[25]。
| $ {B_{\rm{A}}} = \frac{{{m_{释放}}}}{{{m_总}}} \times 100\% 。$ | (1) |
式(1) 中, BA为PAEs在胃肠环境下的生物有效性; m释放为污染物溶解到胃肠液中的质量,kg; m总为污染物在基质中的总质量, kg。
| $ {E_{{\rm{DI}}}} = \frac{{{C_{\rm{F}}} \times {I_{\rm{R}}} \times {E_{\rm{F}}} \times {E_{\rm{D}}}}}{{{B_{\rm{W}}} \times {A_{\rm{T}}}}}。$ | (2) |
式(2) 中, EDI为每日有效暴露量, μg·kg-1·d-1; CF为水和食物中PAEs质量分数, mg·kg-1; IR为水和食物的消费速率, kg·d-1; EF为暴露频率, d·a-1; ED为暴露持续时间,a; BW为体重,kg; AT为平均接触时间,d; BA为胃肠环境下的生物有效性。
根据上述2个等式对居民PAEs日均暴露量进行估算。
将已经获得的暴露量与欧洲食品安全局和美国EPA提出的暴露指导值或参考剂量(RfD)、每日耐受摄入量、每日允许摄入量(ADI)等值进行比较, 若比值小于1, 则表明暴露的PAEs急性暴露风险在可接受的风险范围内;比值大于1, 则表明PAEs构成急性暴露风险。有毒物质的接触风险大小可用接触风险指数(ERI)来表示[26]。
| $ {E_{{\rm{RI}}}} = {E_{{\rm{DI}}}}/{S_i}。$ | (3) |
式(3) 中, ERI为接触风险指数;Si为PAEs用于比较的标准值, 包括暴露指导值、参考剂量值、每日耐受剂量、每日允许浓度等。
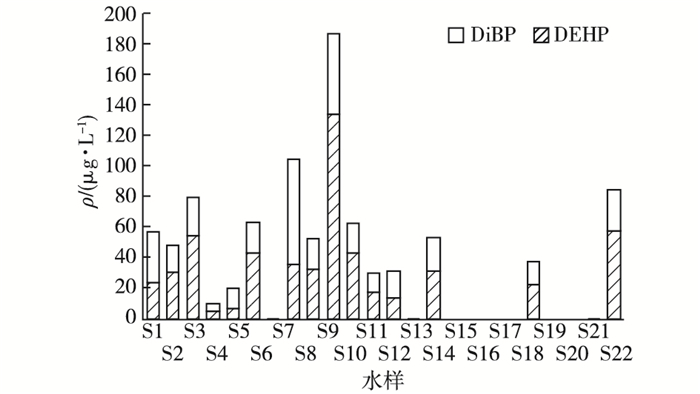
2 结果与讨论 2.1 水体中的PAEs如图 2所示,骆马湖22个采样点水体中检出的PAEs包括DiBP和DEHP 2种, 共有17个采样点位水体检出, 总ρ(PAEs)范围为ND~186.8 μg·L-1, 其中骆马湖湖体的14个采样点全部检出, ρ为0.05~186.8 μg·L-1 (平均值52.94 μg·L-1); 入湖河流的4个采样点位中仅房亭河(S18) 检出, ρ为37.44 μg·L-1; 出湖河流的4个采样点位中仅中运河南段(S22) 检出, ρ为84.16 μg·L-1。在检出的样品中, 每个点位的ρ(DiBP)和ρ(DEHP)相当, 分别为0.03~133.70和0.03~68.81 μg·L-1。DiBP和DEHP是环境介质中检出PAEs的常见类别[12-15, 22]。与国内其他湖泊相比, 骆马湖水体的PAEs污染处于较低水平[19-22]。湖水中PAEs普遍检出, 而入湖和出湖河流中PAEs检出比例较低, 瞬时性是可能的原因, 即由于河流中水样的流动性较强, 为短时间内的PAEs污染水平, 而湖水的驻留时间较长, 反映的是骆马湖水体相对长期的污染平均水平。此外, 也可能湖泊内存在除入湖河流外的其他PAEs污染源, 包括沉积物中PAEs再平衡入湖也可能是原因之一。
|
图 2 骆马湖表层水体中PAEs浓度 Figure 2 PAEs concentrations in the surface water of Lake Luoma |
骆马湖湖底沉积物检出的PAEs有2种(图 4), 与湖水中检出的种类一致, w范围为786.5~1 138 μg·kg-1。其中, w(DiBP)较高, 为751~1 112 μg·kg-1; w(DEHP)较低, 为21.20~59.45 μg·kg-1。DiBP和DEHP的沉积物-水分配系数(KOC)分别为1 020和2.2×104~1×106 L·kg-1[1], 表明DEHP较DiBP更易富集于沉积物、土壤和悬浮颗粒物中。而骆马湖沉积物中w(DiBP)比w(DEHP)高数倍(图 3)。一方面可能是由于DEHP更易发生生物降解[26-27]; 另一方面可能是由于DiBP污染较为严重, 在沉积物中富集周期长, 含量高, DEHP污染周期较短, 尚未在沉积物中大量富集。

|
图 3 骆马湖沉积物中PAEs浓度 Figure 3 PAEs concentrations in the sediments in Lake Luoma |
|
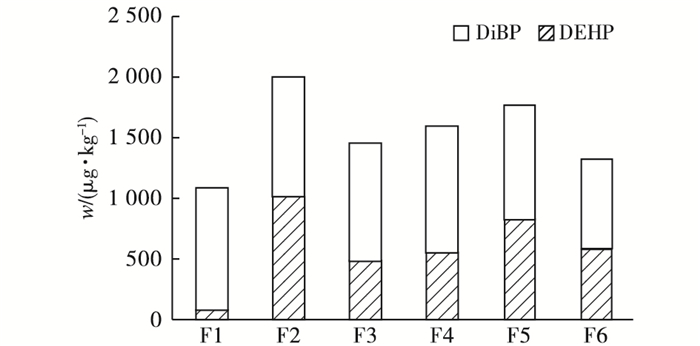
图 4 骆马湖鱼体中PAEs浓度 Figure 4 PAEs concentrations in the fishes of Lake Luoma |
以平均浓度计, 骆马湖湖水(S1~S14) 中ρ(PAEs)为52.94 μg·L-1, 骆马湖沉积物(S1、S3、S9~S12)w(PAEs)为952.4 μg·kg-1, 沉积物中PAEs含量为水体中PAEs浓度的18倍, 表明PAEs易于在水体沉积物中富集。
2.3 鱼体内的PAEs鱼体中检出的PAEs有2种(图 4), 与湖水、沉积物中检出的PAEs种类一致。其中, w(DiBP)和w(DEHP)相近, 分别为78.49~1 011和746.9~1 042 μg·kg-1, 总w(PAEs)为1 078~1 996 μg·kg-1。鱼体中PAEs的种类与水体中类似。鱼体中w(PAEs)平均值为1 533 μg·kg-1, 是水体中PAEs平均含量的29.0倍, 表明DiBP和DEHP在鱼体中富集, 生物富集系数(BCF)为29.0。
2.4 健康风险评价PAEs进入人体的主要途径是通过饮用水和食物, 而我国自来水厂现有的处理技术并不能有效去除PAEs[28-32], 即使采用臭氧-生物活性炭深度处理技术, 对于相对分子质量较大的DEHP和邻苯二甲酸二辛酯(DOP)去除效果仍旧较差[33]。所以直接采用骆马湖水体和鱼类作为主要暴露途径开展健康风险评估。
2.4.1 暴露评估假设居民每日饮水且消费鱼类采用日均值, 则EF取值365 d·a-1,ED取值1 a,AT取值365 d。CF在水和鱼体中分别取水体ρ(DiBP)、ρ(DEHP)平均值31.14和21.80 μg·L-1, 鱼体w(DiBP)、w(DEHP)平均值584.5和948.8 μg·kg-1; IR对于水和鱼类分别取值1 043(成人)[34]、327 mL·d-1(儿童)[34]和142.2(成人)[34]、50 g·d-1 (儿童)[35]; BW取值60(成人)[36]、15 kg(儿童)[36]; BA取值28.3%(DiBP, 饮水)、46.5%(DEHP, 饮水)[37]、16.8%(鱼类消费)[36]。将上述参数带入公式中计算得出, 骆马湖地区居民暴露量DiBP为0.39 (成人)、0.64 μg·kg-1·d-1 (儿童),DEHP为0.49 (成人)、0.75 μg·kg-1·d-1(儿童)。
2.4.2 风险表征目前国际上尚无权威DiBP的参考剂量值, 该研究采用美国安全品协会的数值(0.098 mg·kg-1·d-1)[38], DEHP以美国EPA规定的参考剂量(0.02 mg·kg-1·d-1)[39]为参考标准, 根据健康风险计算结果, 骆马湖经口摄入的DiBP接触风险指数(ERI)分别为0.004(成人)、0.007(儿童),DEHP为0.02(成人)、0.04(儿童)。因此, 骆马湖居民的PAEs暴露量不会构成急性毒性。但是, 研究表明PAEs具有生物蓄积性[2]和雌激素效应[8], 其蓄积后的慢性毒性不可忽视。从暴露评估和风险表征结果来看, PAEs对儿童的暴露和风险更大, 应该引起重视。
3 结论(1) 在11种PAEs中, 骆马湖水体、沉积物、鱼体中均检出2种PAEs, 分别为DiBP和DEHP。水体(包括湖水和出入湖河流)ρ(PAEs)为ND~186.78 μg·L-1 (平均值39.22 μg·L-1); 沉积物污染水平较为一致, w(PAEs)为786.5~1138 μg·kg-1 (平均值952.4 μg·kg-1); 鱼体中w(PAEs)为1 078~1 996 μg·kg-1 (平均值1 533 μg·kg-1)。
(2) 骆马湖水体、沉积物、鱼体内PAEs分布规律呈现浓度增加的趋势, 表明PAEs(主要为DiBP和DEHP)具有生物富集性。
(3) 与国内其他水源地相比, 骆马湖PAEs污染水平较低, 但由于PAEs具有持久性和蓄积性, 应加强污染防护, 防止水质继续恶化, 以免影响其水源地的功能。
(4) 健康风险评价结果表明, 骆马湖周边居民PAEs暴露量不会构成急性毒性, 但是具有蓄积性, 长期的慢性毒性值得关注, 尤其是儿童的暴露风险较高, 应引起重视。
骆马湖面积较大, 沉积物特性变化较大, 且该研究中的样品采集仅进行1次, 对于骆马湖的风险表征存在一定的不确定性因素, 需要开展进一步的调查研究全面评估骆马湖水体污染状况。
| [1] |
NET S, SEMPÉRÉ R, DELMONT A, et al. Occurrence, Fate, Behavior and Ecotoxicological State of Phthalates in Different Environmental Matrices[J]. Environmental Science & Technology, 2015, 49(7): 4019-4035. (  0) 0) |
| [2] |
PEIJNENBURG W J G M, STRUIJS J. Occurrence of Phthalate Esters in the Environment of the Netherlands[J]. Ecotoxicology and Environmental Safety, 2006, 63(2): 204-215. DOI:10.1016/j.ecoenv.2005.07.023 (  0) 0) |
| [3] |
ZHANG L, LIU J, LIU H, et al. The Occurrence and Ecological Risk Assessment of Phthalate Esters (PAEs) in Urban Aquatic Environments of China[J]. Ecotoxicology, 2015, 24(5): 967-984. DOI:10.1007/s10646-015-1446-4 (  0) 0) |
| [4] |
崔学慧, 李炳华, 陈鸿汉, 等. 中国土壤与沉积物中邻苯二甲酸酯污染水平及其吸附研究进展[J]. 生态环境学报, 2010, 19(2): 472-479. CUI Xue-hui, LI Bing-hua, CHEN Hong-han, et al. A Review of Phthalic Acid Esters Contamination and Sorption in Soil and Sediment, China[J]. Ecology and Environmental Sciences, 2010, 19(2): 472-479. (  0) 0) |
| [5] |
胡雄星, 韩中豪, 刘必寅, 等. 邻苯二甲酸酯的毒性及其在环境中的分布[J]. 环境科学与管理, 2007, 32(1): 37-40. HU Xiong-xing, HAN Zhong-hao, LIU Bi-yin, et al. Distribution of Phthalic Acid Esters in Environment and Its Toxicity[J]. Environmental Science and Management, 2007, 32(1): 37-40. (  0) 0) |
| [6] |
马宁, 徐海滨. 邻苯二甲酸二异丁酯的毒理学研究进展[J]. 中国食品卫生杂志, 2010, 22(5): 467-470. MA Ning, XU Hai-bin. Progress on Toxicology of Diisobutyl Phthalate[J]. Chinese Journal of Food Hygiene, 2010, 22(5): 467-470. (  0) 0) |
| [7] |
HARRIS C A, HENTTU P, PARKER M G, et al. The Estrogenic Activity of Phthalate Esters in Vitro[J]. Environmental Health Perspectives, 1997, 105(8): 802-811. DOI:10.1289/ehp.97105802 (  0) 0) |
| [8] |
MOORE N P. The Oestrogenic Potential of the Phthalate Esters[J]. Reproductive Toxicology, 2000, 14(3): 183-192. DOI:10.1016/S0890-6238(00)00068-X (  0) 0) |
| [9] |
CHEN X, XU S, TAN T, et al. Toxicity and Estrogenic Endocrine Disrupting Activity of Phthalates and Their Mixtures[J]. International Journal of Environmental Research and Public Health, 2014, 11(3): 3156-3168. DOI:10.3390/ijerph110303156 (  0) 0) |
| [10] |
EPA-440/5-80-067, Ambient Water Quality Criteria for Phthalate Esters[S].
(  0) 0) |
| [11] |
周文敏, 傅德黔, 孙宗光. 水中优先控制污染物黑名单[J]. 中国环境监测, 1990(4): 1-3. ZHOU Wen-min, FU De-qian, SUN Zong-guang. The Black List of Priority Pollutants in water[J]. Environmental Monitoring in China, 1990(4): 1-3. (  0) 0) |
| [12] |
沙玉娟, 夏星辉, 肖翔群. 黄河中下游水体中邻苯二甲酸酯的分布特征[J]. 中国环境科学, 2006, 26(1): 120-124. SHA Yu-juan, XIA Xing-hui, XIAO Xiang-qun. Distribution Characters of Phthalic Acid Ester in the Waters Middle and Lower Reaches of the Yellow River[J]. China Environmental Science, 2006, 26(1): 120-124. (  0) 0) |
| [13] |
王凡, 沙玉娟, 夏星辉, 等. 长江武汉段水体邻苯二甲酸酯分布特征研究[J]. 环境科学, 2008, 29(5): 1163-1169. WANG Fan, SHA Yu-juan, XIA Xing-hui, et al. Distribution Characteristics of Phthalic Acid Esters in the Wuhan Section of the Yangtze River[J]. Environmental Science, 2008, 29(5): 1163-1169. (  0) 0) |
| [14] |
张彦鹏, 周爱国, 刘存富, 等. 长江流域武汉段水体中邻苯二甲酸酯含量研究[J]. 环境科学与技术, 2011, 34(11): 130-134. ZHANG Yan-peng, ZHOU Ai-guo, LIU Cun-fu, et al. Phthalic Acid Esters in Wuhan Section of Yangtze River[J]. Environmental Science and Technology, 2011, 34(11): 130-134. DOI:10.3969/j.issn.1003-6504.2011.11.027 (  0) 0) |
| [15] |
FAN W, XIA X H, SHA Y J. Distribution of Phthalic Acid Esters in Wuhan Section of the Yangtze River, China[J]. Journal of Hazardous Materials, 2008, 154(1/2/3): 317-324. (  0) 0) |
| [16] |
杜娴. 重庆主城两江水体与沉积物中邻苯二甲酸酯和多环芳烃污染水平及特征[D]. 重庆: 重庆大学, 2012. DU Xian.Levels and Characteristics of Phthalate Esters and Polycyclic Aromatic Hydrocarbons in the Yangtze River and Jialing River From Chongqing's Urban Areas[D].Chongqing:Chongqing University, 2012. (  0) 0) |
| [17] |
许川, 舒为群, 罗财红, 等. 三峡库区水环境多环芳烃和邻苯二甲酸酯类有机污染物健康风险评价[J]. 环境科学研究, 2007, 20(5): 57-60. XU Chuan, SHU Wei-qun, LUO Cai-hong, et al. Water Environmental Health Risk Assessment of PAHs and PAEs in the Three Gorges Reservoir[J]. Research of Environmental Sciences, 2007, 20(5): 57-60. (  0) 0) |
| [18] |
JIE C. Phthalate Acid Esters in Potamogeton crispus L. From Haihe River, China[J]. Chemosphere, 2009, 77(1): 48-52. DOI:10.1016/j.chemosphere.2009.05.043 (  0) 0) |
| [19] |
陆继龙, 郝立波, 王春珍, 等. 第二松花江中下游水体邻苯二甲酸酯分布特征[J]. 环境科学与技术, 2007, 30(12): 35-37. LU Ji-long, HAO Li-bo, WANG Chun-zhen, et al. Distribution Characteristics of Phthalic Acid Esters in Middle and Lower Reaches of No. 2 Songhua River[J]. Environmental Science and Technology, 2007, 30(12): 35-37. DOI:10.3969/j.issn.1003-6504.2007.12.013 (  0) 0) |
| [20] |
王超英, 李碧芳, 郝金声, 等. 红枫湖及其污染源中邻苯二甲酸酯类化合物的测定[J]. 贵州教育学院学报(自然科学), 2006, 17(4): 42-44. WANG Chao-ying, LI Bi-fang, HAO Jin-sheng, et al. Determination of Phthalae Esters in Hongfeng Lake and Its Pollution Source[J]. Journal of Guizhou Education Institute (Natural Science), 2006, 17(4): 42-44. (  0) 0) |
| [21] |
张付海. 巢湖水中五种邻苯二甲酸酯的检测和微生物降解研究[D]. 合肥: 安徽农业大学, 2005.
(  0) 0) |
| [22] |
申艳艳, 许茜, 殷雪琰, 等. 玄武湖中邻苯二甲酸酯的测定及分布特征[J]. 东南大学学报(自然科学版), 2010, 40(6): 1337-1341. SHEN Yan-yan, XU Qian, YIN Xue-yan, et al. Determination and Distribution Features of Phthalate Esters in Xuanwu Lake[J]. Journal of Southeast University (Natural Science Edition), 2010, 40(6): 1337-1341. (  0) 0) |
| [23] |
申霞, 洪大林, 谈永锋, 等. 骆马湖生态环境现状及其保护措施[J]. 水资源保护, 2013, 29(3): 39-43. SHEN Xia, HONG Da-lin, TAN Yong-feng, et al. Ecological Environment of Luoma Lake and Protection Measures[J]. Water Resources Protection, 2013, 29(3): 39-43. (  0) 0) |
| [24] |
叶玲. 骆马湖面临的环境问题和保护对策[J]. 污染防治技术, 2015, 28(6): 87-88, 96. YE Ling. The Environmental Problems and Protection Countermeasures of Luoma Lake[J]. Pollution Control Technology, 2015, 28(6): 87-88, 96. (  0) 0) |
| [25] |
曾锋, 傅家谟, 盛国英, 等. 不同菌源的微生物对邻苯二甲酸二异丁酯(DIBP)生物降解性的比较[J]. 中国环境科学, 1999, 19(4): 322-324. ZENG Feng, FU Jia-mo, SHENG Guo-ying, et al. The Comparative Study of Biodegradability of Diisobutyl Phthalate (DIBP) by Microorganisms From Different Bacteria Sources[J]. China Environmental Science, 1999, 19(4): 322-324. (  0) 0) |
| [26] |
柴素芬, 曾锋, 傅家谟, 等. DEHP的微生物降解性研究[J]. 中山大学学报(自然科学版), 2000, 39(4): 57-60. CHAI Su-fen, ZENG Feng, FU Jia-mo, et al. Study of Biodegradability of Di(2-Ethylhexyl) Phthalate[J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2000, 39(4): 57-60. (  0) 0) |
| [27] |
于涵, 胡建英, 金晓辉, 等. 北方某水厂原水和处理过程中邻苯二甲酸酯类的监测[J]. 给水排水, 2005, 31(6): 20-23. YU Han, HU Jian-ying, JING Xiao-hui, et al. Determination of Phthalic Acid Ester in Waterworks in North China[J]. Water & Wastewater Engineering, 2005, 31(6): 20-23. (  0) 0) |
| [28] |
郑永红, 张治国, 高良敏. 饮用水中邻苯二甲酸酯的调查及去除研究[J]. 水处理技术, 2013, 39(6): 17-19, 23. ZHENG Yong-hong, ZHANG Zhi-guo, GAO Liang-min. Study on Investigation and Removal of Phthalate Esters in Drinking Water[J]. Technology of Water Treatment, 2013, 39(6): 17-19, 23. (  0) 0) |
| [29] |
吴平谷, 韩关根, 王惠华, 等. 饮用水中邻苯二甲酸酯类的调查[J]. 环境与健康杂志, 1999, 16(6): 338-339. WU Ping-gu, HAN Guan-gen, WANG Hui-hua, et al. An Investigation on Phthalates in Drinking Water[J]. Journal of Environment and Health, 1999, 16(6): 338-339. (  0) 0) |
| [30] |
张付海, 张敏, 朱余, 等. 合肥市饮用水和水源水中邻苯二甲酸酯的污染现状调查[J]. 环境监测管理与技术, 2008, 20(2): 22-24. ZHANG Fu-hai, ZHANG Min, ZHU Yu, et al. Investigation of Pollution Status of Phthalates in Drinking Water and Water Source in the City of Hefei[J]. The Administration and Technique of Environmental Monitoring, 2008, 20(2): 22-24. (  0) 0) |
| [31] |
高旭, 余仲勋, 郭劲松, 等. 臭氧-生物活性炭工艺对饮用水中邻苯二甲酸酯类的去除中试研究[J]. 环境工程学报, 2011, 5(8): 1773-1778. GAO Xu, YU Zhong-xun, GUO Jin-song, et al. Pilot Study on Removal of Phthalate Esters From Drinking Water Using Ozone-Zeolite/Activated Carbon Filler Technique[J]. Chinese Journal of Environmental Engineering, 2011, 5(8): 1773-1778. (  0) 0) |
| [32] |
于云江, 叶昊, 杨彦, 等. 太湖流域(苏南地区)经口介质中邻苯二甲酸酯的生物有效性及人体暴露评估[J]. 环境化学, 2014, 33(2): 194-205. YU Yun-jiang, YE Hao, YANG Yan, et al. The Bioaccessibility and Exposure Assessment of PAEs via Oral Media in Taihu Lake Basin of South Jiangsu Province[J]. Environmental Chemistry, 2014, 33(2): 194-205. DOI:10.7524/j.issn.0254-6108.2014.02.007 (  0) 0) |
| [33] |
EPA/600/R-09/052A, Exposure Factors Handbook:2011 Edition[S].
(  0) 0) |
| [34] |
LEUNG S S, CHAN S M, LUI S, et al. Growth and Nutrition of Hong Kong Children Aged 0-7 Years[J]. Journal of Paediatrics and Child Health, 2000, 36(1): 56-65. DOI:10.1046/j.1440-1754.2000.00441.x (  0) 0) |
| [35] |
CHENG Z, NIE X P, WANG H S, et al. Risk Assessments of Human Exposure to Bioaccessible Phthalate Esters Through Market Fish Consumption[J]. Environment International, 2013, 57/58: 75-80. DOI:10.1016/j.envint.2013.04.005 (  0) 0) |
| [36] |
杨彦, 于云江, 杨洁, 等. 太湖流域人群活动行为模式暴露参数研究[J]. 环境与健康杂志, 2013, 30(3): 230-234. YANG Yan, YU Yun-jiang, YANG Jie, et al. Exposure Parameters of Human Activity Pattern in Taihu Lake Basin[J]. Journal of Environmental and Health, 2013, 30(3): 230-234. (  0) 0) |
| [37] |
林钦, 石凤琼, 柯常亮, 等. 水产品中邻苯二甲酸酯残留与健康风险评价研究进展[J]. 南方水产科学, 2014, 10(1): 92-99. LIN Qin, SHI Feng-qiong, KE Chang-liang, et al. Residues of Phthalic Acid Esters in Aquatic Products and Their Health Risk Assessment[J]. South China Fisheries Science, 2014, 10(1): 92-99. (  0) 0) |
| [38] |
KENT R C.Toxicity Review for Diisobutyl Phthalate (DiBP, CSARN 84-69-5).U. S. Consumer Product Safety Commission[EB/OL].[2013-08-01].http://www.cpsc.gov/PageFiles/125773/dibp.pdf.
(  0) 0) |
| [39] |
US EPA.Di(2-ethylhexyl)Phthalate (DEHP) (CASRN 117-81-7), Integrated Risk Information System, U. S. Environmental Protection Agency[EB/OL].http://www.epa.gov/iris/subst/0014.htm.
(  0) 0) |




