2. 扬州大学环境科学与工程学院, 江苏 扬州 225100
2. School of Environmental Science and Engineering, Yangzhou University, Yangzhou 225100, China
中国的秸秆年均产生量为7.35亿t, 包括田间秸秆6.46亿t[1], 其中, 约23%进行露天焚烧处置, 排放的污染物对全国有害物质总排放量的贡献巨大[2]。张斯梅等[3]调查发现江苏省稻麦秸秆被遗弃和焚烧的比例在55%以上。秸秆综合利用对稳定农业生态平衡、缓解资源约束、减轻环境压力都具有十分重要的意义。近年来, 土壤碳固定已经成为陆地生态系统碳循环的研究热点, 秸秆还田也是一种有效的土壤固碳途径。李玮等[4]在砂姜黑土上进行4 a的秸秆还田定位试验, 结果表明秸秆还田能显著提高砂姜黑土耕层土壤总有机质、活性有机质含量和碳库管理指数。
鉴于传统秸秆还田存在诸如肥效缓慢、化感物质积累、病虫害风险加重等问题[5], 秸秆发酵床垫料化还田[6]和秸秆炭化还田[7]成为新型秸秆还田方式而日益受到人们的关注。秸秆炭化后生成的生物炭是生物质在缺氧或有限氧气供应和相对低温( < 700 ℃)条件下热解得到的富碳固体产物, 由于其具有多孔性、高阳离子交换量和低容重的特性, 能改善土壤的理化性质, 提高微生物多样性, 故在土壤性状改良、环境污染修复和节能减排等方面发挥着重要作用[7-8]。发酵床养殖技术也被称为原位堆肥技术, 是一种利用秸秆等农业废弃物控制畜场粪便排放与污染的生态养殖模式。陆扬等[6]对连续饲养2批肥猪后发酵床垫料植物毒性的研究表明, 发酵床垫料在连续饲养2批肥猪后, 氮、磷、铜含量显著提高, C/N比和N/P比下降, 对植物无毒性作用, 对根的生长有促进作用。其中, 总铜质量分数低于GB 15618—1995《土壤环境质量标准》中规定的铜质量分数限值, 适合作为有机肥还田。
土壤微生物是土壤生态系统养分循环和能量流动的主导者, 对于维持土壤生态系统的稳定性和土壤的可持续利用具有重要作用[9]。秸秆还田等措施可以增加土壤有机质含量, 进而为微生物提供良好的物质基础, 改变了土壤微生物多样性[10]。土壤微生物多样性研究在探索应对全球气候变化、维持生态服务功能及促进土壤持续利用等方面具有重要意义[11]。为了利用作物秸秆提升土壤固碳容量, 土壤微生物碳源利用模式已成为研究热点。
Biolog-ECO微孔板技术是通过测定土壤微生物对31种不同单一碳源底物的代谢活性差异来表征微生物种群多样性, 并以此表征功能微生物种群变化[12]。目前, 关于不同秸秆还田方式的培肥效果及对土壤微生物的增效作用已有很多报道[13]。就土壤碳固定而言, 目前的研究主要集中在土壤固碳容量方面。有关秸秆炭化还田以及秸秆发酵床垫料化还田对土壤微生物碳源利用多样性的研究还较少[14]。笔者以土壤固碳效果定位试验基地为依托, 利用Biolog-ECO微平板鉴定系统, 针对秸秆炭化还田和秸秆发酵床垫料化还田2种新型秸秆还田方式研究土壤微生物群落功能多样性差异, 解析土壤微生物群落功能及其对碳源特异利用的差异。
1 材料与方法 1.1 试验设计试验于2015年在江苏省农业科学院六合基地(32°29′ N, 118°37′ E)试验田进行, 该地区处于江淮分水岭, 属亚热带季风气候区, 年降水量为979.5 mm, 年平均气温为15.5 ℃, 年无霜期为229 d, 年日照时数为2 199.5 h, 四季分明, 雨热同季。前茬为水稻, 供试土壤类型为黄棕壤, 有机质及养分含量低, 属生产力较低的中低产田。生物炭是小麦秸秆在600 ℃条件下经无氧热裂解制成。秸秆发酵床垫料、秸秆+猪粪发酵均为江苏省农业科学院六合现代循环农业基地有机肥厂提供。试验共设5个处理:秸秆发酵床垫料化还田(SP)、秸秆炭化(补施化肥)还田(BR)、秸秆+猪粪发酵还田(OF)、传统施用化肥〔(NH4)2SO4+Ca(H2PO4)2+KCl〕(CF)和不施肥(CK)对照。
各施肥处理等氮量(纯氮, 3.375 t·hm-2)施用, 其中, 猪粪+秸秆施用量为5.21 t·hm-2, 秸秆发酵床垫料施用量为7.29 t·hm-2, 化肥小区复合肥〔(NH4)2SO4+Ca(H2PO4)2+KCl〕施用量为1.5 t·hm-2, 秸秆生物炭施用量为1.458 t·hm-2(生物炭小区与有机肥小区总碳施用量相同, 所缺氮素由复合肥补充的量为1.41 t·hm-2)。供试土壤及肥料基本理化性状见表 1。试验田各小区具有独立灌排水系统, 面积为96 m2 (8 m×12 m)。试验小区采用单因素裂区、随机区组排列方式, 每个处理设4个重复。在水稻播种前将肥料施入土表, 翻耕使之与土壤充分混合, 翻耕深度为20 cm, 然后耙平。供试水稻品种为南粳9108, 种植密度为2.49×105株·hm-2, 行距为20 cm, 2015年6月播种。
|
|
表 1 供试土壤、有机肥及生物炭的基本性质 Table 1 Basic properties of the soil, composts and biochar tested in the study |
于8月17日水稻分蘖期采样, 五点法分0~5、>5~10和>10~20 cm土层采集土样, 装无菌袋带回室内, 并置于4 ℃冰箱内保存。
称取5 g新鲜土样加入250 mL三角瓶中, 加入45 mL经灭菌的w= 0.85%的NaCl溶液, 25 ℃、200 r·min-1、黑暗条件下振荡60 min。静置30 min, 使大的土壤颗粒沉淀下来, 然后逐步稀释得到10-2、10-3梯度土壤悬液。将10-3稀释液接种到Biolog-ECO平板中, 每孔150 μL, 恒温培养箱(25±1) ℃中培养168 h。温育过程中分别于0、24、48、72、96、120、144和168 h时用Biolog读数仪在750和590 nm处读数[15]。微生物代谢活性用590 nm处的吸光度减去750 nm处的吸光度表示, 其中, 数值为负值时按0处理[16]。
1.3 数据处理与统计分析孔的平均颜色变化率(average well color development, AWCD, IAWCD), 即孔的平均吸光度计算公式[17]为
| $ {I_{{\rm{AWCD}}}} = \sum {({C_i}-R)/n} 。$ | (1) |
式(1) 中, Ci为各孔吸光度, 用590 nm处吸光度与750 nm处吸光度差值表示; R为对照孔吸光度; n为微平板中碳源种类(该研究中为31)。
样品多样性指数的计算参照MAGURRAN[18]的方法。土壤微生物群落功能多样性分析采用温育反应数据进行分析。土壤微生物群落功能多样性以Simpson、McIntosh和Shannon 3种指数来表征[19]。
采用SPSS 19.0软件对土壤微生物碳源利用多样性进行主成分分析(principal component analysis, PCA)。采用Origin 8.0软件进行统计分析与制图, 采用最小显著差数法(LSD)对不同处理间差异显著性进行检验。
结合有机化合物官能团、微生物生理代谢途径和生态功能3个方面, 将Biolog-ECO板的31种碳源底物分为糖类及其衍生物、羧酸、氨基酸、多聚物、酚酸类和胺类6类[17]。在计算土壤微生物对不同碳源的相对利用率时, 选取温育96 h的吸光度进行分析, 因为此时的微生物碳源基本稳定。微生物对6类碳源的相对利用率以每类碳源Biolog-ECO板对应孔的平均颜色变化率(AWCD)为指标[20-21]。
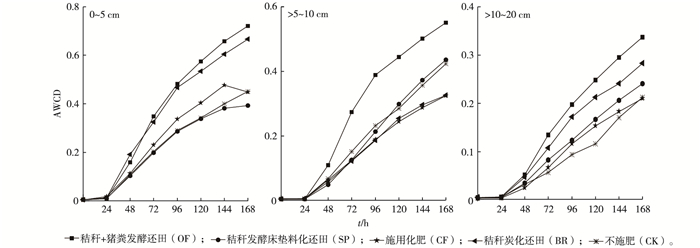
2 结果与分析 2.1 AWCD值变化特征分别计算31种碳源的AWCD值(图 1), 在同一土层, 随着培养时间的延长, 微生物利用碳源量呈逐渐增加趋势。就土壤耕作表层(0~5 cm)而言, 培养24 h时AWCD值开始迅速升高, 156 h时趋于平稳。对比不同秸秆还田方式的微生物AWCD值发现, 96 h时OF处理比SP处理高68.0%, BR处理比CF处理高38.7%。培养结束时, BR和OF处理显著高于其他处理, SP、CF和CK处理之间无显著差异。在耕作亚表层(>5~10 cm), 培养24 h时AWCD值开始迅速升高, 96 h时OF处理比SP处理高82.88%, CF处理比BR处理高1.6%, 截至培养结束168 h时尚未趋于平稳, 此时OF处理显著高于CF和BR处理。在耕作底层(>10~20 cm), 培养24 h时AWCD值开始迅速升高, 96 h时OF处理比SP处理高61.11%, BR处理比CF处理高48.41%。随着培养时间的延长, 差异越来越大, 截至168 h时尚未趋于平稳, 此时OF处理显著高于CF、SP和CK处理。不同土层微生物碳源利用能力由大到小依次为0~5、>5~10和>10~20 cm, 说明随着土层的加深, 微生物的碳源利用能力下降。在耕作层(0~20 cm), OF处理对土壤微生物活性的促进作用比其他处理明显。
|
图 1 不同耕层和秸秆还田方式下Biolog-ECO板上的平均颜色变化率(AWCD) Figure 1 AWCD (average well color development) on Biolog-ECO relative to straw incorporation pattern and soil layer |
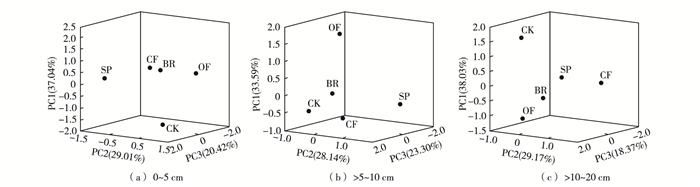
在31种因子中提取3个主成分因子, 各土层第1、2、3主成分累计贡献率均在85%以上, 其余各主成分的贡献率很小, 因此, 用前3个主成分得分来表征不同秸秆还田方式下土壤微生物群落对贡献率较高碳源的代谢特征。图 2中, 样品间得分距离越小, 表示样品间对碳源利用能力相似程度越高。如图 2所示, 在0~5 cm土层CF和BR处理得分接近, OF和SP处理得分距离相差较大。这说明CF和BR处理土壤微生物碳利用多样性十分相似。而OF和SP处理土壤微生物碳利用多样性相差较大。在>5~10 cm土层CF和BR处理得分接近, 同时OF和SP处理得分距离较大, 与0~5 cm土层在得分上有所不同, 却呈现相同的变化趋势。在>10~20土层各处理间得分有较好的分散, 而且各施肥处理得分均低于不施肥对照。可见, 外加碳源能激发表层土壤微生物活性, 相应地减弱耕作底层土壤微生物活性, 秸秆以不同方式施用对土壤微生物碳利用有显著影响。
|
图 2 不同耕层和秸秆还田方式下土壤AWCD主成分分析 Figure 2 PCA of AWCD relative to straw incorporation pattern and soil layer |
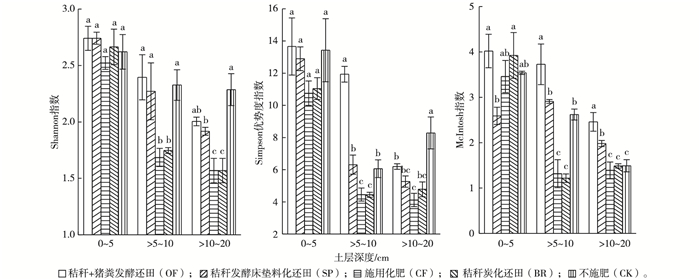
不同施肥处理Shannon指数、Simpson优势度指数和McIntosh指数随土层深度的变化见图 3。不同施肥处理Shannon指数、Simpson优势度指数和McIntosh指数均随着土层的加深而有所下降, 说明土层越深, 土壤微生物多样性越小。不同还田方式之间0~5 cm土层微生物Shannon指数和Simpson指数均无显著差异。在>5~10 cm土层, CF和BR处理土壤微生物多样性指数小于SP和OF处理, 且达到显著水平(P < 0.05)。>10~20 cm土层CF和BR处理土壤微生物Shannon指数、McIntosh指数小于SP和OF处理, 达到显著水平(P < 0.05)。这说明与CF和BR处理相比, OF和SP处理能增加农田>5~10和>10~20 cm土层微生物多样性; 而与SP处理相比, OF处理增加农田土壤微生物多样性的效果更明显。可见, 秸秆还田方式显著影响耕作层(0~20 cm)土壤微生物多样性。
|
图 3 不同耕层和秸秆还田方式下微生物多样性指数 Figure 3 Soil microbial diversity index relative to straw incorporation pattern and soil layer |
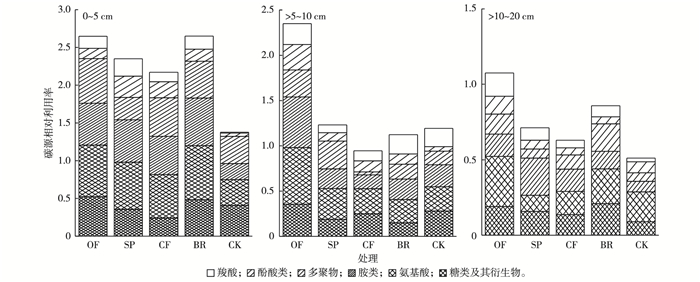
图 4显示不同耕层秸秆还田方式下土壤微生物对6类碳源的相对利用率, 不同秸秆还田方式下0~5 cm土层糖类及其衍生物、氨基酸、胺类、多聚物的相对利用率高于酚酸类和羧酸相对利用率。糖类及其衍生物既是矿化过程的主要物质, 也是大多数异养微生物的重要碳源。在0~5 cm土层, OF处理糖类及其衍生物比SP处理高46.7%, 说明与SP处理相比,OF处理能提高土壤矿化率和异养微生物对碳源的利用; 虽然BR处理土壤中可利用碳少, 但BR处理糖类及其衍生物比CF处理高101.1%, 可能是BR处理可通过改变土壤结构来提高土壤矿化率和异养微生物对碳源的利用。氨基酸是土壤有机氮的重要组成成分, 是植物根系向土壤分泌的大量低分子有机物之一, 是土壤微生物重要的氮源。OF处理土壤微生物对氨基酸的相对利用率比SP处理高9.60%, BR处理比CF处理高24.3%。胺类是由氨分子中的氢被羟基或其他非酸性有机基团取代后衍生的一类有机物, 不同处理土壤微生物对胺类的利用差异较小, 可能是由于土壤中胺类含量较低, 且部分胺类对微生物有毒害作用。羧酸是植物根系分泌物的重要组分, 外加碳源能显著增加土壤微生物对羧酸的利用率, 而各还田方式之间无明显差异, 说明短期还田条件下不同还田方式对植物根系分泌羧酸的影响较小。
|
图 4 不同耕层和秸秆还田方式下土壤微生物对6类碳源的相对利用率 Figure 4 Relative utilization rates of soil carbons of six groups of carbon sources by soil microbes relative to straw incorporation pattern and soil layer OF—秸秆+猪粪发酵还田;SP—秸秆发酵床垫料化还田;CF—施用化肥;BR—秸秆炭化还田;CK—不施肥。 |
不同秸秆还田方式下土壤微生物对多聚物的利用差异较大, OF处理比SP处理高99.0%, 而BR处理与CF处理差异不大。植物通过分泌、淋溶、腐解等途径释放酚酸类物质到土壤中, 对下茬作物产生化感作用。就表层土而言, 与OF处理相比, SP处理提高了土壤微生物对酚酸类化合物的利用, 与CF处理相比, BR处理降低了土壤微生物对酚酸类化合物的利用。统计结果表明, CF处理碳源利用率低于其他处理(CK除外), 施用化肥可减少土壤微生物对糖类及其衍生物、氨基酸、胺类、多聚物的利用。分析耕作层土壤微生物对6种碳源的利用率可以看出, BR和OF处理可促进土壤微生物对碳源的利用。
可见, OF和BR处理能提高表层土碳源利用率, SP处理能提高土壤微生物对较稳定的酚酸类和羧酸类碳源的相对利用率。>10~20 cm土层微生物对稳定性较高的酚酸类和羧酸类碳源相对利用率比0~5 cm土层高。随着土层的加深, 各类碳源相对利用率均有所下降, 各土层碳源相对利用率由大到小依次为0~5、>5~10和>10~20 cm土层。
3 讨论土壤微生物是土壤中比较活跃的成分, 也是土壤物质循环的主动力, 并提供了许多潜在的生态功能。有机物料大都含有丰富的微生物所需的碳源、氮源, 土壤中加入有机物料能够提高有机质含量及微生物群落多样性[22]。AWCD值提供了不同微生物对相同碳源利用的差异性, 反映了微生物对碳源的利用能力, 从功能代谢方面显示了微生物群落结构多样性[23]。笔者分析AWCD值也得到相应结论, OF和SP处理提高了土壤微生物碳代谢能力。郭梨锦等[24]采用磷脂脂肪酸(PLFA)法研究短期耕作和小麦秸秆还田对稻田表层(0~5 cm)土壤微生物群落结构和多样性的结果表明, 秸秆还田提高了表层土壤微生物生物量和微生物多样性。顾美英等[25]利用Biolog对碳源分析的结果表明, 不同秸秆还田方式(秸秆直接还田、过腹还田和炭化还田)均能提高风沙土土壤微生物活性和丰富度指数, 且主成分分析也表明, 不同秸秆还田方式处理土壤微生物群落明显不同。笔者研究中SP、BR和OF处理均提高土壤微生物群落多样性指数, 主成分分析也表明不同秸秆还田方式处理土壤微生物群落明显不同。
笔者研究表明OF处理在增强土壤微生物多样性(图 3)和提高土壤微生物碳利用率(图 4)上均比SP处理有更大优势。这可能是由于2种有机肥生产过程不同、腐熟程度不同进而导致它们有着不同的性质, 如腐殖酸的结构和含量[26]等。在0~5 cm土层, 与SP处理相比, OF处理能提高微生物对糖类及其衍生物、多聚物的利用能力, 可见, 秸秆+猪粪发酵的腐熟程度比秸秆发酵床垫料高。研究表明, 随着堆肥的进行, 腐殖酸中大分子组分含量明显提高, 有机物中不饱和结构的多聚化或联合程度增大, 芳香结构物质与氨基基团有所增加[27]。然而, 发酵床垫料的生成不是简单的堆肥过程, 作为一种新型有机肥, 其腐熟化方面的研究还较少。秸秆炭化还田是一种理化性质不同于供试有机肥(秸秆+猪粪发酵、秸秆发酵床垫料)的秸秆还田方式。笔者研究中, 主成分分析结果表明0~5 cm土层BR和CF处理得分较近(图 2), 就BR处理而言, 除糖类及其衍生物与氨基酸相对利用率比CF处理高以外, 其余碳源相对利用率均与CF处理接近(图 4)。这可能是由于生物炭不能直接为微生物提供碳源、氮源, 另外, 秸秆炭化还田与施用化肥均没有外源微生物的加入。ABUJABHAH等[28]研究结果表明, 添加生物炭后微生物丰度提高, 但堆肥的影响更大, 笔者研究结果与之一致。其中, BR和CF处理没有直接加入有机质碳源, 可能是由于其本身对土壤原有有机质存在激发作用[29], 或者由于其促进植物生长从而引起植物根际激发效应[30], 进而提高微生物丰度。吕美蓉等[31]采集长期定位有机无机配施小区的土壤样品进行室内培育试验, 比较添加不同肥料养分后土壤微生物群落多样性的短期变化, Biolog主成分分析结果表明改变肥料养分投入在短期内对微生物的碳源利用特征具有显著影响。笔者研究中添加不同肥料养分(无肥料养分, 有机肥料养分或无机肥料养分)处理在PC轴也出现明显分异, 显示出添加不同肥料土壤微生物群落碳源代谢的差异性。
GUO等[32]的研究结果也表明秸秆还田对不同土层有不同作用, 其电镜扫描结果显示秸秆还田能提高表层土壤微生物碳利用多样性, 笔者对0~5 cm土层的研究结果与之一致, 但在>10~20 cm土层不同秸秆还田方式均不同程度地降低土壤微生物活性和丰富度指数。这说明笔者试验中SP、BR和OF处理均增加表层土壤有机质和其他养分含量, 从而增加表层土壤微生物多样性。李晨华等[33]研究结果也表明, 长期施肥改变了土壤剖面碳源与氮源的可利用量, 导致施肥处理间土壤微生物群落结构的差异, 特别是在剖面深层更为明显。而笔者研究中>10~20 cm土层不同秸秆还田土壤微生物多样性差异不明显, 可能是笔者试验的施肥年限较短、耕作底层土壤微生物多样性变化较小的缘故。
4 结论利用Biolog数据, 设置3种秸秆还田方式以及传统施用化肥和不施肥5种处理, 分析还田2个月后水稻田不同耕层土壤微生物的碳源代谢特征, 并对比分析土壤微生物对不同碳源的利用率, 得出以下结论:(1) 不同秸秆还田方式因其结构和理化性质不同, 还田后能显著影响土壤微生物碳代谢特征。秸秆+猪粪发酵还田对土壤微生物碳代谢能力、微生物多样性各项指数以及糖类、氨基酸、胺类和多聚物利用率明显高于其他处理。(2) 不同秸秆还田方式能显著影响土壤微生物多样性。与CF和BR处理相比, OF和SP处理能增加农田耕作亚表层及耕作底层的土壤微生物多样性。
| [1] |
韦茂贵, 王晓玉, 谢光辉. 中国各省大田作物田间秸秆资源量及其时间分布[J]. 中国农业大学学报, 2012, 17(6): 32-44. (  0) 0) |
| [2] |
曹国良, 张小曳, 王亚强, 等. 中国区域农田秸秆露天焚烧排放量的估算[J]. 科学通报, 2007, 52(15): 1826-1831. DOI:10.3321/j.issn:0023-074x.2007.15.017 (  0) 0) |
| [3] |
张斯梅, 杨四军, 石祖梁, 等. 江苏省稻麦秸秆收集利用现状分析及对策[J]. 生态与农村环境学报, 2014, 30(6): 706-710. (  0) 0) |
| [4] |
李玮, 乔玉强, 陈欢, 等. 秸秆还田配施氮肥对砂姜黑土有机质组分与碳库管理指数的影响[J]. 生态与农村环境学报, 2014, 30(4): 475-480. (  0) 0) |
| [5] |
MACDONALD L M, FARRELL M, VAN ZWIETEN L, et al. Plant Growth Responses to Biochar Addition:An Australian Soils Perspective[J]. Biology and Fertility of Soils, 2014, 50(7): 1035-1045. DOI:10.1007/s00374-014-0921-z (  0) 0) |
| [6] |
陆扬, 吴淑杭, 周德平, 等. 发酵床养猪垫料的养分转化与植物毒性研究[J]. 农业环境科学学报, 2011, 30(7): 1409-1412. (  0) 0) |
| [7] |
潘根兴, 张阿凤, 邹建文, 等. 农业废弃物生物黑炭转化还田作为低碳农业途径的探讨[J]. 生态与农村环境学报, 2010, 26(4): 394-400. (  0) 0) |
| [8] |
饶霜, 卢阳, 黄飞, 等. 生物炭对土壤微生物的影响研究进展[J]. 生态与农村环境学报, 2016, 32(1): 53-59. DOI:10.11934/j.issn.1673-4831.2016.01.010 (  0) 0) |
| [9] |
DEGENS B P, SCHIPPER L A, SPARLING G P, et al. Decreases in Organic C Reserves in Soils Can Reduce the Catabolic Diversity of Soil Microbial Communities[J]. Soil Biology and Biochemistry, 2000, 32(2): 189-196. DOI:10.1016/S0038-0717(99)00141-8 (  0) 0) |
| [10] |
罗希茜, 郝晓晖, 陈涛, 等. 长期不同施肥对稻田土壤微生物群落功能多样性的影响[J]. 生态学报, 2009, 29(2): 740-748. (  0) 0) |
| [11] |
贺纪正. 面向未来的土壤微生物生态学研究[C]//面向未来的土壤科学. 成都: 电子科技大学出版社, 2012.
(  0) 0) |
| [12] |
靳蓉, 苏静, 刘红宇, 等. 应用BIOLOG ECO微培养技术研究样品中微生物的碳源代谢特征[C]//第三届全国微生物资源学术暨国家微生物资源平台运行服务研讨会会议论文摘要集. [出版地不详]: [出版者不详], 2011. [s. l. ]: [s. n. ], 2011. ]
(  0) 0) |
| [13] |
李晓莎, 武宁, 刘玲, 等. 不同秸秆还田和耕作方式对夏玉米农田土壤呼吸及微生物活性的影响[J]. 应用生态学报, 2015, 26(6): 1765-1771. (  0) 0) |
| [14] |
BELYAEVA O N, HAYNES R J. Comparison of the Effects of Conventional Organic Amendments and Biochar on the Chemical, Physical and Microbial Properties of Coal Fly Ash as a Plant Growth Medium[J]. Environmental Earth Sciences, 2012, 66(7): 1987-1997. DOI:10.1007/s12665-011-1424-y (  0) 0) |
| [15] |
邹春娇, 齐明芳, 马建, 等. Biolog-ECO解析黄瓜连作营养基质中微生物群落结构多样性特征[J]. 中国农业科学, 2016, 49(5): 942-951. DOI:10.3864/j.issn.0578-1752.2016.05.014 (  0) 0) |
| [16] |
BRADIEY R L, SHIPLEY B, BEAULIEU C. Refining Numerical Approaches for Analyzing Soil Microbial Community Catabolic Profiles Based on Carbon Source Utilization Patterns[J]. Soil Biology and Biochemistry, 2006, 38(3): 629-632. DOI:10.1016/j.soilbio.2005.07.002 (  0) 0) |
| [17] |
CHOI K H, DOBBS F C. Comparison of Two Kinds of Biolog Microplates (GN and ECO) in Their Ability to Distinguish Among Aquatic Microbial Communities[J]. Journal of Microbiological Methods, 1999, 36(3): 203-213. DOI:10.1016/S0167-7012(99)00034-2 (  0) 0) |
| [18] |
MAGURRAN A E. Ecological Diversity and Its Measurement[M]. New Jersey: Princeton University Press, 1988, 43-47.
(  0) 0) |
| [19] |
王秀国. 杀菌剂多菌灵高频投入对土壤微生物群落的影响及其生物修复[D]. 杭州: 浙江大学, 2009.
(  0) 0) |
| [20] |
王军. 莠去津对土壤微生物群落结构及分子多样性的影响[D]. 泰安: 山东农业大学, 2012.
(  0) 0) |
| [21] |
JACKSON L E, CALDERON F J, STEENWERTH K L, et al. Responses of Soil Microbial Processes and Community Structure to Tillage Events and Implications for Soil Quality[J]. Geoderma, 2003, 114(3/4): 305-317. (  0) 0) |
| [22] |
孔维栋, 刘可星, 廖宗文. 有机物料种类及腐熟水平对土壤微生物群落的影响[J]. 应用生态学报, 2004, 15(3): 487-492. (  0) 0) |
| [23] |
郑丽萍, 龙涛, 林玉锁, 等. Biolog-ECO解析有机氯农药污染场地土壤微生物群落功能多样性特征[J]. 应用与环境生物学报, 2013, 19(5): 759-765. (  0) 0) |
| [24] |
郭梨锦, 曹凑贵, 张枝盛, 等. 耕作方式和秸秆还田对稻田表层土壤微生物群落的短期影响[J]. 农业环境科学学报, 2013, 32(8): 1577-1584. DOI:10.11654/jaes.2013.08.013 (  0) 0) |
| [25] |
顾美英, 唐光木, 葛春辉, 等. 不同秸秆还田方式对和田风沙土土壤微生物多样性的影响[J]. 中国生态农业学报, 2016(4): 489-498. (  0) 0) |
| [26] |
SUTTON R, SPOSITO G. Molecular Structure in Soil Humic Substances:The New View[J]. Environmental Science & Technology, 2005, 39(23): 9009-9015. (  0) 0) |
| [27] |
唐景春, 孙青, 王如刚, 等. 堆肥过程中腐殖酸的生成演化及应用研究进展[J]. 环境污染与防治, 2010(5): 73-77. (  0) 0) |
| [28] |
ABUJABHAH I S, BOUND S A, DOYLE R, et al. Effects of Biochar and Compost Amendments on Soil Physico-Chemical Properties and the Total Community Within a Temperate Agricultural Soil[J]. Applied Soil Ecology, 2016, 98: 243-253. DOI:10.1016/j.apsoil.2015.10.021 (  0) 0) |
| [29] |
WANG J Y, XIONG Z Q, KUZYAKOY Y. Biochar Stability in Soil:Meta-Analysis of Decomposition and Priming Effects[J]. Bioenergy, 2015, 8(3): 512-523. (  0) 0) |
| [30] |
孙悦, 徐兴良, YAKOVK. 根际激发效应的发生机制及其生态重要性[J]. 植物生态学报, 2014, 38(1): 62-75. (  0) 0) |
| [31] |
吕美蓉, 李忠佩, 刘明, 等. 长期有机无机肥配合施用土壤中添加不同肥料养分后土壤微生物短期变化[J]. 生态与农村环境学报, 2011, 27(4): 69-73. (  0) 0) |
| [32] |
GUO L J, LIN S, LIU T Q, et al. Effects of Conservation Tillage on Topsoil Microbial Metabolic Characteristics and Organic Carbon Within Aggregates Under a Rice (Oryza sativa L.):Wheat (Triticum aestivum L.) Cropping System in Central China[J]. PLoS One, 2016, 11(1): e0146145. DOI:10.1371/journal.pone.0146145 (  0) 0) |
| [33] |
李晨华, 张彩霞, 唐立松, 等. 长期施肥土壤微生物群落的剖面变化及其与土壤性质的关系[J]. 微生物学报, 2014, 54(3): 319-329. (  0) 0) |




