随着经济的发展, 居民对畜禽产品的消费量增长迅速, 随之产生的废物量也快速增加[1]。我国猪场废弃物年排放总量达60亿t, 且大部分污染物被直接释放到环境中, 成为巨大的污染源[2]。猪场废水为富含大量病原体的高浓度有机废水, 排入水体后易造成地表水和地下水水质的严重恶化[3], 一些有机物成分在环境中存留时间持久, 容易威胁人体健康并引起生态风险[4-6]。
臭氧具有强氧化性, 作为化学氧化方法能从生化处理后的废水中去除有毒化学品和难降解有机物[7-8]。臭氧可以氧化复杂的有机分子、酚类等内分泌干扰化学物质[9], 还可以杀灭细菌, 避免病毒繁殖[10]。目前, 在饮用水和工艺用水等水处理中已进行了大量的臭氧氧化研究[11-13], 臭氧氧化技术应用于降低畜禽养殖废水有机污染物的研究近几年也逐渐被重视[14]。但是对于臭氧氧化的应用潜力还需进一步探讨, 以期降低臭氧对环境的影响, 并减少经济成本使之被大规模应用[15]。
苦草(Vallisneria natans)是一种多年生沉水植物, 广泛分布于我国的各种淡水栖息地[16], 能适应各种各样的环境, 在水生生态系统中发挥着重要的生态功能[17]。沉水植物具有完全水生的特点, 苦草分布广泛,又具有良好的实验特性[18]。笔者以生化处理后的猪场废水为试验材料, 进行臭氧氧化-苦草深度处理研究, 考察了不同浓度臭氧氧化处理中有机物的含量和组分变化, 特别是表征矿化度的可溶性有机碳(DOC)含量、表征芳香族化合物和腐殖质含量的UV254和UV436, 表征可生化性情况的DOC/UV254比值, 臭氧氧化-苦草对有机物的作用效果, 以期为深入探讨臭氧氧化机理及在畜禽养殖废水深度处理方面的研究提供依据。
1 材料与方法 1.1 试验地点与材料试验在上海市农业科学院庄行综合试验基地(30°53′ N, 121°23′ E)进行。水样采集于上海市农业科学院畜牧试验场猪场的处理尾水。该场以养殖生猪为主, 占地面积3.3 hm2, 年出栏数3千余头。猪场废水主要包括尿、粪和猪舍冲洗水。日产废水量约5 t, 排放间隔时间为7 d。猪场废水经格栅、氧化塘、人工湿地处理后排放, 处理后尾水水质情况见表 1。试验于2015年9—10月进行, 每隔7 d采水1次, 共采集4次水样, 采样后尽快进行臭氧氧化处理。
|
|
表 1 猪场处理尾水水质指标 Table 1 Quality of pretreated piggery tail water |
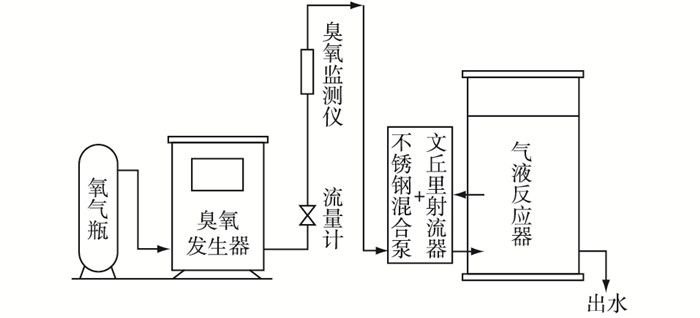
臭氧氧化装置(图 1)由臭氧发生器(WG-S10, 中国威固)、臭氧浓度监测仪(IDEAL-2000, 美国)、不锈钢混合泵(JETB-0.37)、文丘里射流器(A25152) 和气液反应器(不锈钢材质, D=50 cm, H=90 cm)组成。通过臭氧发生器制备臭氧, 臭氧流量为2.5 L·min-1, 由臭氧监测仪在线监测臭氧浓度, 每次处理的水量固定, 设置10、30和50 mg·L-1 3个臭氧投加浓度, 反应时间为30 min, 水温约为20 ℃。处理后的水在通风环境中放置24 h, 保证无剩余臭氧后用于苦草处理, 并采集水样进行指标测定。
|
图 1 臭氧氧化处理装置 Figure 1 Sketch of the apparatus for ozonation treatment |
苦草的培育过程在普通池塘中完成, 采集长势和生长量相对一致的幼苗〔长度约(40±5) cm〕在圆锥形塑料桶(上圆直径40 cm, 下圆直径32 cm, 高56 cm)中培育, 桶中底泥高约15 cm, 每个塑料桶中种植7簇, 每簇2株, 并放入池塘水至淹没叶片, 每个塑料桶下方20 cm处装有排水口。待植物苗进入正常生长阶段(生长旺盛期)并有外扩能力后, 分别加入未处理和不同臭氧浓度处理的水样, 之后每7 d换1次水, 持续4次, 在换水之前进行水样采集。
设CK(对照)、AO1(臭氧投加浓度为10 mg·L-1)、AO2(臭氧投加浓度为30 mg·L-1)、AO3(臭氧投加浓度为50 mg·L-1)4个处理; 各臭氧氧化后的苦草处理方法相同, 每个处理重复3次。
1.4 测定指标与方法溶解性有机碳(DOC)含量采用TOC分析仪(Apollo 9000, Teledyne, 美国)测定; UV254和UV436采用紫外可见分光光度计(UV1801, 中国)测定。半挥发性有机物组分采用气相色谱-质谱联用仪(GCMS-QP2010, 日本岛津)测定。样品预处理采用液液萃取方式[19]。GC-MS分析条件:色谱分离条件为柱温40 ℃保持4 min, 以10 ℃·min-1的速度升到270 ℃, 保持20 min; 离子源温度为200 ℃, 接口温度为280 ℃, 进样口温度为250 ℃, 采用不分流进样方式, 进样时间为2 min, 进样量1 μL; 采用Scan采集方式, 质量范围为35~500 amu, 扫描时间间隔1 s。样品质谱图与数据库(NIST11和NIST11s)进行相似度检索, 保留相似度≥80%的化合物。
1.5 数据统计与分析采用SPSS 13.0软件进行统计分析, Sigmaplot 12.0软件制图。
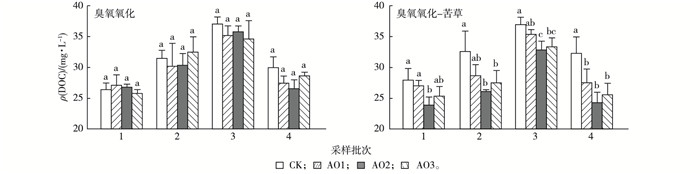
2 结果与分析 2.1 臭氧氧化-苦草处理对猪场尾水中有机碳含量的影响图 2为不同浓度臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水中DOC含量的影响。臭氧投加浓度对DOC含量的影响不显著(P>0.05)。臭氧氧化-苦草处理DOC含量与对照相比显著下降(P < 0.05), 3个不同臭氧投加浓度处理DOC含量分别下降8.5%(AO1)、17.6%(AO2) 和13.8%(AO3)。苦草单独处理对CK的DOC含量无显著影响, 但和臭氧氧化联合作用后对DOC含量影响显著。臭氧单独处理中3个不同投加浓度处理DOC去除率分别为1.3%(AO1)、10.5%(AO2) 和8.0%(AO3)。
|
图 2 不同浓度臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水中可溶性有机碳含量的影响 Figure 2 Dissolved organic carbon(DOC) concentration of the piggery tail water after ozonation or ozonation combined with Vallisneria natans relative to concentration of ozone CK为对照, AO1臭氧投加浓度为10 mg·L-1, AO2臭氧投加浓度为30 mg·L-1, AO3臭氧投加浓度为50 mg·L-1。同一组直方柱上方英文小写字母不同表示同一采样批次不同处理间有机碳含量差异显著(P < 0.05)。 |
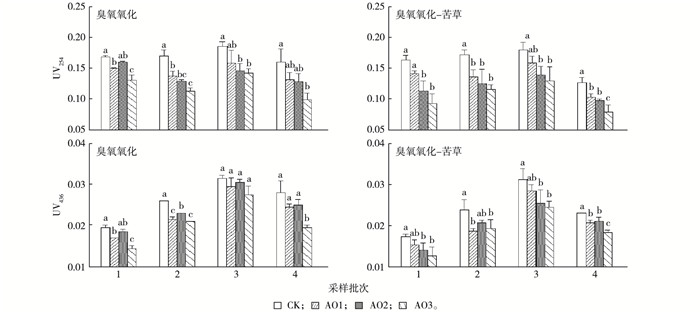
臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水中UV254和UV436均有极显著影响(P < 0.001)。增加臭氧投加浓度可降低水中UV254(图 3), 3个不同臭氧单独氧化水中的UV254分别降低15.6%(AO1)、17.6%(AO2) 和29.4%(AO3)。
|
图 3 不同浓度臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水UV254和UV436的影响 Figure 3 UV254 and UV436 of the piggery tail water after ozonation or ozonation combined with Vallisneria natans relative to concentration of ozone CK为对照, AO1臭氧投加浓度为10 mg·L-1, AO2臭氧投加浓度为30 mg·L-1, AO3臭氧投加浓度为50 mg·L-1。同一组直方柱上方英文小写字母不同表示同一采样批次不同处理间某指标差异显著(P < 0.05)。 |
臭氧氧化-苦草处理水中UV254也有降低趋势, AO1、AO2、AO3处理分别降低16.2%、25.7%和35.3%。苦草单独处理后水中UV254整体呈下降趋势, 但臭氧氧化后UV254降低比例更高, 臭氧单独氧化后水中UV254较CK处理分别下降8.1%(AO1)、15.9%(AO2) 和14.6%(AO3)。
臭氧单独氧化使猪场处理尾水中UV436降低, AO1、AO2和AO3处理分别降低12.2%、7.6%和22.0%。臭氧氧化-苦草处理后水中UV436也有降低趋势, AO1、AO2和AO3处理分别降低12.9%、14.7%和21.8%。苦草单独处理水中UV436亦呈降低趋势, CK处理降低9.9%, AO1、AO2和AO3处理分别降低10.6%、16.9%和9.5%。
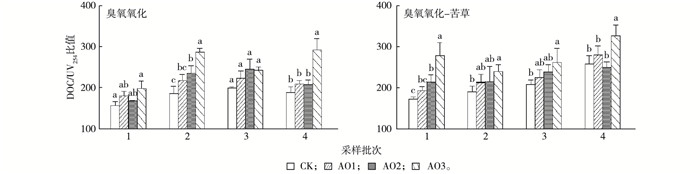
不同浓度臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水中DOC/UV254比值的影响如图 4所示。臭氧单独氧化和臭氧氧化-苦草处理对DOC/UV254比值均有极显著影响(P < 0.001)。随着臭氧投加浓度的增加, DOC/UV254比值有增加趋势, 臭氧单独处理中AO1、AO2和AO3处理的DOC/UV254比值分别增加13.9%、16.7%和39.4%。臭氧氧化-苦草处理亦增加DOC/UV254比值, AO1、AO2和AO3处理分别增加10.3%、12.3%和35.6%。苦草单独处理后, DOC/UV254比值有所增加, CK处理增加13.3%, AO1、AO2和AO3处理则分别增加9.9%、9.1%和11.3%。
|
图 4 不同浓度臭氧单独氧化和臭氧氧化-苦草处理对猪场尾水DOC/UV254比值的影响 Figure 4 DOC/UV254 of the piggery tail water after ozonation or ozonation combined with Vallisneria natans relative to concentration of ozone CK为对照, AO1臭氧投加浓度为10 mg·L-1, AO2臭氧投加浓度为30 mg·L-1, AO3臭氧投加浓度为50 mg·L-1。同一组直方柱上方英文小写字母不同表示同一采样批次不同处理间DOC/UV254比值差异显著(P < 0.05)。 |
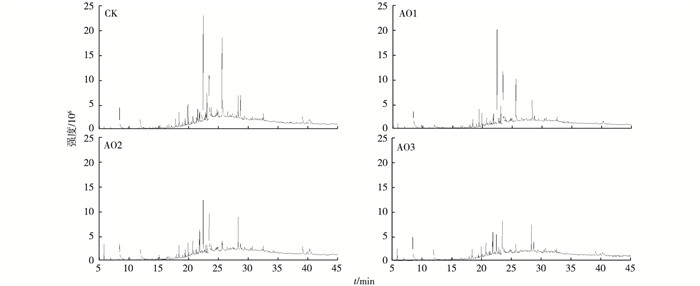
通过GC-MS定性分析以看出, 猪场处理尾水中半挥发性有机物组分复杂(图 5)。从表 2可知, 猪场废水在臭氧氧化前后都含有的有机物有45个, 说明它们属于难被臭氧降解有机物, 其中醇类13个,烷烃类11个,酯类11个,酸类3个,酮类3个,胺类2个,醛类1个,其他类1个。表 5中同样列出了臭氧氧化前后, 养猪废水中半挥发性有机物发生变化的种类。臭氧氧化后, 检测出的有机物数量有减少趋势, AO3处理的水中有机物数量最少, AO1处理的水中有机物数量不降反升, 这是由于其烷烃数量增加的缘故。AO1处理后酯类物质的数量增加, AO3处理能将胺类物质转化。臭氧处理后的水中存在原水中没有检测出的有机物, 包括烷烃、烯烃和醛类。值得注意的是, 臭氧处理浓度越高, 检测出的质谱峰强度值越低(图 5), 因为许多大分子化合物变成小分子化合物。表 2中列出的是4批次采样中至少有3次被检测到且相似度≥80%的有机物, 还有很多复杂的小分子化合物没有列出。
|
图 5 不同浓度臭氧单独氧化处理猪场尾水的GC-MS质谱图 Figure 5 Mass chromatogram of the piggery tail water after ozonation relative to concentration of ozone CK为对照, AO1臭氧投加浓度为10 mg·L-1, AO2臭氧投加浓度为30 mg·L-1, AO3臭氧投加浓度为50 mg·L-1。 |
|
|
表 2 臭氧氧化前后猪场处理尾水中含有的特征有机物和发生变化的有机物种类 Table 2 Organic pollutants common in treated and untreated piggery tail water and new organic pollutants in treated piggery tail water |
猪场废水中含有高浓度有机物, 其中一些有机物在生物处理后依然存在, 潜在影响生态系统的健康。DOC值是反映水中有机污染物去除效果的最佳参数, 它是唯一可以表征化学过程和生物降解过程中矿化程度的参数[20]。臭氧单独氧化对DOC含量的影响不显著, 说明臭氧单独氧化不能使有机物完全被矿化, 这与CARBAJO等[21]的研究结果相似。研究发现, 沉水植物对有机物的去除效果不显著[22], 笔者试验中臭氧氧化-苦草处理使DOC含量下降, 可能是因为整个系统中的有机物并没有去除, 只是发生了转化, 从而对水的矿化度造成影响。
UV254表征废水中254 nm处具有C=C、C=O双键的一类不饱和有机物和芳香族化合物的含量, 如酚类、多环芳烃、芳香酮和芳香醛等; 腐殖酸占水体总有机物的50%~90%, 用UV436表征水中腐殖质含量。猪场尾水的UV254和UV436随着臭氧投加浓度的增加呈降低趋势, 这与KIM等[23]的研究结果一致, 说明臭氧氧化可有效降解开放的芳香环和腐殖质[24]。臭氧氧化-苦草处理使UV254和UV436进一步降低, 说明臭氧氧化-苦草处理可以提高芳香族化合物和腐殖质的降解效率。
研究表明, 植物主要通过3种机理去除环境中的有机物, 包括植物直接吸收、植物根系释放分泌物和酶以及植物和根际微生物的联合作用[25]。苦草处理可降低水中UV254和UV436, 但臭氧氧化后降低幅度更大, 且AO2处理的去除效率最高, 说明臭氧氧化的前处理能构造有利于沉水植物吸收或微生物降解有机物的环境, 对水体自净能力的提高具有促进作用。
当废水中TOC/UV254比值大于30时适用于生化处理[26]。因此,DOC/UV254比值可作为可生化性的评价指标。不同浓度臭氧单独氧化和臭氧氧化-苦草处理均增加了猪场尾水的DOC/UV254比值, 说明臭氧氧化能提高畜禽养殖废水的可生化性[27]。
臭氧分子和不同有机物的反应速率差距很大, 许多常见的水污染物具有较低的直接氧化速率常数[28], 通常臭氧不能将有机物完全分解为CO2和H2O。在很多情况下, 有机物可以转化为极性更强、分子量更小的代谢物。形成的化合物往往不能进一步与臭氧反应, 即形成了最终产物。利用GC-MS对半挥发性有机物进行定性分析, 发现猪场尾水中有机物成分组成复杂, 且臭氧氧化后有机物数量并没有明显减少, 说明有机物可能没有被降解, 只是发生了转化[29]。从臭氧氧化前后都含有的有机物种类可以看出, 直链或小分子有机物不能都被臭氧完全降解, 如酸类、醇类等。从分类中可以看出, 水中含有饱和链中羟基和氨基基团丰富的物质, 它们是已知的自由基清除剂[30]。此外, 臭氧浓度、反应时间、水体本身污染物的化学性质和水质组成都会影响氧化程度[31], 这些都可能是造成臭氧氧化后有机物矿化不完全的原因。臭氧可以与不饱和位点反应, 生成新的有机物[32]。臭氧氧化后特征有机物数量有减少趋势, 但也有新物质的生成, 可能是臭氧使有机物的长链分子部分断裂,大分子物质变成了小分子物质[30]。在臭氧氧化前后有机物数量发生变化的种类中, 烷烃数量增加, 说明长链烷烃可能被氧化成为支链较短的烷烃; 胺类物质多数具有高毒性, 高浓度臭氧可将其转化。经AO1处理后酯类物质数量增加, 可能是因为生成了氧化不完全的中间产物。结果表明, 虽然臭氧氧化不能将有机物完全矿化, 但分子形态的改变使其易于被微生物分解, 水体经臭氧氧化后排入环境中, 可以有效缩短有机污染物的存留时间。
4 结论臭氧单独氧化对猪场处理尾水中DOC含量的影响差异不显著, 臭氧氧化-苦草显著降低了DOC含量, AO1、AO2和AO3处理分别降低8.5%、17.6%和13.8%。臭氧单独氧化和臭氧氧化-苦草处理显著降低了猪场尾水中的UV254和UV436, 增加了DOC/UV254比值。苦草处理使AO2处理中的有机物含量降低幅度最大, 对DOC、UV254和UV436去除率达10.5%、15.9%和16.9%。臭氧氧化可以使猪场处理尾水中半挥发性有机物的分子形态发生变化, 使大分子变为小分子, 从而减轻了尾水排放后对自然水体的冲击, 提高了污染物的自然降解能力。
| [1] |
MACAULEY J J, QIANG Z, ADAMS C D, et al. Disinfection of Swine Wastewater Using Chlorine, Ultraviolet Light and Ozone[J]. Water Research, 2006, 40(10): 2017-2026. DOI:10.1016/j.watres.2006.03.021 (  0) 0) |
| [2] |
WANG H, XIONG H, HUI Z, et al. Mixotrophic Cultivation of Chlorella Pyrenoidosa With Diluted Primary Piggery Wastewater to Produce Lipids[J]. Bioresource Technology, 2012, 104(1): 215-220. (  0) 0) |
| [3] |
VANOTTI M B, SZOGI A A, HUNT P G, et al. Development of Environment Entally Superior Treatment System to Replace Anaerobic Swine Lagoons in the USA[J]. Bioresource Technology, 2007, 98(17): 3184-3194. DOI:10.1016/j.biortech.2006.07.009 (  0) 0) |
| [4] |
ADAMS R H, OLAIN-CASTRO D, GUZMIN-OSORÍO F J, et al. Relationship Between Geomorphology and Contamination With Weathered Hydrocarbons in an Old River Levee/Marsh Association[J]. International Journal of Environmental Science & Technology, 2009, 6(4): 527-538. (  0) 0) |
| [5] |
OLGUIN E J, GALICIA S, MERCADO G, et al. Annual Productivity of Spirulina(Arthrospira) and Nutrient Removal in a Pig Wastewater Recycling Process Under Tropical Conditions[J]. Journal of Applied Phycology, 2003, 15(2/3): 249-257. DOI:10.1023/A:1023856702544 (  0) 0) |
| [6] |
吴娜伟, 孔源, 陈颖, 等. 我国畜禽养殖项目环境影响评价制度分析[J]. 生态与农村环境学报, 2016, 32(2): 342-344. WU Na-wei, KONG Yuan, CHEN Ying, et al. Analysis of the Environmental Impact Assessment System for Livestock and Poultry Breeding Projects in China[J]. Journal of Ecology and Rural Environment, 2016, 32(2): 342-344. (  0) 0) |
| [7] |
TAMBOSI J L, DE SENA R F, GEBHARDT W, et al. Physicochemical and Advanced Oxidation Process:A Comparison of Elimination Results of Antibiotic Compounds Following an MBR Treatment[J]. Ozone:Science & Engineering, 2009, 31(6): 428-435. (  0) 0) |
| [8] |
SILVA G H R, DANIEL L A, BRUNING H, et al. Anaerobic Effluent Disinfection Using Ozone:Byproducts Formation[J]. Bioresource Technology, 2010, 101(18): 6981-6986. DOI:10.1016/j.biortech.2010.04.022 (  0) 0) |
| [9] |
TRIPATHI S, PATHAK V, TRIPATHI D M, et al. Application of Ozone Based Treatments of Secondary Effluents in the Tropical Cities[J]. Bioresource Technology, 2011, 102(3): 2481-2486. DOI:10.1016/j.biortech.2010.11.028 (  0) 0) |
| [10] |
KIM I, TANAKA H. Use of Ozone-Based Processes for the Removal of Pharmaceuticals Detected in a Wastewater Treatment Plant[J]. Water Environmental Research, 2010, 82(4): 294-301. DOI:10.2175/106143009X12487095236630 (  0) 0) |
| [11] |
RATPUKDI T, SIRIPATTANAKUL S, KHAN E. Mineralization and Biodegradability Enhancement of Natural Organic Matter by Ozone-VUV in Comparison With Ozone, VUV, Ozone-UV, and UV:Effects of pH and Ozone Dose[J]. Water Research, 2010, 44(11): 3531-3543. DOI:10.1016/j.watres.2010.03.034 (  0) 0) |
| [12] |
HOLLENDER J, ZIMMERMANN S G, KOEPKE S, et al. Elimination of Organic Micropollutants in a Municipal Wastewater Treatment Plant Upgraded With a Full-Scale Post-Ozonation Followed by Sand Filtration[J]. Environmental Science & Technology, 2009, 43(20): 7862-7869. (  0) 0) |
| [13] |
汤传栋, 张宇峰, 王伟民, 等. 水力空化辅助臭氧氧化去除水产养殖水体中叶绿素a[J]. 生态与农村环境学报, 2014, 30(4): 505-508. TANG Chuan-dong, ZHANG Yu-feng, WANG Wei-min, et al. Removal of Chlorophyll-a From Aquaculture Water With Hydrodynamic Cavitation-Assisted Ozonation Method[J]. Journal of Ecology and Rural Environment, 2014, 30(4): 505-508. (  0) 0) |
| [14] |
GAN K, MOU X, XU Y, et al. Application of Ozonated Piggery Wastewater for Cultivation of Oil-Rich Chlorella Pyrenoidosa[J]. Bioresource Technology, 2014, 171: 285-290. DOI:10.1016/j.biortech.2014.08.105 (  0) 0) |
| [15] |
MCGIVNEY W, KAWAMURA S. Cost Estimating Manual for Water Treatment Facilities[M]. Hoboken, USA: John Wiley & Sons, 2008, 37.
(  0) 0) |
| [16] |
WANG C, ZHANG S H, WANG P F, et al. Metabolic Adaptations to Ammonia-Induced Oxidative Stress in Leaves of the Submerged Macrophyte Vallisneria natans(Lour.) Hara[J]. Aquatic Toxicology, 2008, 87(2): 88-98. DOI:10.1016/j.aquatox.2008.01.009 (  0) 0) |
| [17] |
HAUXWELL J, FRAZER T K, OSENBERG C W. An Annual Cycle of Biomass and Productivity of Vallisneria americana in a Subtropical Spring-Fed Estuary[J]. Aquatic Botany, 2007, 87(1): 61-68. DOI:10.1016/j.aquabot.2007.03.003 (  0) 0) |
| [18] |
JIANG J, GU X, SONG R, et al. Microcystin-LR Induced Oxidative Stress and Ultrastructural Alterations in Mesophyll Cells of Submerged Macrophyte Vallisneria natans(Lour.) Hara[J]. Journal of Hazardous Materials, 2011, 190(1): 188-196. (  0) 0) |
| [19] |
魏复盛. 水和废水监测分析方法[M]. 北京: 中国环境科学出版社, 2002, 84-524. WEI Fu-sheng. Methods for the Monitoring and Analysis of Water and Wastewater[M]. Beijing: Environmental Science Press, 2002, 84-524. (  0) 0) |
| [20] |
GOTTSCHALK C, LIBRA J A, SAUPE A. Ozonation of Water and Wastewater:A Practical Guide to Understanding Ozone and Its Application[J]. International Journal of Environmental Studies, 2000(5): 795-796. (  0) 0) |
| [21] |
CARBAJO J B, PETRE A L, ROSAL R, et al. Continuous Ozonation Treatment of Ofloxacin:Transformation Products, Water Matrix Effect and Aquatic Toxicity[J]. Journal of Hazardous Materials, 2015, 292: 34-43. DOI:10.1016/j.jhazmat.2015.02.075 (  0) 0) |
| [22] |
王丽卿, 李燕, 张瑞雷. 6种沉水植物系统对淀山湖水质净化效果的研究[J]. 农业环境科学学报, 2008, 27(3): 1134-1139. WANG Li-qing, LI Yan, ZHANG Rui-lei. The Purification of Lake Dianshan Water Quality With Six Species of Submerged Macrophyte Systems[J]. Journal of Agro-Environment Science, 2008, 27(3): 1134-1139. (  0) 0) |
| [23] |
KIM H C, CHOI W J, MAENG S K, et al. Ozonation of Piggery Wastewater for Enhanced Removal of Contaminants by S.Quadricauda and the Impact on Organic Characteristics[J]. Bioresource Technology, 2014, 159(5): 128-135. (  0) 0) |
| [24] |
PUNZI M, NILSSON F, ANBARASAN A, et al. Combined Anaerobic-Ozonation Process for Treatment of Textile Wastewater:Removal of Acute Toxicity and Mutagenicity[J]. Journal of Hazardous Materials, 2015, 292(5): 52-60. (  0) 0) |
| [25] |
RAMASWAMI A, RUBIN E, BONOLA S. Non-Significance of Rhizosphere Degradation During Phytoremediation of MTBE[J]. International Journal of Phytoremediation, 2003, 5(4): 315-331. (  0) 0) |
| [26] |
TAMBO N, KAMEI K. Treatability Evaluation of General Organic Matter Matrix Conception and Its Application for a Regional Water and Wastewater System[J]. Water Research, 1978, 12(11): 931-950. DOI:10.1016/0043-1354(78)90077-5 (  0) 0) |
| [27] |
HSU Y C, YANG H C, CHEN J H. The Enhancement of the Biodegradability of Phenolic Solution Using Preozonation Based on High Ozone Utilization[J]. Chemosphere, 2004, 56(2): 149-158. DOI:10.1016/j.chemosphere.2004.02.011 (  0) 0) |
| [28] |
HOIGNÉ J, BADE H, HAAG W R, et al. Rate Constants of Reactions of Ozone With Organic and Inorganic Compounds in Water Ⅲ:Inorganic Compounds and Radicals[J]. Water Research, 1985, 19(18): 993-1004. (  0) 0) |
| [29] |
潘松青, 张召基, 陈少华. 臭氧氧化法深度处理养猪废水研究[J]. 安全与环境学报, 2014, 14(6): 153-157. PAN Song-qing, ZHANG Zhao-ji, CHEN Shao-hua. On the Advanced Treatment of Swine Sewage Via Ozonation Process[J]. Journal of Safety and Environment, 2014, 14(6): 153-157. (  0) 0) |
| [30] |
NÖTHE T, FAHLENKAMP H, SONNTAG C. Ozonation of Wastewater:Rate of Ozone Consumption and Hydroxyl Radical Yield[J]. Environmental Science & Technology, 2009, 43(15): 5990-5995. (  0) 0) |
| [31] |
KATSOYIANNISI A, CANONICA S, VON GUNTEN U. Efficiency and Energy Requirements for the Transformation of Organic Micropollutants by Ozone, O3/H2O2 and UV/H2O2[J]. Water Research, 2011, 45(13): 3811-3822. DOI:10.1016/j.watres.2011.04.038 (  0) 0) |
| [32] |
TAY K S, MADEHI N. Ozonation of Ofloxacin in Water:By-Products, Degradation Pathway and Ecotoxicity Assessment[J]. Science of the Total Environment, 2015, 520: 23-31. DOI:10.1016/j.scitotenv.2015.03.033 (  0) 0) |




