2. 华晋焦煤有限责任公司, 吕梁 033000
2. Huajin Coking Coal Co., Ltd., Lyuliang 033000, China
催化燃烧由于具有热效率高、燃烧温度低[1]、NOx排放水平低等优点受到了广泛关注[2-3]。相比于传统的扩散火焰燃烧,催化燃烧是气体燃料在催化剂作用下发生的无焰燃烧,避免了可见光能量消耗,使得催化燃烧的热效率更高;同时催化剂的存在降低了燃烧温度[4],抑制了NOx的生成[5]。以往的实验研究工作[6-9]表明,催化燃烧和NOx排放特性受载体孔隙率、比表面积以及空气过剩系数和气速等因素的共同影响,也与反应器的几何尺寸有关,但实验方法仅对反应器出口的NOx浓度进行测量,难以探明反应器内部NOx的生成及转换过程。数值模拟方法利用数学模型研究催化燃烧的全过程,又可探究反应器内部的NOx生成机理,因此受到越来越多的关注。Moallemi等[10]使用零维的全混流燃烧模型研究了催化燃烧反应器的出口温度。邢丹等[11]使用一维数值模型研究了催化反应器轴向上温度与反应物浓度随燃料质量流率的变化。一维模拟由于无法考虑反应器径向的速度、温度和组分浓度的差异,尤其是无法考虑催化壁面的边界层速度发展对孔道内传热传质的影响,会使计算结果与实际情况有较大出入。Yan等[12]使用二维模型对反应器孔道内部的流动、传质、传热和反应过程进行数值模拟,研究了气速和壁面材料对孔道内流场、温度场和浓度场的影响;但其仅采用表面催化反应机理,忽略了孔道内的气相反应与表面反应的相互影响[13],且未对反应器的NOx排放进行研究。
针对以往研究中存在的问题,本文建立了较完整的数学模型用于研究二维反应器的催化燃烧特性与NOx生成机理。本文以二维孔道内的甲烷/空气预混催化燃烧为研究对象,系统分析了不同气体浓度及反应器孔径对催化反应器内流场与NOx排放量的影响。本文的数学模型中不仅使用了详细的催化燃烧机理模型,也包含了完整的机理模型以描述气体燃烧,并将表面催化反应和气相反应进行耦合。
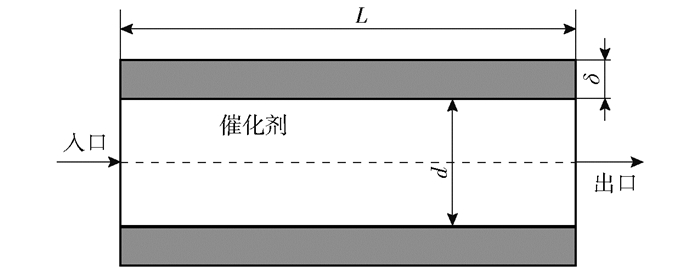
1 物理与计算模型 1.1 物理模型和边界条件本文所模拟的蜂窝型整体催化反应器由大量内壁面涂覆有Pt催化剂的细长孔道结构组成,具有结构简单、压降低等优点。由于孔道的结构、内部流动和反应均相同,因此选择单个孔道作为模拟对象来代表整体反应器的特性。单孔道的结构模型如图 1所示。孔道长度10 mm,孔道外壁的固体基体厚度0.4 mm,密度1 680 kg/m3,比热容1 020 J/(kg·K),热导率1.46 W/(m·K)。由于反应器体积大且向外界散热少,各孔道之间无传热,因此将孔道外壁面简化为绝热壁面。孔道内壁面上Pt催化剂的负载率为2.72×10-5 mol/m2,孔道内壁面为导热壁面,满足孔道内气体与固体基体之间的热量交换。在本文的研究中,反应器入口的进气温度为300 K,气速为0.5 m/s,均为定值。在甲烷浓度过低时,NOx的排放量很低可以忽略,当甲烷体积分数超过9.5%时,根据甲烷燃烧的化学方程式,甲烷-空气混合物中的氧气浓度低于甲烷完全燃烧所需的氧气浓度,使得甲烷燃烧不完全,因此选择甲烷体积分数范围为4%~9%。
|
图 1 单孔道结构模型 Fig.1 Schematic of the single channel model |
本文采用二维轴对称模型。孔道内的气体流速低且孔道内径小,最大雷诺数 =55,因此采用层流流动模型。组分求解采用有限速率组分输运模型。反应在高温、常压下进行,使用理想气体模型。本文不考虑体积力、耗散作用及辐射。描述上述物理模型的控制方程有
连续方程
| $ \frac{\partial }{\partial {{x}_{j}}}\left( \rho {{u}_{j}} \right)=0$ | (1) |
动量方程
| $ \frac{\partial }{\partial {{x}_{j}}}\left( \rho {{u}_{j}}{{u}_{i}} \right)=\frac{\partial p}{\partial {{x}_{i}}}+\frac{\partial }{\partial {{x}_{j}}}\left[ \mu \left( \frac{\partial {{u}_{i}}}{\partial {{x}_{j}}}+\frac{\partial {{u}_{j}}}{\partial {{x}_{i}}} \right) \right] $ | (2) |
能量方程
| $ \begin{align} & \rho h\frac{\partial {{u}_{i}}}{\partial {{x}_{j}}}=\frac{\partial }{\partial {{x}_{j}}}\left( \lambda \frac{\partial T}{\partial {{x}_{j}}} \right)+\frac{\partial }{\partial {{x}_{j}}}\left( \lambda \sum\limits_{s=1}^{{{N}_{\text{g}}}}{{{h}_{s}}{{D}_{j, m}}\rho \frac{\partial {{Y}_{s}}}{\partial {{x}_{j}}}} \right)+ \\ & q \\ \end{align} $ | (3) |
式中,xi,xj为i,j坐标轴方向;ρ为密度,kg/m3;ui,uj为i,j方向的速度,m/s;μ为气体动力黏度,Pa/s;h为物质的反应焓变,kJ/mol;hs为物质s的反应焓,kJ/mol;λ为导热系数,W/(m·K);T为温度,K;Ng为气相的组分数;Dj, m为物质j的扩散系数,m2/s;Ys为物质s的体积分数;q为反应的热效应,kJ。其中
在催化壁面上
| $ q=\sum\limits_{s={{N}_{\text{g}}}}^{{{N}_{\text{g}}}+{{N}_{\text{S}}}}{h_{s}^{0}{{R}_{s}}{{M}_{s}}}$ | (4) |
式中,NS为固相的组分数;Hs0为组分s的标准摩尔生成焓,kJ/mol;Rs为组分s的生成或消耗速率,mol/(m3·s);Ms为组分s的摩尔质量,g/mol。
组分方程
| $ \rho {{u}_{j}}\frac{\partial {{Y}_{s}}}{\partial {{x}_{j}}}=-\frac{\partial }{\partial {{x}_{j}}}\left( {{D}_{j, m}}\rho \frac{\partial {{Y}_{s}}}{\partial {{x}_{j}}} \right)+{{R}_{s}} $ | (5) |
在催化壁面上Rs满足
| $ {{R}_{s}}{{M}_{s}}=-{{D}_{j, m}}\rho \left( \frac{\partial {{Y}_{s}}}{\partial n} \right)+{{Y}_{s, w}}{{\rho }_{w}}{{u}_{n}} $ | (6) |
式中,un为壁面处垂直壁面的Stefan流速度分量,其中
| $ {{R}_{s}}=\sum\limits_{k=1}^{{{K}_{s}}}{{{V}_{rs}}{{k}_{r}}\prod\limits_{j=1}^{{{N}_{\text{g}}}+{{N}_{\text{S}}}}{{{\left[ {{c}_{j}} \right]}^{{{V}_{jr}}\mathit{'}}}}}$ | (7) |
式中,cj为组分j的浓度;Ks为表面基元反应的数量;Ng+NS为总组分数;Vrs和Vjr′为化学计量系数;kr为第r个反应的反应速率常数,且有
| $ {{k}_{r}}={{A}_{r}}{{T}^{{{\beta }_{r}}}}\exp \left( -\frac{{{E}_{\text{a},r}}}{RT} \right)\prod\limits_{s=1}^{{{N}_{s}}}{\theta _{s}^{\mu }\exp }\left( \frac{{{\varepsilon }_{r,s}}{{\theta }_{s}}}{RT} \right)$ | (8) |
式中,Ar为反应r的指前因子;βr为反应的温度系数;Ea,r为反应活化能,kJ/mol;θs为组分s的表面覆盖率; εr, s为覆盖参数。
理想气体状态方程
| $ p=\rho RT\sum{\frac{{{Y}_{s}}}{{{M}_{s}}}} $ | (9) |
表面反应采用Deutschmann等[14]提出的甲烷在Pt表面上的催化反应机理,该机理包含7个吸附反应,11个表面反应,以及5个解吸附反应。气相反应采用包括氮氧化物形成和再燃的甲烷燃烧反应机理GRI 3.0[15],它包含53种组分、325个基元反应。该气相反应与表面反应机理的耦合很好地描述了甲烷的催化燃烧过程[16]。使用计算流体力学商用软件Fluent17.2对二维轴对称模型进行计算,使用SIMPLE算法耦合计算压力与速度,使用二阶迎风格式对动量及各组分进行求解。
2 数值模拟结果与分析 2.1 模型验证为验证本文数值模拟方法的准确性,首先对文献[17]的相关实验研究进行数值模拟,并与实验结果进行对比。计算条件按照文献[17]的实验条件进行设置。
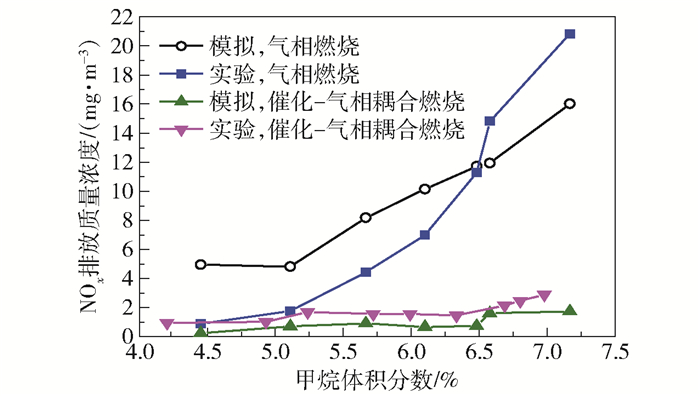
图 2为不同入口甲烷浓度条件下,气相燃烧和催化-气相耦合燃烧时NOx的出口浓度。对于无催化剂涂覆的气相燃烧,甲烷体积分数从4.4%升高至6.9%的过程中,模拟结果与实验结果差距逐渐缩小,在甲烷体积分数为6.9%时,模拟结果与实验结果相同;随着甲烷体积分数增加至7.6%,模拟结果与实验结果差距增大,但最大差距仅为4 mg/m3。以上结果表明该气相反应机理用于甲烷的气相燃烧是可靠的。催化-气相耦合燃烧的数值模拟结果略低于实验结果,最大差距为0.6 mg/m3,这是由实验所使用的催化剂涂覆不均匀,与模拟的理想情况有差异造成的。通过对上述模拟结果与实验结果的比较及分析,可以认为模拟结果和实际情况相符,本文所使用的催化-气相耦合燃烧数值模型是准确可靠的。
|
图 2 实验值与模拟结果的对比 Fig.2 Comparison of experimental values and simulated results |
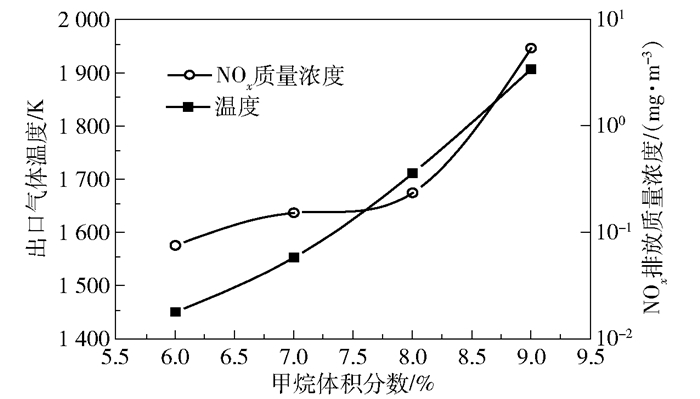
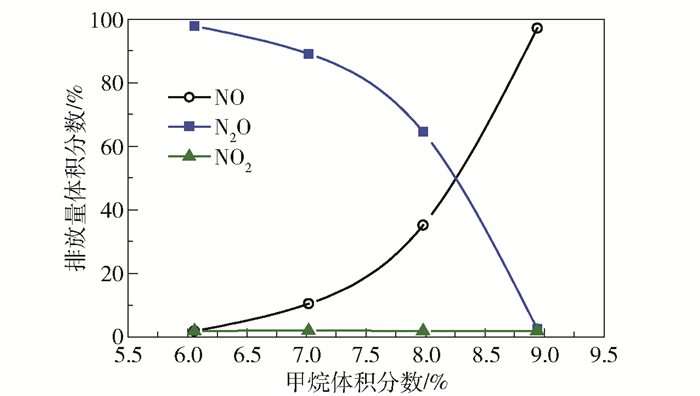
采用催化-气相耦合燃烧数值模型对不同入口甲烷浓度进行研究。图 3为孔道出口温度和NOx浓度随入口甲烷浓度增加的变化曲线。从图中可以看出,随着甲烷浓度的增加,出口温度由1 450 K逐渐升高至1 900 K。甲烷体积分数从6%升高至8%时,NOx排放量由0.08 mg/m3缓慢增加至0.22 mg/m3;当甲烷体积分数达到9%时,NOx排放量迅速上升至5.2 mg/m3。图 4表示不同甲烷浓度下,孔道出口处3种污染物(NO、N2O、NO2)排放量占总NOx排放量体积分数的变化情况。甲烷体积分数从8%升至9%时,NO排放量所占比例从35%迅速升高至99%,这是因为在9%的甲烷体积分数下,出口温度超过1 800 K,此时孔道内生成大量的热力型NO[18],导致NO比例和NOx浓度的大幅度上升。
|
图 3 不同甲烷浓度下出口温度与NOx浓度的变化 Fig.3 Temperature and NOx emissions with different methane concentrations at the outlet |
|
图 4 不同甲烷浓度下出口处3种NOx比例的变化 Fig.4 Proportion of three nitrogen oxides with different methane concentrations at the outlet |
在本文的操作条件下,入口甲烷体积分数为9%时NOx的排放质量浓度远低于30 mg/m3的排放标准。
2.3 孔道直径的影响孔道直径是影响反应器性能的重要参数。相比于一维模拟仅能获得反应器的轴向数据而无法模拟径向上参数变化的情况,本文所使用的二维数值模拟考虑了反应器径向上的温度分布和速度分布对燃烧和排放特性的影响。本文对孔道长度10 mm,壁厚0.4 mm,内径分别为0.5 mm、0.8 mm、1.1 mm、1.4 mm、1.7 mm的燃烧器进行催化-气相耦合燃烧二维模拟研究。
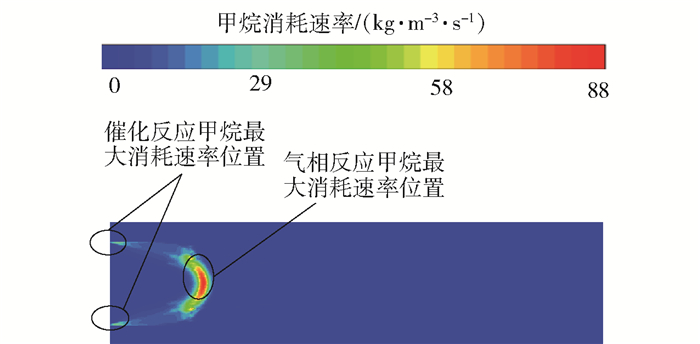
2.3.1 孔道直径对甲烷消耗速率和甲烷浓度分布的影响图 5表示孔道直径为1.7 mm时,反应器内的甲烷消耗速率分布情况。可以看到,在孔道壁面上,入口壁面处的甲烷消耗速率最大。这是因为甲烷在壁面上发生催化燃烧,入口处甲烷浓度最高,催化反应速率最大,之后随着甲烷的消耗,催化反应速率逐渐变小,因此在整个壁面上孔道入口处催化反应的甲烷消耗速率最大。在孔道中,甲烷最大消耗速率的位置在孔道中轴线上的甲烷峰面上,这是因为气相反应主要发生在甲烷峰面上,催化反应抑制气相反应的发生,距离壁面越远,催化反应对气相反应的抑制作用越小,气相反应速率越大,因此在孔道中轴线的甲烷峰面上气相反应的甲烷消耗速率最大。
|
图 5 甲烷的消耗速率分布 Fig.5 The distribution of methane consumption rate |
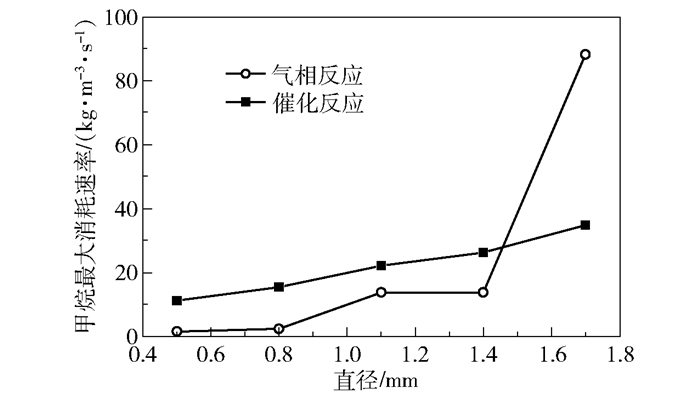
图 6表示孔道中发生的气相反应和壁面上发生的催化反应中甲烷最大消耗速率随孔径的变化情况。可以看出,随着孔径的增加,气相反应和催化反应中甲烷的最大消耗速率均增加。当孔道直径小于1.4 mm时,由于壁面对气相反应的抑制,催化反应甲烷最大消耗速率均大于气相反应。当孔道直径为1.7 mm时,气相反应中的甲烷最大消耗速率与孔径为1.4 mm时相比,由17 kg/(m3·s)迅速增加至88 kg/(m3·s),而催化反应的甲烷最大消耗速率为34 kg/(m3·s),远低于气相反应。
|
图 6 不同孔径下的甲烷最大消耗速率 Fig.6 Maximum consumption rate of methane for different pore sizes |
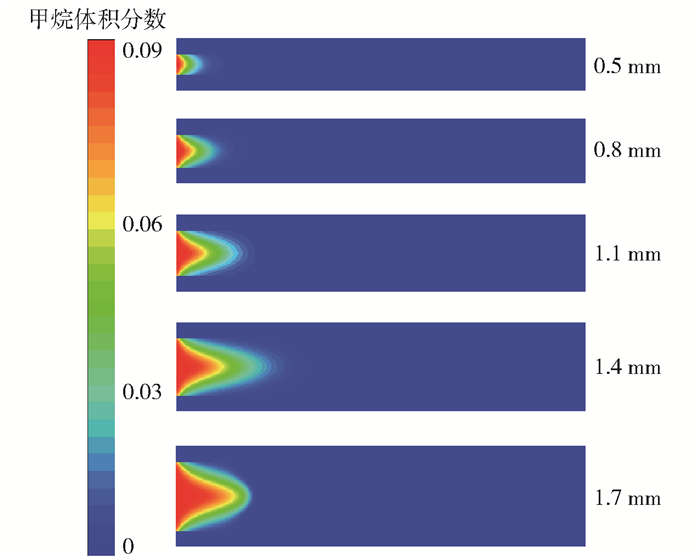
图 7为反应器中的甲烷浓度分布。在径向上,距离壁面位置越远,甲烷浓度越高,这是因为相比于中轴线处,壁面处的甲烷更容易参与催化反应,所以中轴线上的甲烷浓度较高。在轴向上,随着反应器孔径从0.5 mm增加至1.4 mm,甲烷完全反应所需的长度从1.2 mm增加至3.4 mm,当孔径为1.7 mm时,所需长度反而缩短至2.1 mm。孔径从0.5 mm增加至1.4 mm时,虽然甲烷最大消耗速率有所提高,但是随着孔径的增大,进入孔道的燃料量的增长幅度大于甲烷最大消耗速率的增长幅度,因此需要更长的轴向距离使甲烷完全反应。当孔径为1.7 mm时,气相反应的甲烷最大消耗速率是孔径为1.4 mm时的5.2倍,因此甲烷完全转化所需要的轴向长度比孔径为1.4 mm时有所缩短。
|
图 7 不同孔径下的甲烷浓度分布 Fig.7 Distribution of methane concentration for different pore diameters |
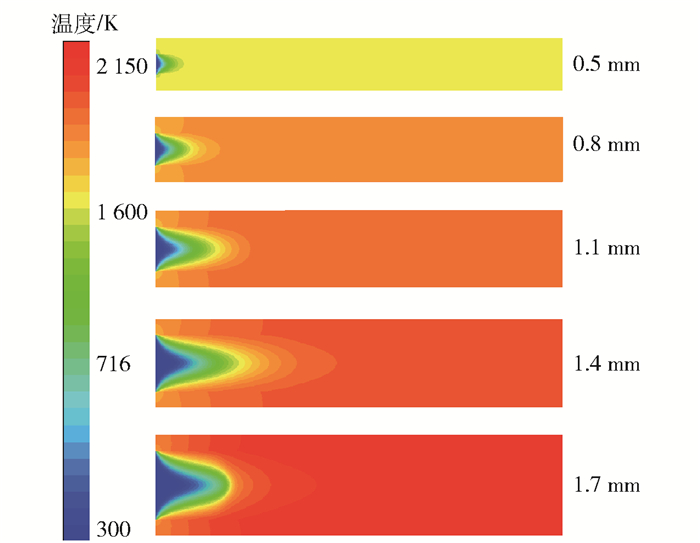
图 8为反应器内的温度分布。随着孔径的增大,进入孔道的燃料量增加,反应器出口温度从1 593 K升高至2 106 K。在轴向上,孔径从0.5 mm增加至1.4 mm时,气体达到最高温度所需的长度从0.6 mm增加至4.6 mm,当孔径为1.7 mm时,所需长度缩短至3.9 mm。这是因为甲烷的反应导致孔道内温度升高,因此孔道内的温度分布与甲烷浓度分布相似,气体达到最高温度所需长度与甲烷完全反应所需长度的变化趋势也相同。
|
图 8 不同孔径下的温度分布 Fig.8 Temperature distribution of reactors with different pore sizes |
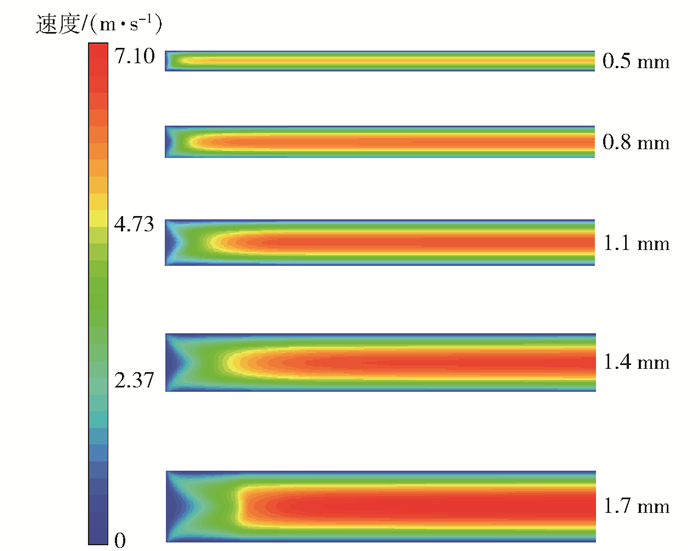
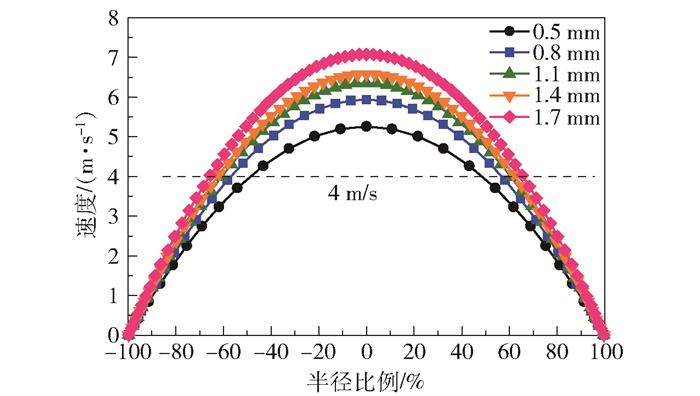
图 9为孔道内的流速分布情况。随着孔径的增大,反应器内最大流速从5.25 m/s升高至7 m/s。因为气体速度与温度呈正比,所以气体达到最大速度所需长度与达到最高温度所需长度的变化趋势相同。孔径从0.5 mm增加至1.4 mm时,气体达到最大速度所需长度从0.8 mm增加至4.5 mm,而在孔径为1.7 mm时所需长度减少至2.9 mm。孔径不仅对轴向上的流速分布产生影响,也影响了径向流速分布。图 10为反应器出口处的径向流速分布,可以看出,随着孔径的增大,高速区域所占的比例增加。例如孔径为0.5 mm时有47%的区域流速超过4 m/s,孔径为1.7 mm时有65%的区域流速超过4 m/s。孔径越大,孔道内部体积越大,高速区域所占比例也越大,因此孔道内高速区的体积随着孔径的增大而迅速增加。
|
图 9 不同孔径的反应器内的流速分布 Fig.9 Velocity distribution in reactors with different pore sizes |
|
图 10 不同孔径的反应器出口处径向上的流速分布 Fig.10 Velocity distribution in the radial direction at the outlet of reactors with different pore sizes |
以上对甲烷浓度、温度和流速分布的分析表明,孔径通过影响甲烷的反应来影响反应器内的温度分布,进而改变反应器内的流速分布。
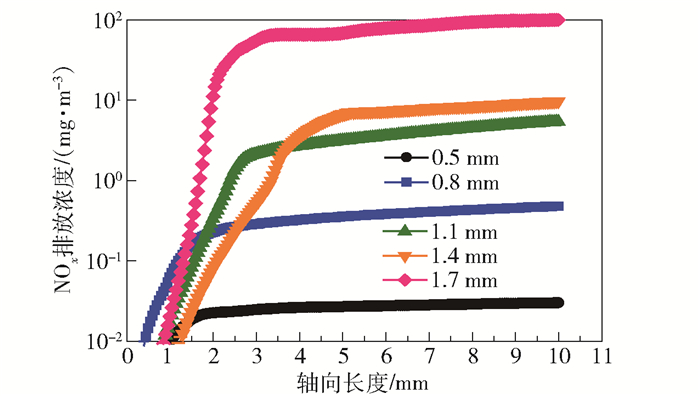
2.3.3 孔道直径对单位面积放热量和NOx排放量的影响从孔道中轴线上的NOx浓度分布(图 11)可以看出,NOx浓度沿轴向的分布规律与甲烷浓度、温度和流速的分布规律相同,孔道直径从0.5 mm增加至1.4 mm时,NOx浓度达到稳定所需的长度由1 mm增加至5 mm,当孔道直径为1.7 mm时,所需长度与1.4 mm孔径时相比缩短了2 mm。这是因为温度和流速均影响NOx的生成,温度影响热力型NOx的生成过程,流速影响燃料停留时间,因此快速型NOx的生成速率与燃料停留时间有关。孔道直径的改变影响了气相反应与表面催化反应的速率,进而影响了孔道内温度和速度的分布,从而改变了NOx的浓度分布。
|
图 11 不同孔径反应器轴线上的NOx浓度 Fig.11 NOx concentration on the axis of reactors with different pore sizes |
随孔道直径的减小,NOx排放量从100 mg/m3迅速降低至0.028 mg/m3。孔径减小对NOx排放量的影响体现在以下两方面。(1)进入反应器燃料量的减少,使孔道内温度降低,减少了热力型NOx的生成;另外温度的降低导致了流速的降低,增加了燃料的停留时间,也减少了快速型NOx的生成。(2)小孔径抑制了生成NOx的气相反应的发生:①孔径的减小有利于孔道内反应物的径向扩散,促进了表面催化反应的发生[19],而表面催化反应对气相反应有抑制作用[20];②由于壁面熄火效应,孔径越小,气相反应越难发生。因此,随着孔径的减小,出口NOx浓度迅速降低。
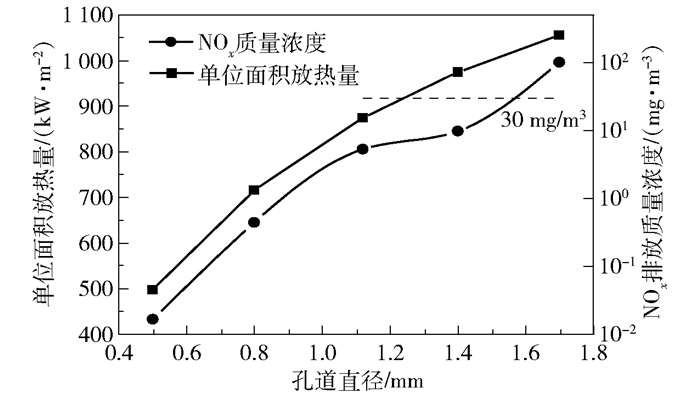
图 12为反应器的单位面积放热量和NOx排放量与孔径大小的关系。在进气速度与进气浓度相同的情况下,反应器的单位面积放热量正比于孔道截面积与反应器总截面积的比值。孔道直径从1.7 mm降至0.5 mm的过程中,由于在本文的二维模拟中孔道壁厚保持不变,孔道截面积与反应器总截面积的比值随着内径的减小而迅速减小,所以反应器单位面积放热量从1 055 kW/m2降低至500 kW/m2。
|
图 12 不同孔径反应器的单位面积放热量与NOx排放浓度 Fig.12 Heat release value per square meter and NOx emissions of reactors with different pore sizes |
当孔径为1.7 mm时,反应器的单位面积放热量最大,NOx的排放量达到100 mg/m3,远远超过最低排放标准的30 mg/m3。在孔径为1.4 mm时,反应器的单位面积放热量为974 kW/m2,比1.7 mm孔径时仅降低了81 kW/m2,但NOx排放量只有9.72 mg/m3,低于排放标准。因此在本文操作条件下,1.4 mm是最合适的反应器孔道直径。
3 结论(1) 加大甲烷浓度会改变NOx的组成成分,并使NOx排放量升高。入口甲烷体积分数从6%升高至9%,NO排放量占总NOx排放量的比例从接近0增至99%,NOx排放量升高至5.3 mg/m3。
(2) 孔径尺寸对催化燃烧过程影响较大。孔径大小影响催化反应和气相反应的反应速率,进而改变了反应器内的甲烷浓度分布、温度分布以及速度分布,最终对反应器内NOx的生成与排放量产生影响。
(3) 在本文研究的孔径范围内,催化燃烧的NOx排放量都较低。反应器单位面积发热量和NOx排放量随着反应器孔径的减小而迅速降低。最合适的反应器孔道直径为1.4 mm,在该孔径下反应器单位面积发热量为974 kW/m2,且NOx排放量低于排放标准。
| [1] |
EGUCHI K, ARAI H. Recent advances in high temperature catalytic combustion[J]. Catalysis Today, 1996, 29(1-4): 379-386. DOI:10.1016/0920-5861(95)00308-8 |
| [2] |
訾学红, 戴洪兴, 何洪. 天然气催化燃烧在燃气轮机和锅炉中的应用[J]. 工业催化, 2008, 16(6): 40-44. ZI X H, DAI H X, HE H. Application of natural gas catalytic combustion in gas turbines and boilers[J]. Industrial Catalysis, 2008, 16(6): 40-44. (in Chinese) DOI:10.3969/j.issn.1008-1143.2008.06.010 |
| [3] |
杜小春.甲烷催化燃烧的应用研究-天然气催化燃烧炉和热水器的研制[D].成都: 四川大学, 2005. DU X C. Applied studies on methane catalytic combustion-Development of a natural gas premixed catalytic burner and boiler for household applications[D]. Chengdu: Sichuan University, 2005. (in Chinese) http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y775816 |
| [4] |
LI Y X, LUO C M, LIU Z L, et al. Catalytic combustion of CH4/air mixtures over metal foam monoliths[J]. Energy Procedia, 2015, 66: 249-252. DOI:10.1016/j.egypro.2015.02.044 |
| [5] |
CERRI I, SARACCO G, SPECCHIA V. Methane combustion over low-emission catalytic foam burners[J]. Catalysis Today, 2000, 60(1/2): 21-32. |
| [6] |
LYUBOVSKYL M, KARIM H, MENACHERRY P, et al. Complete and partial catalytic oxidation of methane over substrates with enhanced transport properties[J]. Catalysis Today, 2003, 83(1-4): 183-197. DOI:10.1016/S0920-5861(03)00231-1 |
| [7] |
SPECCHIA S, CIVERA A, SARACCO G, et al. Palladium/perovskite/zirconia catalytic premixed fiber burners for efficient and clean natural gas combustion[J]. Catalysis Today, 2006, 117(4): 427-432. DOI:10.1016/j.cattod.2006.06.041 |
| [8] |
QU Z G, FENG X B. Catalytic combustion of premixed methane/air in a two-zone perovskite-based alumina pileup-pellets burner with different pellet diameters[J]. Fuel, 2015, 159: 128-140. DOI:10.1016/j.fuel.2015.06.066 |
| [9] |
FENG X B, QU Z G, GAO H B. Premixed lean methane/air combustion in a catalytic porous foam burner supported with perovskite LaMn0.4Co0.6O3 catalyst with different support materials and pore densities[J]. Fuel Processing Technology, 2016, 150: 117-125. DOI:10.1016/j.fuproc.2016.05.009 |
| [10] |
MOALLEMI F, BATLEY G, DUPONT V, et al. Chemical modelling and measurements of the catalytic combustion of CH4/air mixtures on platinum and palladium catalysts[J]. Catalysis Today, 1999, 47(1-4): 235-244. DOI:10.1016/S0920-5861(98)00304-6 |
| [11] |
邢丹, 刘明侯, 徐侃. 多孔介质催化燃烧特性的数值分析[J]. 中国科学技术大学学报, 2012, 42(1): 41-46, 59. XING D, LIU M H, XU K. Numerical study on combustion in a porous medium with Pt catalyst[J]. Journal of University of Science and Technology of China, 2012, 42(1): 41-46, 59. (in Chinese) DOI:10.3969/j.issn.0253-2778.2012.01.007 |
| [12] |
YAN Y F, HUANG W P, TANG W M, et al. Numerical study on catalytic combustion and extinction characteristics of pre-mixed methane-air in micro flatbed channel under different parameters of operation and wall[J]. Fuel, 2016, 180: 659-667. DOI:10.1016/j.fuel.2016.04.085 |
| [13] |
刘子琨, 周俊虎, 杨卫娟, 等. 甲烷微尺度燃烧中气相反应与催化反应间的相互作用[J]. 化工进展, 2017, 36(6): 2094-2100. LIU Z K, ZHOU J H, YANG W J, et al. Interactions between gas-phase reaction and catalytic reaction in methane microscale combustion[J]. Chemical Industry and Engineering Progress, 2017, 36(6): 2094-2100. (in Chinese) |
| [14] |
DEUTSCHMANN O, MAIER L I, RIEDEL U, et al. Hydrogen assisted catalytic combustion of methane on platinum[J]. Catalysis Today, 2000, 59(1/2): 141-150. |
| [15] |
SMITH G P, GOLDEN D M, FRENKLACH M, et al. GRI-Mech home page[EB/OL].[2019-01-10]. http://www.me.berkeley.edu/gri_mech/.
|
| [16] |
LI Y H, CHEN G B, HSU H W, et al. Enhancement of methane combustion in microchannels:effects of catalyst segmentation and cavities[J]. Chemical Engineering Journal, 2010, 160(2): 715-722. DOI:10.1016/j.cej.2010.03.057 |
| [17] |
许考.预混天然气催化燃烧及其传热传质特性的研究[D].北京: 北京工业大学, 2006. XU K. Study on catalytic combustion of premixed natural gas and its heat and mass transfer characteristics[D]. Beijing: Beijing University of Technology, 2006. (in Chinese) http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1164654 |
| [18] |
张笑慰, 范卫东, 李宇, 等. 天然气燃烧NOx排放特性实验研究及数值模拟[J]. 锅炉技术, 2015, 46(1): 70-74. ZHANG X W, FAN W D, LI Y, et al. Experimental and numerical investigations of the NOx emission characteristics of methane flames[J]. Boiler Technology, 2015, 46(1): 70-74. (in Chinese) DOI:10.3969/j.issn.1672-4763.2015.01.017 |
| [19] |
冉景煜, 祁文杰, 王蕊蕊. 微通道粗糙度对甲烷催化燃烧影响的数值研究[J]. 工程热物理学报, 2014, 35(6): 1244-1247. RAN J Y, QI W J, WANG R R. Numerical study of the micro-channel rough surface on methane catalytic combustion[J]. Journal of Engineering Thermophysics, 2014, 35(6): 1244-1247. (in Chinese) |
| [20] |
伍亨, 钟北京. 空间反应和入口速度对甲烷催化反应的影响[J]. 清华大学学报(自然科学版), 2005, 45(5): 670-672, 676. WU H, ZHONG B J. Influence of the gas-phase reaction and the inlet velocity on the catalytic reaction of CH4[J]. Journal of Tsinghua University (Science and Technology), 2005, 45(5): 670-672, 676. (in Chinese) DOI:10.3321/j.issn:1000-0054.2005.05.024 |








