2. 常州大学 石油化工学院 江苏省绿色催化材料与技术重点实验室, 常州 213164;
3. 北京化工大学 常州先进材料研究院, 常州 213164
2. Jiangsu Key Laboratory of Advanced Catalytic Materials and Technology, School of Petrochemical Engineering, Changzhou University, Changzhou 213164;
3. Changzhou Institute of Advanced Materials, Beijing University of Chemical Technology, Changzhou 213164, China
锂-空气电池的理论比能量密度可以高达3500W·h/kg,被认为是极具应用前景的能量储存和转换系统[1]。但是,目前锂-空气电池存在充放电效率低、循环性能差等问题[2],而研发廉价、高导电性、高催化活性和高稳定性的氧气还原反应(ORR)催化剂是提高锂-空气电池性能的重要途径。
Pt及其合金是目前性能最好的ORR电催化剂[3-4],然而这类催化剂存在价格昂贵、储量稀少、易中毒失活等问题,因此开发取代Pt的非贵金属催化剂得到了广泛的关注[5]。近年来,人们发现替代Pt的ORR非贵金属催化剂主要有3类:①Fe(或Co)/N/C型催化剂[6-7];②基于非贵金属的硫属元素化合物[8]、氮化物和氮氧化物[9-10];③碳基无金属化物[11]。在这些非贵金属催化剂中,Fe(或Co)/N/C型催化剂以其显著的ORR活性(包括催化活性和稳定性)在锂-空气电池的应用中具有很大的潜力[6-7],而另外两种催化剂因其形成的活性位点的催化活性较低及在高电化学电势下的稳定性较差,无法比拟商用Pt/C催化剂[8-11]。因此,探索和开发先进的Fe(或Co)/N/C催化剂来代替Pt催化剂对于促进锂-空气电池的大规模应用具有重要意义。金属有机骨架(metal-organic frameworks, MOFs)由于具有高比表面积、均匀的孔径分布和丰富的金属/有机物质等独特性质,被广泛用作合成Fe(或Co)/N/C型催化剂的前驱体[12-13]。在高温下热处理MOFs得到的Fe(或Co)/N/C型催化剂继承了MOFs特有的高比表面积和优异的孔隙率等特点,表面拥有致密的活性位点,如本课题组[14]用水热法合成的FeCo/N/C型双功能催化剂展现出优异的氧气还原反应和氧气析出反应催化活性;Wang等[15]通过热转换法合成的Fe/N/C型催化剂具有很高的ORR催化活性,半波电位达到0.82V(vs. RHE)。
在前人工作[16]的基础上,本文尝试了新的合成方法,采用Co和Zn的沸石咪唑酯骨架结构材料(zeolitic imidazolate frameworks, ZIFs)共同生长于氧化石墨(GO)表面合成前驱体,经过高温碳化得到Co@N-doped rGO催化剂,同时提高了作为ORR活性位点Co的占比;通过调整金属(Zn和Co)加入量和热处理温度等条件,探究了制备Co@N-doped rGO催化剂的最佳条件。
1 实验部分 1.1 实验试剂六水合硝酸钴(Co(NO3)2·6H2O)、六水合硝酸锌(Zn(NO3)2·6H2O)、2-甲基咪唑(C4H6N2),分析纯,聚乙烯吡咯烷酮(PVP),平均分子量58000,四丁基氢氧化铵溶液(C16H37NO,质量浓度约为0.25g/mL的水溶液),均购于上海阿拉丁试剂有限公司;氧化石墨(GO),SE2431W,常州第六元素材料科技股份有限公司;无水乙醇(C2H5OH),分析纯,国药集团化学试剂有限公司;Nafion溶液,5%,阿法埃莎(中国)化学有限公司;Pt/C催化剂,20%,Johnson Matthey公司;炭黑,Vulcan XC-72,卡博特公司。
1.2 催化剂的制备取一定量的氧化石墨加入去离子水中,超声5h形成均一分散液,分散液中每mL去离子水含2mg GO。取100mL的GO分散液放入250mL烧杯内,超声30min后改为磁力搅拌,然后依次加入0.01mol的2-甲基咪唑、15mL的四丁基氢氧化铵溶液和2g的聚乙烯吡咯烷酮。搅拌30min后,采用恒压漏斗滴加35mL混合硝酸盐水溶液,该混合硝酸盐水溶液含有0.002mol的六水合硝酸锌和0.003mol的六水合硝酸钴,继续室温下搅拌72h并超声1h,然后用去离子水离心洗涤3次,冷冻干燥后得到固体前驱体,记做S-1。采用与上述相同的步骤,控制GO用量和2-甲基咪唑、六水合硝酸锌、六水合硝酸钴物质的量比1:2:3不变,制备金属元素(Co和Zn)物质的量增大为原来的2倍和5倍的前驱体,相应样品分别记做S-2和S-5。
取合成的前驱体(S-n, n=1, 2, 5)置于管式炉中,在氮气气氛下以5℃/min的升温速率从室温升至所需温度,并保持该温度3h,之后在氮气气氛下自然冷却至室温,离心洗涤并干燥,得到催化剂S-n-t(t为对应温度,值为750, 850, 950)。将GO直接在氮气气氛下进行同样的热处理,得到的样品记作GO-850。
1.3 催化剂结构表征催化剂的晶相结构分析采用德国布鲁克AXS公司的D8FOCUSX型X射线衍射仪,扫描范围5° ~ 80°,步长0.02°,Cu/Kα (λ=0.154056nm)X射线,管电压40kV,电流100mA。
采用日本电子公司的JSM-6360LA型扫描电子显微镜(SEM)观察催化剂的表面形貌。
采用美国ThermFisher Scientific公司的ESCALAB 250型光电子能谱仪分析催化剂的表面化学元素。X射线源为Al-Kα,通过能30eV,所测元素的结合能用C 1s的标准结合能284.6eV进行校正。
1.4 电化学性能测试将2.5mg炭黑和2.5mg催化剂分散到含50μL的5% Nafion和1mL无水乙醇的混合溶液中,超声形成均一的分散相,然后取21μL滴在玻碳电极(直径为5mm)上,自然干燥,得到工作电极。催化剂在玻碳电极上的负载量为0.24mg/cm2。
所有电化学性能测试均在配有旋转圆盘电极(rotating disk electrode, RDE,泰州科瑞特分析仪器有限公司)的电化学工作站(CHI760E, 上海辰华仪器有限公司)上进行。采用三电极体系测试,碳棒为对电极,KCl饱和的Ag/AgCl电极为参比电极,电解液为0.1mol/L KOH。本文所有电位均根据E(vs.RHE)=E(vs. Ag/AgCl)+0.197V+0.0591 pH转换为标准氢电极。
在ORR电化学性能测试前,工作电极在N2饱和的0.1mol/L KOH电解液中以0.05V/s的扫描速率于1.15~-0.05V的电压范围内用循环伏安法[17]扫描直至曲线稳定。N2背景曲线在N2饱和的0.1mol/L KOH电解液中,以0.005V/s的扫描速率在相同电压范围内测得。催化剂的ORR线性扫描伏安曲线(linear sweep voltammetry,LSV)[17]在O2饱和的0.1mol/L KOH电解液中以0.005V/s的扫描速率测得,旋转圆盘电极速度分别为400、625、900、1225、1600、2025和2500r/min。以在O2饱和电解液中测得的电流密度与N2背景电流密度之间的差值作为催化剂的ORR电流密度。催化剂ORR活性稳定性采用计时电流法[17],以1600r/min的转速在氧气饱和的0.1mol/L KOH电解液下测试,整个过程在0.66V下持续64800s。
采用Koutecky-Levich(K-L)方程[18]来进一步研究催化剂的ORR过程,并计算不同催化剂的电子转移数n。K-L方程为
| $ \begin{array}{l}{\frac{1}{i}=\frac{1}{i_{\mathrm{k}}}+\frac{1}{i_{\mathrm{d}}}=\frac{1}{i_{\mathrm{k}}}+\frac{1}{B \omega^{1 / 2}}} \\ {B=0.62 n F c_{0_{2}} D_{0_{2}}^{2 / 3} v^{-1 / 6}}\end{array} $ |
式中,i为表观电流密度;ik为反应动力学限制电流密度;id为扩散电流密度;B为Levich常数;ω为RDE的转速,rad/s;n为总的电子转移数;F为法拉第常数(96485C/mol[18]);cO2为0.1mol/L KOH中饱和氧气浓度(1.2×10-3mol/cm3[18]);DO2为0.1mol/L KOH中O2的扩散系数(1.9×10-5cm2/s[18]);v为0.1mol/L KOH溶液的动力学黏度(0.01cm2/s[18])。
采用Tafel方程[19]对1600r/min下催化剂的ORR极化曲线进行处理,Tafel方程为
| $ \begin{aligned} \eta &=\frac{2.3 R T}{\alpha n_{\alpha} F} \lg i^{0}-\frac{2 \cdot 3 R T}{\alpha n_{\alpha} F} \lg \left|i_{\mathrm{k}}\right| \\ i_{\mathrm{k}} &=\frac{i_{\mathrm{d}} i}{i_{\mathrm{d}}-i} \end{aligned} $ |
式中,η为电压,V;i0为交换电流密度,mA/cm2;R为通用气体常数;T为温度,K;α为转移系数;nα为电子转移数。
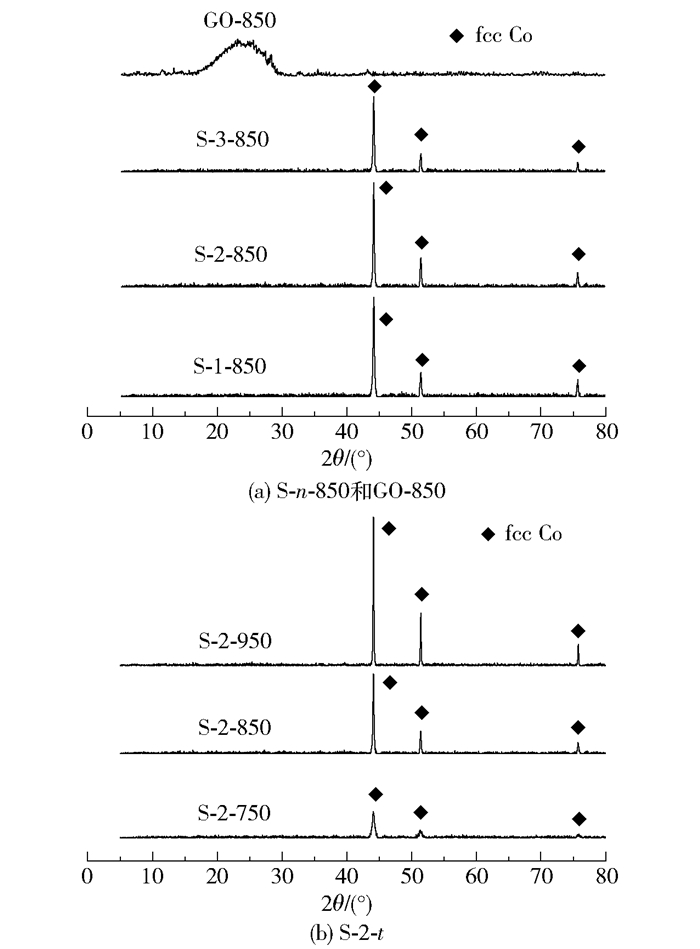
2 结果与讨论 2.1 催化剂的结构表征结果图 1 (a)是S-n-850 (n=1, 2, 5)及GO-850的XRD谱图,图 1(b)是S-2-t (t=750, 850, 950)的XRD谱图。从图 1 (a)可见,GO-850在2θ为25.12°处有一衍射峰,该峰对应石墨的(002)晶面[20]。加入不同比例GO的系列催化剂S-n-t的衍射峰特征没有明显区别,即在2θ为44.2°,51.5°和75.9°处均有明显的衍射峰,对应于面心立方(fcc)的单质Co的特征峰(JCPDS NO. 89-7093)[21]。从图 1 (b)可见,前驱体S-2经过不同温度热处理后,Co的衍射峰位置没有改变,但是衍射峰的强度有较大差别,温度越高,衍射峰越强,说明Co的结晶度随着温度的升高而增大。
|
图 1 S-n-850、GO-850及S-2-t的XRD谱图 Fig.1 XRD patterns of S-n-850, GO-850 and S-2-t |
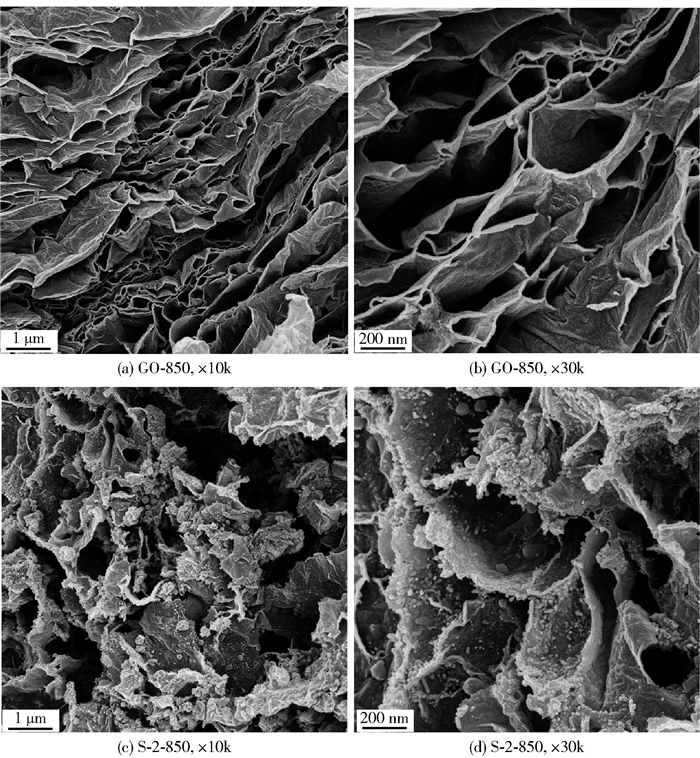
图 2(a)、(b)是GO-850的SEM图,(c)、(d)是S-2-850的SEM图。从图中可见,GO经过高温热处理后呈现层状分布[22];加入了GO的催化剂S-2-850整体结构与GO-850相似,也呈层状分布,表面有金属小颗粒团簇[23]生成,而非大颗粒的金属团聚,比表面积显著增大,活性物种充分暴露。这种结构十分有利于电子的传导,对催化剂电催化性能的提升起着至关重要的作用。
|
图 2 GO-850和S-2-850的SEM图 Fig.2 SEM images of GO-850 and S-2-850 |
初始的Zn形成Co的空间隔离,碳化过程能够抑制Co的聚集,Zn的蒸发也能增大催化剂的比表面积[24]。GO经高温碳化变成的还原氧化石墨(reduced graphene oxide, rGO)能够增强催化剂的导电性,强化电催化反应过程的电荷转移,同时还能分散Co基纳米颗粒,进一步暴露活性物种,充分发挥活性物种的催化性能[25]。
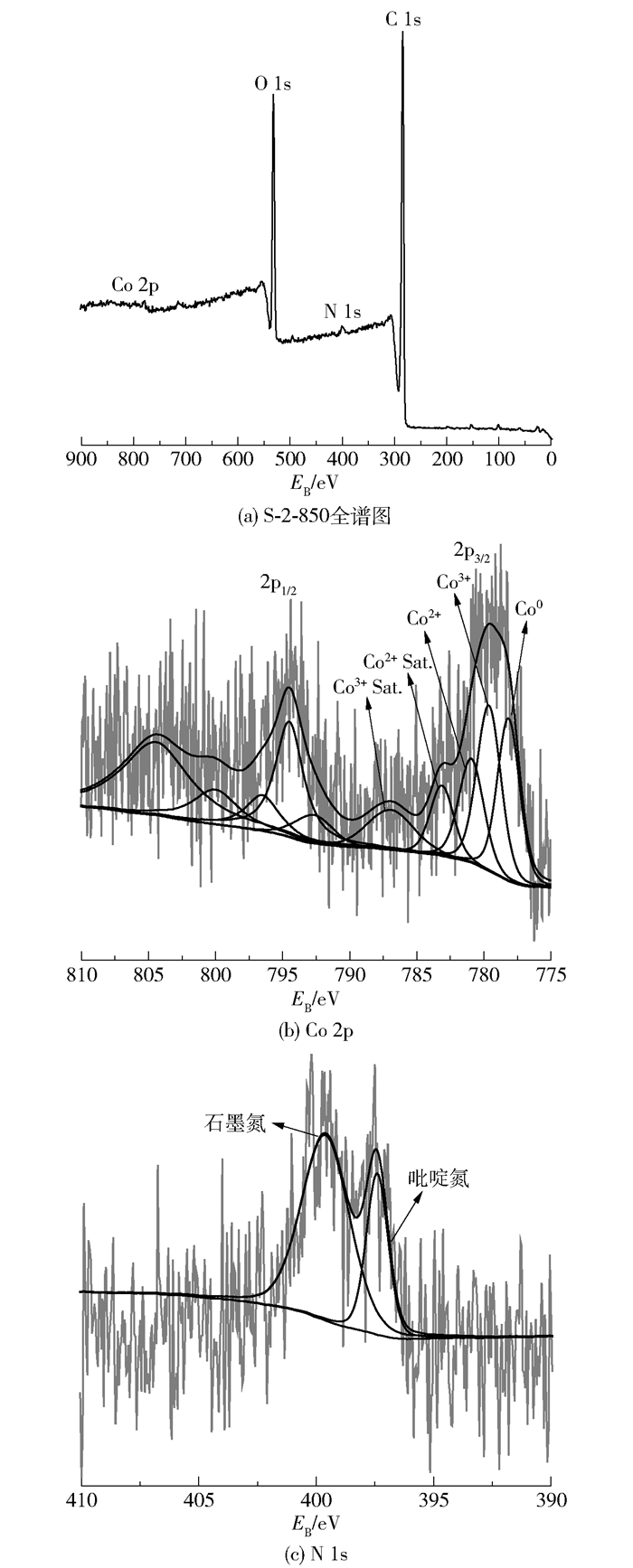
图 3给出了催化剂S-2-850的XPS全谱图及Co、N元素的高分辨能谱图。图 3(a)表明,催化剂S-2-850表面包含元素C、N、O和Co的能谱峰,元素占比分别为80.1%、1.5%、18.1%和0.3%。使用软件XPSPEAK41对高分辨Co 2p和N 1s进行拟合,得到结果如图 3(b)、(c)。对高分辨Co 2p3/2分峰后,在结合能为778.1eV、779.6eV和781.0eV处的拟合峰分别对应Co0、Co3+和Co2+,在结合能为783.2eV和786.9eV处的拟合峰分别对应Co2+和Co3+的卫星峰[26]。高分辨N 1s可拟合成2个能谱峰,结合能分别位于397.4eV和399.6eV处,对应吡啶氮和石墨氮,相对含量分别为28.6%和71.4%,这两种结构的氮通常被认为是ORR的活性位点[16]。
|
图 3 催化剂S-2-850的XPS全谱图及元素高分辨能谱图 Fig.3 XPS full and high resolution spectra of the S-2-850 catalyst |
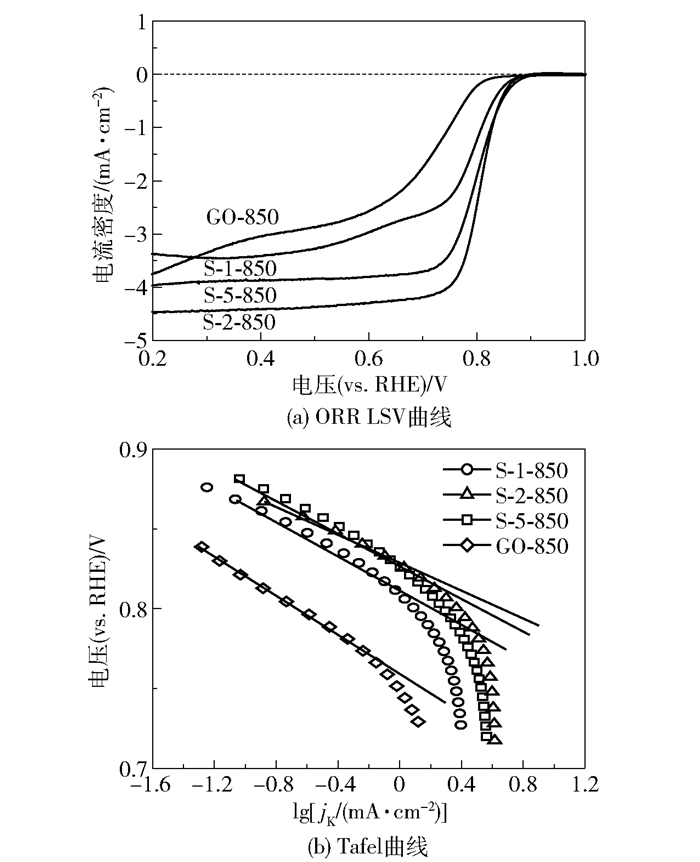
图 4 (a)是S-n-850 (n=1, 2, 5)和GO-850在旋转圆盘电极速度为1600r/min下的LSV曲线,表 1是催化剂的ORR电化学数据。从表 1可见,不同金属/GO比例的S-n-850的起始电位(电流密度达到-0.1mA/cm2时的电位, 下同)和半波电位相较于GO-850均有显著增大,其中,催化剂S-2-850的起始电位和半波电位最大(分别为0.871V和0.804V),表明S-2-850有较好的ORR催化活性。图 4 (b)是催化剂S-n-850和GO-850的ORR性能的Tafel曲线。加入不同比例GO的S-n-850的Tafel斜率均比GO-850的Tafel斜率小,说明此系列催化剂的动力学过程要比GO-850快,其中催化剂S-2-850的Tafel斜率最小,为49.6mV/dec,可知催化剂S-2-850的ORR催化反应有较快的动力学过程。
|
图 4 不同催化剂在1600r/min下的ORR LSV曲线和Tafel曲线 Fig.4 ORR LSV curves and Tafel curves of the catalysts at an electrode rotation rate of 1600r/min |
| 下载CSV 表 1 S-n-850(n=1, 2, 5)和GO-850的ORR电化学数据 Table 1 ORR electrochemical data for S-n-850(n=1, 2, 5) and GO-850 |
使用RDE测试催化剂S-n-850(n=1, 2, 5)在不同转速下的LSV曲线及在不同电压下的K-L曲线附在补充材料中(如图S1所示)。在极限扩散区域,同一个催化剂的极限电流密度随着转速的减小而减小,不同转速下的LSV曲线基本平行;在同一电压下,不同转速的电流密度几乎等间距,i-1和ω-1/2呈现出良好的线性关系[27]。
2.2.2 热处理温度对ORR活性影响将前驱体S-2在N2气氛保护下分别于750℃和950℃进行与催化剂S-2-850相同的热处理,得到催化剂S-2-750和S-2-950。
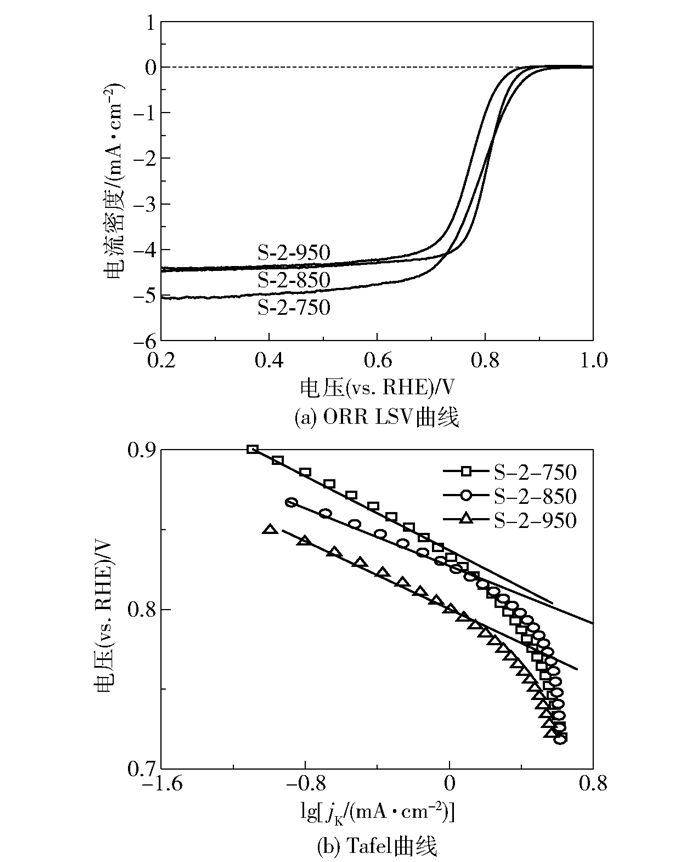
图 5 (a)是S-2-t (t=750, 850, 950)的LSV曲线。表 2是S-2-t的ORR电化学数据。催化剂S-2-750、S-2-850和S-2-950的起始电位分别为0.895V、0.871V和0.850V,半波电位分别为0.786V、0.804V和0.770V。催化剂S-2-850的半波电位最高,说明其相比于另外两种催化剂具有更好的ORR催化活性。图 5 (b)是催化剂S-2-t ORR性能的Tafel曲线。各个催化剂的Tafel斜率大小关系为:S-2-850 < S-2-950 < S-2-750,说明S-2-850在ORR催化过程中依然具有较快的动力学过程。
|
图 5 催化剂S-2-t在1600r/min下的LSV曲线和Tafel曲线 Fig.5 ORR LSV curves and Tafel curves of the S-2-t catalysts with an electrode rotation rate of 1600r/min |
| 下载CSV 表 2 S-2-t和20% Pt/C的ORR电化学数据 Table 2 ORR electrochemical data for S-2-t and 20% Pt/C |
采用相同方法测试20% Pt/C的ORR催化性能,即不同转速下的LSV曲线及K-L曲线,结果如补充材料中的图S4所示,可以得出20% Pt/C的起始电位和半波电位分别为0.940V和0.840V。
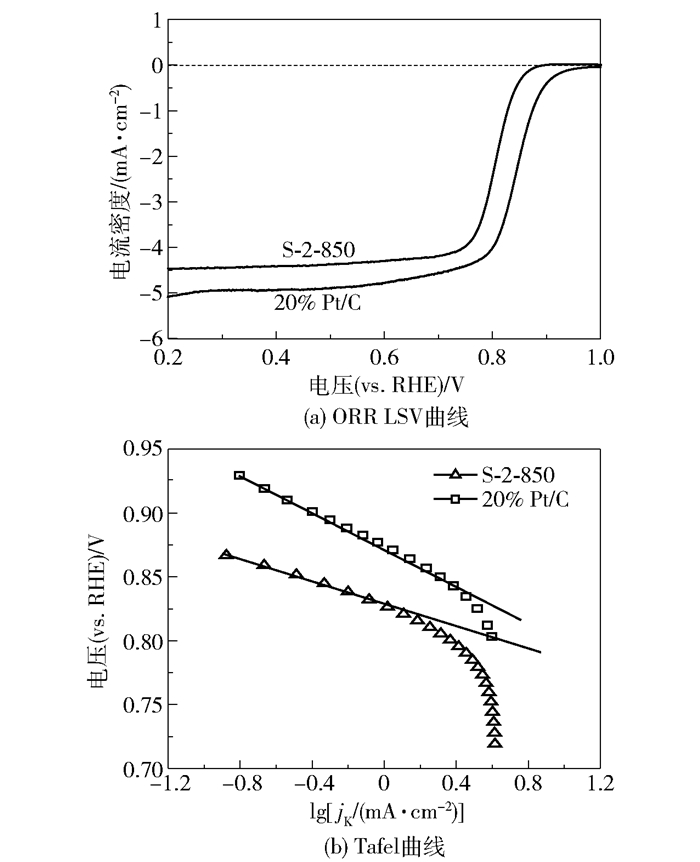
图 6(a)是S-2-850和20% Pt/C的LSV曲线。可以看出,S-2-850的半波电位小于20% Pt/C的半波电位,表明在ORR催化性能方面,S-2-850仍比不上商用20% Pt/C。图 6(b)是S-2-850和20% Pt/C的ORR性能的Tafel曲线。20% Pt/C的Tafel斜率为68.1mV/dec,高于催化剂S-2-850的49.6mV/dec,表明与商用20% Pt/C相比,S-2-850有较快的动力学过程。采用Tafel拟合方程η=a+blgi (a=(2.3RTlgi0)/αnαF; b=-2.3RT/αnαF),计算催化剂的动力学参数。对于20% Pt/C,a=0.356V,b=68.1mV/dec,i0=5.92×10-3mA/cm2;对于S-2-850,a=0.399V,b=49.6mV/dec,i0=9.03×10-6mA/cm2。可见,催化剂S-2-850的交换电流密度与20% Pt/C相比仍有一定差距。然而在陈君等[28]的研究中,ORR催化活性表现最好的是Co- ZnO(1:2)@CN-800纳米催化剂,其起始电位和半波电位分别为0.90V和0.78V,与本文的S-2-850相比,两者的起始电位十分接近,而催化剂S-2-850的半波电位达到了0.804V,高于Co-ZnO(1:2) @CN-800的半波电位。
|
图 6 S-2-850和20% Pt/C的ORR LSV曲线和Tafel曲线 Fig.6 ORR LSV and Tafel curves of S-2-850 and 20% Pt/C |
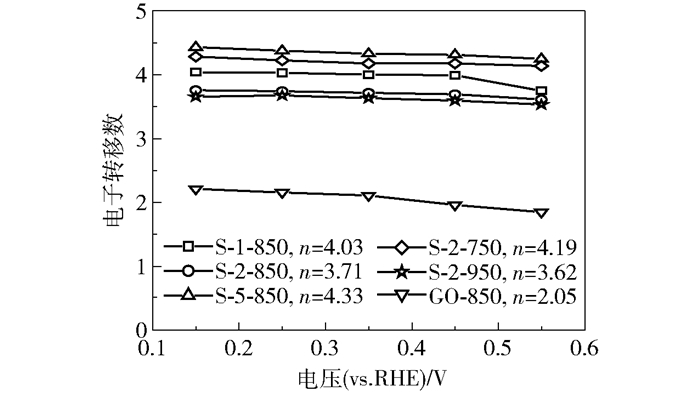
根据拟合的K-L方程计算各个催化剂的理论电子转移数如图 7所示。可以看出,电位0.15 ~ 0.55V范围内,催化剂GO-850的电子转移数为2.05,因此该范围内的ORR反应为2电子反应途径。而加入GO的S-n-t (n=1, 2, 5;t=750, 850, 950)催化剂的电子转移数均接近4,可见催化剂S-n-t主要为4电子反应途径。
|
图 7 不同催化剂的电子转移数 Fig.7 Number of electrons transferred for different catalysts |
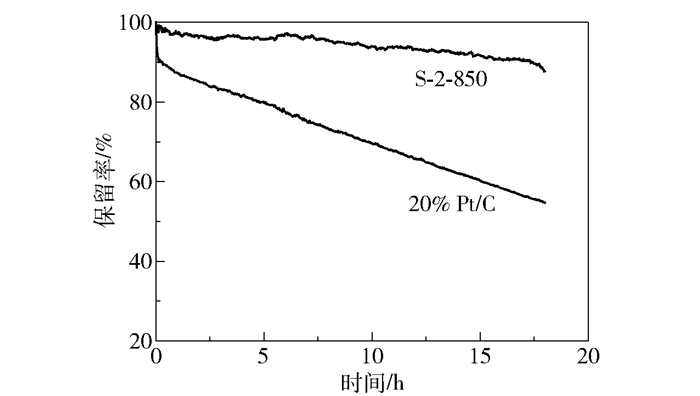
采用计时电流法测试催化剂S-2-850的ORR活性稳定性,作为对比,也在相同条件下测试了20% Pt/C的ORR活性稳定性,结果如图 8所示。经过64800s之后,催化剂S-2-850的放电电流保持在初始电流的87.7%;而20% Pt/C的放电电流仅保持在初始电流的54.7%,表明催化剂S-2-850的活性稳定性要优于20% Pt/C。
|
图 8 催化剂的ORR计时电流曲线 Fig.8 Chronoamperometric responses for the ORR with different catalysts |
通过搅拌反应法可合成ZIF(ZnCo)与GO复合材料,在N2气氛下热处理得到了一系列不同配比和处理温度的Co@N-doped rGO催化剂。实验结果表明,合成Co@N-doped rGO的Co与GO的最佳质量比为1.77,最佳热处理温度为850℃;所制备的催化剂S-2-850的起始电位和半波电位分别为0.871V和0.804V,电子转移数接近一级反应4电子转移路径,具有较高的ORR催化活性。虽然本文催化剂的活性仍不如商用20% Pt/C,但通过更为深入系统的研究,将有可能制备出更高效的基于ZIFs的电催化剂。
| [1] |
AURBACH D, MCCLOSKEY B D, NAZAR L F, et al. Advances in understanding mechanisms underpinning lithium-air batteries[J]. Nature Energy, 2016, 1(9): 16128. DOI:10.1038/nenergy.2016.128 |
| [2] |
ABRAHAM K M, JIANG Z. A polymer electrolyte-based rechargeable lithium/oxygen battery[J]. Journal of the Electrochemical Society, 1996, 143(1): 1-5. |
| [3] |
SHAO M H, PELES A, SHOEMAKER K. Electrocatalysis on platinum nanoparticles:particle size effect on oxygen reduction reaction activity[J]. Nano Letters, 2011, 11(9): 3714-3719. DOI:10.1021/nl2017459 |
| [4] |
GUO S J, ZHANG S, SU D, et al. Seed-mediated synthesis of core/shell FePtM/FePt (M=Pd, Au) nanowires and their electrocatalysis for oxygen reduction reaction[J]. Journal of the American Chemical Society, 2013, 135(37): 13879-13884. DOI:10.1021/ja406091p |
| [5] |
LIM H D, LEE B, BAE Y, et al. Reaction chemistry in rechargeable Li-O2 batteries[J]. Chemical Society Reviews, 2017, 46(10): 2873-2888. DOI:10.1039/C6CS00929H |
| [6] |
杨洋, 马雨蒙, 李朋伟, 等. 非贵金属氧还原电催化剂的研究进展[J]. 电池, 2018, 48(1): 56-59. YANG Y, MA Y M, LI P W, et al. Research progress in non-precious metal electrocatalyst for oxygen reduction reaction[J]. Battery Bimonthly, 2018, 48(1): 56-59. (in Chinese) |
| [7] |
WANG H, YIN F X, LI G R, et al. Preparation, characterization and bifunctional catalytic properties of MOF(Fe/Co) catalyst for oxygen reduction/evolution reactions in alkaline electrolyte[J]. International Journal of Hydrogen Energy, 2014, 39(28): 16179-16186. DOI:10.1016/j.ijhydene.2013.12.120 |
| [8] |
WANG H L, LIANG Y Y, LI Y G, et al. Co1-x S-graphene hybrid:a high-performance metal chalcogenide electro-catalyst for oxygen reduction[J]. Angewandte Chemie International Edition, 2011, 50(46): 10969-10972. DOI:10.1002/anie.v50.46 |
| [9] |
CAO B F, VEITH G M, DIAZ R E, et al. Cobalt molybdenum oxynitrides:synthesis, structural characterization, and catalytic activity for the oxygen reduction reaction[J]. Angewandte Chemie International Edition, 2013, 52(41): 10753-10757. DOI:10.1002/anie.201303197 |
| [10] |
SUN T, WU Q, ZHUO O, et al. Manganese oxide-induced strategy to high-performance iron/nitro gen/carbon electrocatalysts with highly exposed active sites[J]. Nanoscale, 2016, 8(16): 8480-8485. DOI:10.1039/C6NR00760K |
| [11] |
YU D S, ZHANG Q, DAI L M. Highly efficient metal-free growth of nitrogen-doped single-walled carbon nanotubes on plasma-etched substrates for oxygen reduction[J]. Journal of the American Chemical Society, 2010, 132(43): 15127-15129. DOI:10.1021/ja105617z |
| [12] |
SONG G Q, WANG Z Q, WANG L, et al. Preparation of MOF (Fe) and its catalytic activity for oxygen reduction reaction in an alkaline electrolyte[J]. Chinese Journal of Catalysis, 2014, 35(2): 185-195. DOI:10.1016/S1872-2067(12)60729-3 |
| [13] |
ZHANG M D, DAI Q B, ZHENG H G, et al. Novel MOF-derived Co@N-C bifunctional catalysts for highly efficient Zn-air batteries and water splitting[J]. Advanced Materials, 2018, 30(10): 1705431. DOI:10.1002/adma.v30.10 |
| [14] |
WANG H, YIN F X, LV P L, et al. Metal-organic-framework-derived FeCo alloy core@nitrogen-doped carbon shell nanoparticles anchored on carbon nanotubes for rechargeable Li-O2 battery[J]. International Journal of Hydrogen Energy, 2017, 42(4): 2127-2133. DOI:10.1016/j.ijhydene.2016.11.118 |
| [15] |
WANG X J, ZHANG H G, LIN H H, et al. Directly converting Fe-doped metal-organic frameworks into highly active and stable Fe-N-C catalysts for oxygen reduction in acid[J]. Nano Energy, 2016, 25: 110-119. DOI:10.1016/j.nanoen.2016.04.042 |
| [16] |
WEI J, HU Y X, LIANG Y, et al. Nitrogen-doped nanoporous carbon/graphene nano-sandwiches:synthesis and application for efficient oxygen reduction[J]. Advanced Functional Materials, 2015, 25(36): 5768-5777. DOI:10.1002/adfm.201502311 |
| [17] |
HE X B, YIN F X, LI G R. A Co/metal-organic-framework bifunctional electrocatalyst:the effect of the surface cobalt oxidation state on oxygen evolution/reduction reactions in an alkaline electrolyte[J]. International Journal of Hydrogen Energy, 2015, 40(31): 9713-9722. DOI:10.1016/j.ijhydene.2015.06.027 |
| [18] |
YI Q F, ZHANG Y H, LIU X P, et al. Carbon-supported Fe/Co-N electrocatalysts synthesized through heat treatment of Fe/Co-doped polypyrrole-polyaniline composites for oxygen reduction reaction[J]. Science China Chemistry, 2014, 57(5): 739-747. DOI:10.1007/s11426-013-5027-1 |
| [19] |
SANKARASUBRAMANIAN S, SEO J, MIZUNO F, et al. Elucidating the oxygen reduction reaction kinetics and the origins of the anomalous Tafel behavior at the lithium-oxygen cell cathode[J]. The Journal of Physical Chemistry C, 2017, 121(9): 4789-4798. DOI:10.1021/acs.jpcc.6b09747 |
| [20] |
司玉军, 熊中平, 李敏娇, 等. 氧化石墨制备氮掺杂氧还原反应电催化剂[J]. 电源技术, 2018, 42(1): 58-60, 64. SI Y J, XIONG Z P, LI M J, et al. Prepared electrocatalyst by oxidized graphite for nitrogen doping oxygen reduction reaction[J]. Chinese Journal of Power Sources, 2018, 42(1): 58-60, 64. (in Chinese) DOI:10.3969/j.issn.1002-087X.2018.01.016 |
| [21] |
CHO J U, WU J H, MIN J H, et al. Control of magnetic anisotropy of Co nanowires[J]. Journal of Magnetism and Magnetic Materials, 2006, 303(2): e281-e285. DOI:10.1016/j.jmmm.2006.01.082 |
| [22] |
WANG H L, HAO Q L, YANG X J, et al. Graphene oxide doped polyaniline for supercapacitors[J]. Electroch-emistry Communications, 2009, 11(6): 1158-1161. DOI:10.1016/j.elecom.2009.03.036 |
| [23] |
WEI J, HU Y X, LIANG Y, et al. Graphene oxide/core-shell structured metal-organic framework nano-sandwiches and their derived cobalt/N-doped carbon nanosheets for oxygen reduction reactions[J]. Journal of Materials Chemistry A, 2017, 5(21): 10182-10189. DOI:10.1039/C7TA00276A |
| [24] |
成巍, 陈彩玲, 于影, 等. 基于ZIFs合成的中空双金属(Zn, Co)S纳米晶及其赝电容性质研究[J]. 高等学校化学学报, 2017, 38(8): 1303-1308. CHENG W, CHEN C L, YU Y, et al. Facile synthesis of ZIFs-derived hollow bimetal (Zn, Co)S nanocrystals for supercapacitors[J]. Chemical Journal of Chinese Univer sities, 2017, 38(8): 1303-1308. (in Chinese) |
| [25] |
WANG M Y, WANG Q, ZHU W, et al. Metal porphyrin intercalated reduced graphene oxide nanocomposite utilized for electrocatalytic oxygen reduction[J]. Green Energy & Environment, 2017, 2(3): 285-293. |
| [26] |
CHEN B H, HE X B, YIN F X, et al. MO-Co@N-doped carbon (M=Zn or Co):vital roles of inactive Zn and highly efficient activity toward oxygen reduction/evolution reactions for rechargeable Zn-air battery[J]. Advanced Functional Materials, 2017, 27(37): 1700795. DOI:10.1002/adfm.v27.37 |
| [27] |
LI T F, PENG Y X, LI K, et al. Enhanced activity and stability of binuclear iron (Ⅲ) phthalocyanine on graphene nanosheets for electrocatalytic oxygen reduction in acid[J]. Journal of Power Sources, 2015, 293: 511-518. DOI:10.1016/j.jpowsour.2015.05.099 |
| [28] |
陈君, 隆继兰. 双中心MOFs衍生的Co-ZnO@CN纳米材料作为电化学催化剂用于氧还原反应的研究[J]. 分子催化, 2017, 37(5): 463-471. CHEN J, LONG J L. Bi-centered MOFs-derived Co-ZnO@CN nano-material as efficient electrocatalyst for oxygen reduction reaction[J]. Journal of Molecular Catalysis (China), 2017, 37(5): 463-471. (in Chinese) |








